Unterschied zwischen wässriger und nichtwässriger Lösung
Der Schlüsselunterschied zwischen wässriger und nichtwässriger Lösung ist das Die Lösungsmittel einer wässrigen Lösung ist Wasser, während in nichtwässrigen Lösungen das Lösungsmittel eine andere Substanz als Wasser ist.
Eine Lösung enthält ein Lösungsmittel und einen gelösten Stoff (en). Die gelösten Stoffe werden im Lösungsmittel aufgelöst. Hier sollten die gelösten Stoffe und das Lösungsmittel die gleiche Polarität haben. Wenn das Lösungsmittel polar ist und gelöste Stoffe nichtpolar oder umgekehrt, lösen sich die gelösten Stoffe nicht im Lösungsmittel, und wir können keine Lösung erhalten.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist wässrige Lösung
3. Was ist eine nichtwässrige Lösung
4. Seite an Seitenvergleich - wässrige gegen nichtwässrige Lösung in tabellarischer Form
5. Zusammenfassung
Was ist eine wässrige Lösung?
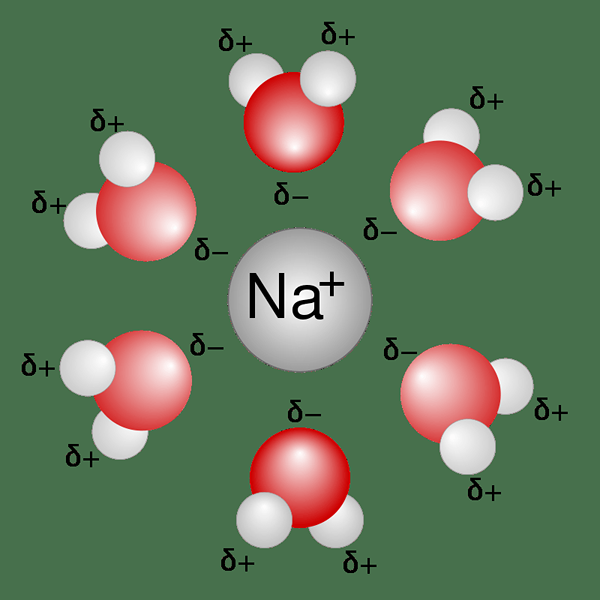
Eine wässrige Lösung ist jede Lösung, die Wasser als Lösungsmittel enthält. Hier müssen die gelösten Stoffe hydrophil und polar sein, um sich in Wasser aufzulösen, um eine wässrige Lösung zu ergeben. Obwohl wir Wasser als universelles Lösungsmittel nennen, können wir uns nicht fast alles darin auflösen. Zum Beispiel können wir Fett in Wasser nicht auflösen.

Abbildung 01: Natriumionen im Wasser
Beim Schreiben einer chemischen Gleichung verwenden wir das Symbol (AQ) als Index, um anzuzeigen, dass die Substanz in einer wässrigen Lösung liegt. Wenn sich der gelöste Stoff beim Auflösen in Wasser in Ionen dissen kann, sagen wir, dass eine wässrige Lösung leitfähig ist, da sie aufgrund des Vorhandenseins von Ionen Strom durch die Lösung leiten kann.
Was ist eine nichtwässrige Lösung?
Eine nichtwässrige Lösung ist eine Lösung, die wir erhalten, indem wir einen gelösten Stoff in einem anderen Lösungsmittel als Wasser auflösen. Das Lösungsmittel kann eine organische Verbindung wie Aceton, Toluol, Ether, Alkohol, Benzol usw. sein.

Abbildung 02: Jod in Alkohol
Das Lösungsmittel kann polar oder unpolar sein und je nach Polarität, während sich gelöste Stoffe im Lösungsmittel auflösen. Lösungen von Jod in Alkohol und Lösungen von Jod in Kohlenstofftetrachlorid sind Beispiele für nichtwässrige Lösungen.
Was ist der Unterschied zwischen wässriger und nichtwässriger Lösung?
Wir können Lösungen je nach Lösungsmittel in zwei Gruppen als wässrig und nichtwässrig unterteilen. Der Hauptunterschied zwischen wässriger und nichtwässriger Lösung besteht darin, dass das Lösungsmittel einer wässrigen Lösung Wasser ist, während in nichtwässrigen Lösungen das Lösungsmittel eine andere Substanz als Wasser ist. Wässrige Lösungen von Natriumchlorid, wässrigem Ammoniak usw. sind Beispiele für wässrige Lösungen, während Jodlösungen in Alkohol, Jodlösungen in Kohlenstofftetrachlorid usw. sind nichtwässrige Lösungen.

Zusammenfassung -wässrige gegen nichtwässrige Lösung
Grundsätzlich können wir Lösungen je nach Lösungsmittel in zwei Gruppen als wässrig und nichtwässrig unterteilt. Der Hauptunterschied zwischen wässriger und nichtwässriger Lösung besteht darin, dass das Lösungsmittel einer wässrigen Lösung Wasser ist, während in nichtwässrigen Lösungen das Lösungsmittel eine andere Substanz als Wasser ist.
Referenz:
1. Helmenstine, Anne Marie. „Definition der wässrigen Lösung in der Chemie.”Thoughtco, Jan. 13, 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Na+H2O" von Taxman -(Public Domain) über Commons Wikimedia
2. "J Crows Lugol's Jod 2" von Amin - eigene Arbeit (CC BY -SA 4.0) über Commons Wikimedia


