Unterschied zwischen Azeotrop und Rohstoffdestillation
Schlüsselunterschied - Azeotropic vs Rohstoff Destillation
Der Schlüsselunterschied Zwischen der azeotropen und der extraktiven Destillation ist das in der azeotropen Destillation, Die Bildung eines Azeotrops ist erforderlich, um die Komponenten einer Mischung zu trennen, während in der extraktiv.
Destillation ist der Prozess der Reinigung einer Flüssigkeit durch einen Erwärmungs- und Kühlprozess. In der azeotropen Destillation wird vor der Trennung von Komponenten von einer Mischung ein Azeotrop gebildet. Ein Azeotrope ist eine Mischung von Komponenten mit einem konstanten Siedepunkt. Im extraktiven Destillationsprozess besteht keine Notwendigkeit, ein Azeotrop zu bilden. Bei dieser Methode wird eine dritte Komponente zu einer binären Mischung hinzugefügt. Diese dritte Komponente kann die Volatilität vorhandener Komponenten beeinflussen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist die azeotrope Destillation
3. Was ist eine extraktive Destillation
4. Seite an Seitenvergleich - Azeotrope und extraktive Destillation in tabellarischer Form
5. Zusammenfassung
Was ist die azeotrope Destillation?
Azeotrope Destillation ist eine Trennungstechnik, mit der die Komponenten einer Mischung durch Bildung eines Azeotrops getrennt werden. Azeotrope sind Komponentenmischungen mit einem konstanten Siedepunkt. Diese Art von Mischung kann nicht durch einfache Destillation in Komponenten unterteilt werden, da alle Komponenten den gleichen Siedepunkt haben. Wenn ein azeotropes Gemisch gekocht wird, ist der Anteil der Komponenten in der Flüssigkeit und der Dampfphase gleich.
Bei der Azeotropen -Destillationsmethode wird eine neue Komponente (bekannt als Mitnahme) zum azropen Gemisch hinzugefügt, um ein neues Azeotrop zu bilden, das bei einer niedrigeren Temperatur kocht als die vorhandene Azeotrope. Dann hat das System zwei nicht mischbare flüssige Phasen mit unterschiedlichen Siedepunkten (heterogen).

Abbildung 01: Das System der Trennung von Ethanol (E) von Wasser (W) unter Verwendung von Benzol (b)
Betrachten wir zum Beispiel eine Mischung aus Ethanol und Wasser. Es ist bekannt als a Binärer Azeotrop Weil es zwei mischbare Komponenten in der Mischung gibt. Wenn Benzol als Unternehmer zu diesem Gemisch hinzugefügt wird, kann es die Volatilität anderer Komponenten in der Mischung beeinflussen. Die Mischung wird jetzt als Tertiär -Azeotrop bezeichnet, da in der Mischung drei Komponenten enthalten sind. Wenn diese Mischung destilliert ist, ist es als azeotrope Destillation bekannt.
Was ist eine extraktive Destillation?
Die extraktive Destillation ist eine Trennungstechnik, die die Zugabe einer dritten Komponente zu einer binären Mischung umfasst, um die Trennung der beiden Komponenten zu ermöglichen. Die dritte Komponente verdampft jedoch während des Destillationsprozesses nicht; Die dritte Komponente sollte weniger volatil sein. Oder sollte es einen höheren Siedepunkt haben.
Wenn das binäre Gemisch zwei Komponenten mit relativ ähnlichen Siedepunkten aufweist, können diese Komponenten nicht durch einfache Destillation getrennt werden. Dies geschieht, da beide Komponenten bei nahezu ähnlichen Temperaturen verdampft werden (schlechte Auflösung).
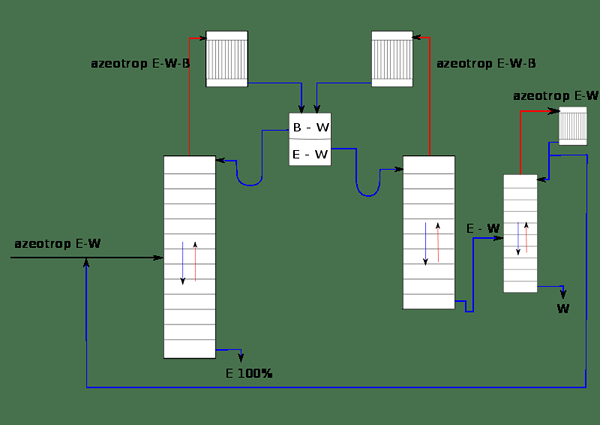
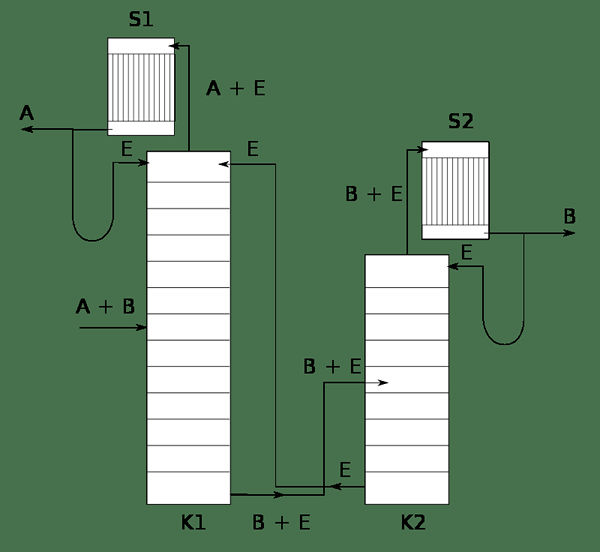
Abbildung 02: Ein System, das die extraktive Destillation der A- und B -Mischung unter Verwendung von E -Lösungsmittel zeigt
Während des extraktiven Destillationsprozesses wird kein Azeotrop gebildet. Der Prozess beinhaltet ein Lösungsmittel mit einer sehr geringen Volatilität als Lösungsmittel des Komponentengemisches. Es ist als Trennungslösungsmittel bekannt. Während der Destillation wird die Komponente mit höchster Volatilität leicht als oberes Produkt verdampft. Der Rest ist das Lösungsmittel und die andere Komponente (in der binären Mischung). Da das Lösungsmittel kein Azeotrop mit der zweiten Komponente bildet, kann es auch leicht mit einer verfügbaren Methode getrennt werden.
Beispielsweise kann die Extraktion von Toluol aus Paraffin in der extraktiven Destillationsmethode erfolgen. Die Mischung aus Toluol und Iso-Oktan hat nahezu ähnliche molekulare Gewichte. Daher ist die Trennung von Toluol aus dieser Mischung sehr schwierig. Aber wenn Phenol zu dieser Mischung hinzugefügt wird, nimmt der Siedepunkt von Iso-Oktan zu. Dies erleichtert es einfach, Toluol von dieser Mischung zu trennen.
Was ist der Unterschied zwischen azeotropem und extraktiver Destillation?
Azeotrope vs extraktive Destillation | |
| Azeotrope Destillation ist eine Trennungstechnik, mit der die Komponenten einer Mischung durch Bildung eines Azeotrops getrennt werden. | Die extraktive Destillation ist eine Trennungstechnik, die die Zugabe einer dritten Komponente zu einer binären Mischung umfasst, um die Trennung der beiden Komponenten zu ermöglichen. |
| Technik | |
| Bei der Azeotropendestillationstechnik ist die Bildung eines Azeotrops vor der Destillation wichtig. | In der extraktiven Destillationstechnik wird der Mischung eine nichtflüchtige Komponente zugesetzt. |
| Trennung | |
| Die azeotrope Destillation trennt eine Komponente in die Dampfphase, die die gleiche chemische Zusammensetzung wie in der Flüssigkeitsphase aufweist. | Die extraktive Destillation trennt eine Komponente von einer Substanzenmatrix. |
Zusammenfassung - Azeotropic vs Rohstoff Destillation
Destillation ist eine chemische Technik, die zur Trennung verschiedener Komponenten in einer Mischung verwendet wird. Es gibt viele Arten von Destillationstechniken, wobei die einfache Destillation der einfachste Typ ist. Azeotrope Destillation und extraktive Destillation sind zwei wichtige Arten der Destillation. Der Unterschied zwischen der Azeotropen und der extraktiv.
Referenz:
1. „Azeotrope Destillation.”Wikipedia, Wikimedia Foundation, 4. April. 2018. Hier verfügbar
2. „Rohige Destillation.Wikipedia, Wikimedia Foundation, 14. Januar. 2018. Hier verfügbar
3. „Azeotrope.”Wikipedia, Wikimedia Foundation, 8. April. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.'Distil Extract'by Joanna Kośmider - eigene Arbeit, (Public Domain) über Commons Wikimedia
2.'Azeotr Distill2'by Joanna Kośmider - eigene Arbeit, (öffentlich zugänglich) über Commons Wikimedia


