Unterschied zwischen Butan und Butene
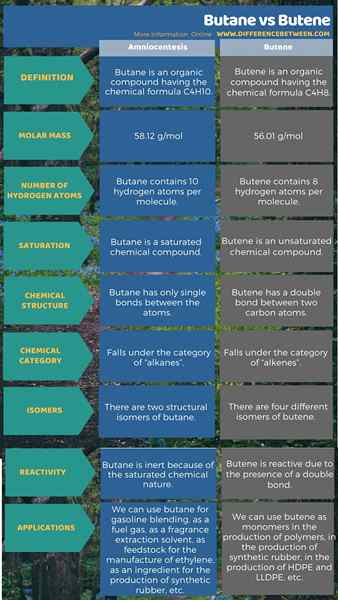
Der Schlüsselunterschied Zwischen Butan und Buten ist das die Butan hat keine doppelten oder dreifachen Bindungen zwischen Kohlenstoffatomen, während das Buten eine doppelte Bindung zwischen Kohlenstoffatomen enthält.
Butan und Buten sind organische Verbindungen mit vier Kohlenstoffatomen pro Molekül. Sie haben jedoch Unterschiede in ihren chemischen Strukturen wie ihrer chemischen Bindung und einer Reihe von Wasserstoffatomen. Daher haben sie auch unterschiedliche chemische und physikalische Eigenschaften.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Butan
3. Was ist Butene
4. Seite an Seite Vergleich - Butan gegen Buten in tabellarischer Form
5. Zusammenfassung
Was ist Butan?
Butan ist eine organische Verbindung mit der chemischen Formel C4H10. Es ist ein Alkan; Somit ist es eine gesättigte Verbindung. Daher gibt es zwischen den Atomen dieses Moleküls keine doppelten oder dreifachen Bindungen. Es existiert als Gas bei Raumtemperatur und Druck. Diese Verbindung hat vier Kohlenstoffatome und 10 Wasserstoffatome. Diese Atome ordnen entweder in einer linearen Struktur oder in einer verzweigten Struktur an. Wir nennen die lineare Struktur als "n-Butane" und die verzweigte Struktur als "Isobuten". Nach dem IUPAC -Nomenklatursystem bezieht sich der Begriff Butan jedoch auf die lineare Form. Isobuten hat einen Methylzweig, der an einem Drei-Kohlenstoff-Rückgrat befestigt ist.
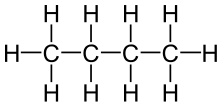
Abbildung 01: Chemische Struktur von N-Butan
Die Molmasse dieses Gases beträgt 58.12 g/mol. Es ist ein farbloses Gas. Es hat einen benzinähnlichen Geruch. Das Schmelzen und die Siedepunkte betragen –134 ° C bzw. 1 ° C. Darüber hinaus ist dieses Gas ein hochflammbares und leicht verflüssigtes Gas. Bei der Verflüssigung verdampft es schnell bei Raumtemperatur. Wenn es genügend Sauerstoff gibt, verbrennt dieses Gas, das Kohlendioxid und Wasserdampf ergibt. Aber wenn die Sauerstoffmenge begrenzt ist, bildet er auch Kohlenstoffruhr und Kohlenmonoxid; aufgrund unvollständiger Verbrennung.
Wenn wir die Verwendung von Butan in Betracht ziehen, können wir es für Benzinmischungen als Brennstoffgas als Duft -Extraktionslösungsmittel als Ausgangsmaterial für die Herstellung von Ethylen als Inhaltsstoff für die Herstellung von synthetischen Gummi usw. verwenden.
Was ist Butene?
Butene ist eine organische Verbindung mit der chemischen Formel C4H8. "Butylen" ist ein Synonym für dieselbe Verbindung. Diese Verbindung hat vier Kohlenstoffatome und 8 Wasserstoffatome. Es gibt eine doppelte Bindung zwischen zwei Kohlenstoffatomen. Daher ist es eine ungesättigte Verbindung. Es fällt unter die Kategorie der Alkene. Es ist ein farbloses Gas bei Raumtemperatur und Druck. Wir können dieses Gas als kleinere Bestandteil des Rohöls finden. Somit können wir diese Verbindung über katalytisches Rissen in einer Raffinerie erhalten.
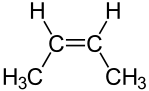
Abbildung 02: (2Z) -but-2-enge Isomer von Butene
Aufgrund des Vorhandenseins der Doppelbindung hat diese Verbindung Isomere. Es gibt vier große Isomere; Sie sind, aber 1-en, (2Z) -but-2-en, (2E) -but-2-en und 2-methylprop-1-en (Isobutylen). All diese Isomere existieren als Gase. Wir können sie mit zwei Methoden verflüssigen; Wir können die Temperatur senken oder den Druck erhöhen. Diese Gase haben unterschiedliche Gerüche. Darüber hinaus sind sie sehr entflammbar. Die Doppelbindung macht diese Verbindungen reaktiver als die Alkane mit einer ähnlichen Anzahl von Kohlenstoffatomen. Bei der Betrachtung der Anwendungen dieser Verbindung können wir sie als Monomere in der Herstellung von Polymeren, bei der Herstellung von synthetischen Gummi, bei der Herstellung von HDPE und LLDPE usw. verwenden.
Was ist der Unterschied zwischen Butan und Butene?
Butan ist eine organische Verbindung mit der chemischen Formel C4H10 und Butene ist eine organische Verbindung mit der chemischen Formel C4H8. Beide sind organische Verbindungen, die vier Kohlenstoffatome und unterschiedliche Anzahl von Wasserstoffatomen enthalten. Hauptsächlich ist der Hauptunterschied zwischen Butan und Buten in ihren chemischen Strukturen. Das heißt, eine Doppelbindung ist im Buten vorhanden, fehlt aber in Butan. Darüber hinaus macht dies Butene reaktiver. Darüber hinaus hat Butene vier verschiedene Isomere, während Butan nur zwei Isomere hat.
Die folgende Infografik enthält weitere Details zum Unterschied zwischen Butan und Butenein -Tabellformform.

Zusammenfassung -Butan gegen Butene
Butan und Buten sind organische Verbindungen, die als Gase bei Raumtemperatur und Druck existieren. Der Hauptunterschied zwischen Butan und Buten besteht darin, dass der Butan keine doppelten oder dreifachen Bindungen zwischen Kohlenstoffatomen hat, während das Buten eine doppelte Bindung zwischen Kohlenstoffatomen enthält.
Referenz:
1. "Butan.”Wikipedia, Wikimedia Foundation, 22. August. 2018. Hier verfügbar
2. „Butene.”Wikipedia, Wikimedia Foundation, 22. August. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1."Butan Lewis" von Neurotiker ⇌ - eigene Arbeit, (Public Domain) über Commons Wikimedia
2.”Cis-2-buten” von Neurotiker-eigene Arbeit (öffentlich zugänglich) über Commons Wikimedia


