Unterschied zwischen CIS und Trans -Isomeren
Der Schlüsselunterschied Zwischen cis und trans -Isomeren befindet sich die CIS Isomer hat die gleichen Atome auf derselben Seite der Doppelbindung, während das Trans -Isomer zwei der gleichen Atome auf den gegenüberliegenden Seiten der Doppelbindung aufweist.
Isomere sind unterschiedliche Verbindungen mit der gleichen molekularen Formel. Es gibt verschiedene Arten von Isomeren. Aber wir können die Isomere hauptsächlich als konstitutionelle Isomere und Stereoisomere in zwei Gruppen einteilen. Hier sind die konstitutionellen Isomere Isomere, bei denen sich die Konnektivität von Atomen in Molekülen unterscheidet. In Stereoisomeren verbinden sich Atome im Gegensatz zu konstitutionellen Isomeren in derselben Reihenfolge. Daher unterscheiden sich Stereoisomere nur in der Anordnung ihrer Atome im Weltraum. Außerdem sind Stereoisomere von zwei Arten; Enantiomere und Diastereomere. Darüber hinaus sind CIS und Trans Isomere die beiden Formen von Diastereomeren.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind cis isomere
3. Was sind Trans -Isomere
4. Seite für Seitenvergleich - cis vs Trans Isomere in tabellarischer Form
5. Zusammenfassung
Was sind cis isomere?
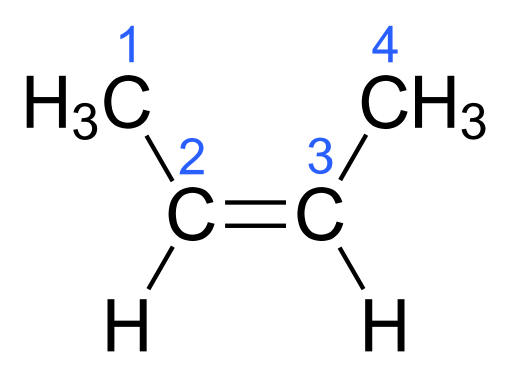
Das Molekül, bei dem zwei der gleichen Atome auf der gleichen Seite der Doppelbindung liegen. Das CIS -Isomer hat einen höheren Siedepunkt im Vergleich zum Trans -Isomer. Der Grund dafür sind die stärkeren intermolekularen Kräfte in cis -Isomeren.

Abbildung 01: cis Isomer von Butene
Zum Beispiel in 1,2-Dichlorethan, wenn das Molekül cis ist, befinden sich zwei weitere elektronegative Chloratome auf einer Seite des Moleküls. Aus diesem Grund hat diese Seite des Moleküls eine geringfügige negative Ladung, während die andere Seite eine leichte positive Ladung hat. Daher kann das Molekül eine polare und Dipol-Dipol-Wechselwirkung zwischen Molekülen auftreten. Diese zusätzlichen intermolekularen Kräfte im cis -Isomer verleihen ihm einen höheren Siedepunkt im Vergleich zu Trans -Isomeren.
Was sind Trans -Isomere?
Ein Molekül mit zwei der gleichen Atome auf der gegenüberliegenden Seite der Doppelbindung ist der Trans -Isomer. Trans-Isomere haben niedrigere Siedepunkte, da das Gesamtmolekül, obwohl es eine Ladungstrennung gibt.
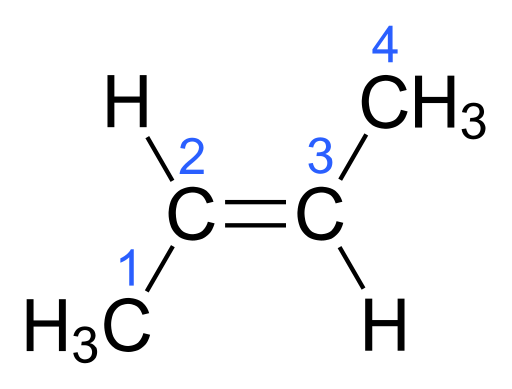
Abbildung 02: Trans Isomer von Butene
Trotzdem haben Trans -Isomere einen höheren Schmelzpunkt. Trans -Isomere haben eine geradere Form und sie packen gut ein. Daher erfordert es eine höhere Energie, um das Molekül zu schmelzen, das ihm einen höheren Schmelzpunkt verleiht.
Was ist der Unterschied zwischen CIS und Trans -Isomeren?
Das Molekül, bei dem zwei der gleichen Atome auf der gleichen Seite der Doppelbindung liegen. Andererseits ist ein Molekül mit zwei der gleichen Atome auf den gegenüberliegenden Seiten der Doppelbindung als Trans Isomer bekannt. Daher ist dies der Hauptunterschied zwischen CIS und Trans -Isomeren. Durch den Vergleich ihrer Eigenschaften können wir auch einen gewissen Unterschied zwischen CIS und Trans -Isomeren identifizieren. Die CIS-Isomere sind polar, während die Trans-Isomere vergleichsweise unpolar sind. Daher hat das CIS -Isomer den höheren Siedepunkt im Vergleich zu dem im trans -Isomer. Trans -Isomere haben jedoch einen höheren Schmelzpunkt; Im Gegensatz dazu haben cis -Moleküle einen niedrigeren Schmelzpunkt. Dies liegt hauptsächlich daran, dass die Transmoleküle gut gepackt sind als cis -Moleküle.
Die folgende Infografik zeigt den Unterschied zwischen cis und trans -Isomeren in tabellarischer Form.
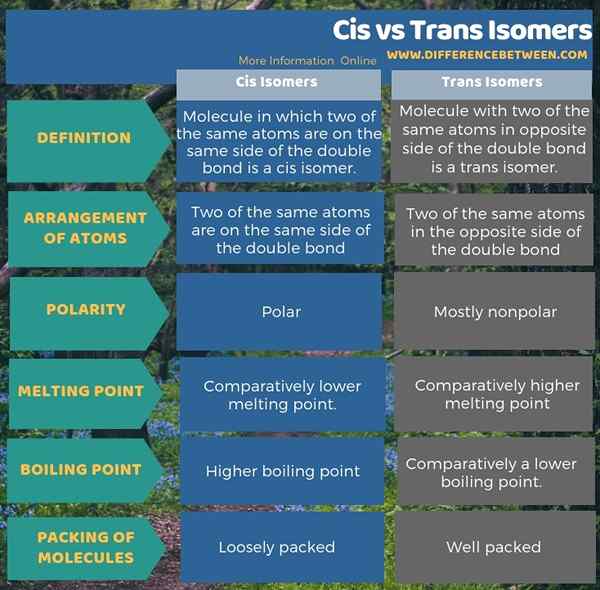
Zusammenfassung - cis vs Trans Isomere
Zusammenfassend lässt sich sagen. Der Hauptunterschied zwischen cis und trans -Isomeren besteht darin, dass das CIS -Isomer auf derselben Seite der Doppelbindung gleich.
Referenz:
1. „CIS-Trans-Isomerismus.Wikipedia, Wikimedia Foundation, 11. Juni 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”Cis-2-buten“ von Jaga-eigene Arbeit (CC BY-SA 3).0) über Commons Wikimedia
2."Trans-2-Butene" von Jaga-eigene Arbeit (CC BY-SA 3).0) über Commons Wikimedia


