Unterschied zwischen Stickstoffmonoxid und Dinitrogenpentoxid
Der Schlüsselunterschied Zwischen Stickstoffmonoxid und Dinitrogenpentoxid ist das Stickstoffmonoxid ist ein farbloses Gas, während Dinitrogenpentoxid ein weißer Feststoff ist.
Stickstoffmonoxid und Dinitrogenpentoxid sind chemische Verbindungen, die Stickstoff und Sauerstoff enthalten. Dies sind Oxide von Stickstoff. Sie haben jedoch unterschiedliche chemische und physikalische Eigenschaften.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Stickstoffmonoxid
3. Was ist Dinitrogenpentoxid
4. Seite für Seitenvergleich - Stickstoffmonoxid gegen Dinitrogenpentoxid in tabellarischer Form
5. Zusammenfassung
Was ist Stickstoffmonoxid?
Stickstoffmonoxid ist eine anorganische Verbindung mit der chemischen Formel Nr. Wir nennen es Stickoxid, da es ein Stickstoffoxid ist. Es ist tatsächlich ein freies Radikal, weil es ein ungepaartes Elektron hat. Darüber hinaus handelt es sich um ein heteronukleäres Diatommolekül.
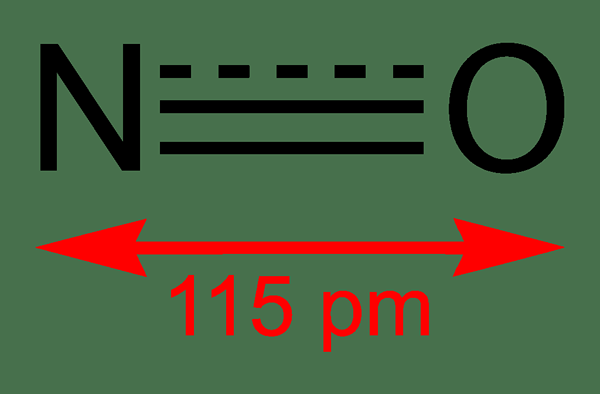
Abbildung 01: Stickstoffstruktur und die Bindungslänge zwischen N und O
Die Molmasse dieser Verbindung beträgt 30 g/mol. Es kommt als farbloses Gas vor. Darüber hinaus beträgt sein Schmelzpunkt –164 ° C, während der Siedepunkt –152 ° C beträgt, was im Vergleich zu denen anderer Oxide von Stickstoff sehr geringe Werte sind. Wir können dieses freie Radikal durch Oxidation von Ammoniak bei 850 ° C in Gegenwart eines Platinkatalysators produzieren. Auf der Laborskala können wir es jedoch durch die Verringerung der verdünnten Salpetersäure mit Kupfer vorbereiten.
Was ist Dinitrogenpentoxid?
Dinitrogenpentoxid ist eine anorganische Verbindung mit der chemischen Formel N2Ö5. Wir nennen es Stickstoffpentoxid. Es ist ein binäres Stickstoffoxid. Darüber hinaus ist es instabil und kann als gefährlicher Oxidationsmittel wirken. Die Molmasse der Verbindung ist 108.01 g/mol. Es tritt eine weiße Farbe fest.

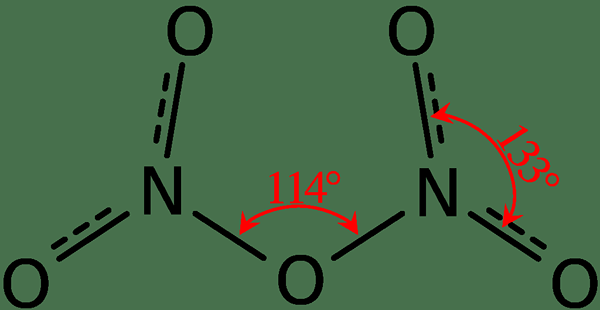
Abbildung 02: Struktur des Dinitickstoffpentoxids
Darüber hinaus beträgt der Schmelzpunkt dieser Verbindung 41 ° C und bei 47 ° C unterliegt diese Verbindung Sublimation. Diese Verbindung reagiert mit Wasser und ergibt Salpetersäure. Darüber hinaus ist die molekulare Form des Dinitrogenpentoxidmoleküls planar. Wir können diese Verbindung über dehydrierende Salpetersäure mit Phosphorpentoxid produzieren.
Was ist der Unterschied zwischen Stickstoffmonoxid und Dinitrogenpentoxid?
Stickstoffmonoxid ist eine anorganische Verbindung mit der chemischen Formel NO, während Dinitrogenpentoxid eine anorganische Verbindung mit der chemischen Formel n ist2Ö5. Der Hauptunterschied zwischen Stickstoffmonoxid und Dinitrogenpentoxid besteht darin. Darüber hinaus können wir Stickstoffmonoxid durch Oxidation von Ammoniak bei 850 ° C in Gegenwart eines Platinkatalysators produzieren. Die Produktion von Dinitrogenpentoxid erfolgt jedoch über dehydrierende Salpetersäure mit Phosphorpentoxid. Bei der Betrachtung der molekularen Form ist Stickstoffmonoxid linear, während Dinitrogenpentoxid planar ist.
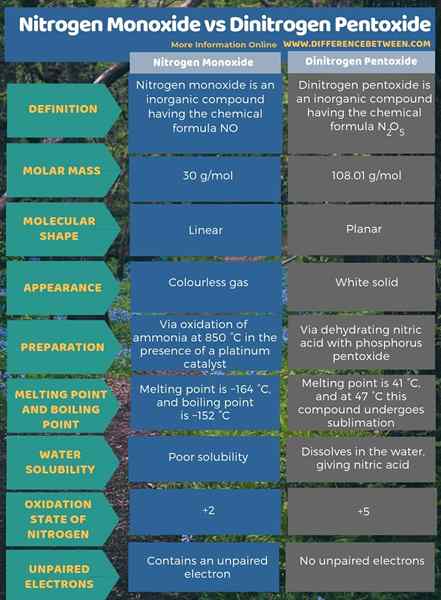
Zusammenfassung -Stickstoffmonoxid gegen Dinitrogenpentoxid
Stickstoffmonoxid ist eine anorganische Verbindung mit der chemischen Formel NO, während Dinitrogenpentoxid eine anorganische Verbindung mit der chemischen Formel n ist2Ö5. Der Hauptunterschied zwischen Stickstoffmonoxid und Dinitrogenpentoxid besteht darin.
Referenz:
1. Mowry, Curtis et al. „Materials Charakterisierungsaktivitäten für„ Nehmen Sie unsere Söhne und Töchter zum Arbeitstag “2013.Jan. 2013, doi: 10.2172/1096449.
Bild mit freundlicher Genehmigung:
1. "Ni-Oxid-2D" von Yiny. - Eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Dinitrogenpentoxid" von Krishnavedala - eigene Arbeit (Public Domain) über Commons Wikimedia


