Unterschied zwischen pH und Puffer
Der Schlüsselunterschied zwischen pH und Puffer ist, dass die PH ist eine logarithmische Skala, während ein Puffer eine wässrige Lösung ist.
Wir können den pH -Wert einer Flüssigkeit verwenden, um festzustellen, ob es sich um eine Säure oder eine Base handelt. Es ist auch hilfreich bei der Bestimmung der Pufferkapazität eines Puffer. Eine Pufferlösung enthält eine Mischung aus einer schwachen Säure und ihrer konjugierten Base oder umgekehrt. Daher neigt es dazu, Veränderungen im pH -Wert der Lösung zu widerstehen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist pH
3. Was ist Puffer
4. Seite für Seitenvergleich - pH -vs -Puffer in tabellarischer Form
5. Zusammenfassung
Was ist pH?
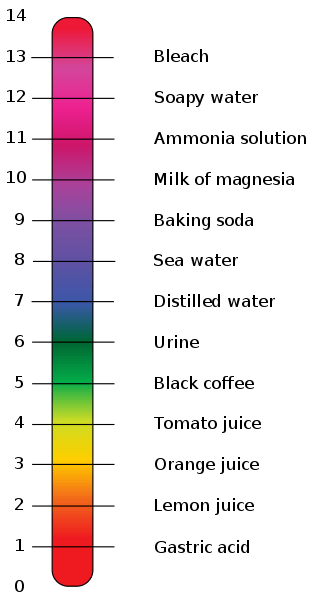
PH ist eine logarithmische Skala, die wir verwenden, um die Säure oder die Basizität einer wässrigen Lösung zu bestimmen. Es ist der negative Basis 10 Logarithmus der Wasserstoffionenkonzentration, gemessen in der Einheit mol/l. Wenn wir es genauer ausdrücken, sollten wir die Aktivität von Wasserstoffionen anstelle der Konzentration verwenden. Die pH -Skala hat Zahlen von 0 bis 14. Lösungen mit einem pH -Wert von weniger als 7 sind sauer und wenn der pH -Wert höher als 7 ist, ist es eine grundlegende Lösung. Der pH 7 zeigt eine neutrale Lösung an, ich.e. reines Wasser.

Abbildung 01: pH von verschiedenen Komponenten
Die Gleichung für die Bestimmung des pH -Werts lautet wie folgt:
PH = log10(AH+)
Hier ist „A“ die Aktivität von Wasserstoffionen (H+). Der pH -Wert hängt von der Temperatur der Lösung ab, da die Temperatur die Aktivität einer chemischen Spezies verändern kann. Wenn wir daher den pH -Wert einer wässrigen Lösung geben, sollten wir die Temperatur angeben, bei der der pH genau gemessen wurde. Wir verwenden die pH -Skala, um die Qualität von Wasser, Boden usw. zu bestimmen.
Was ist Puffer?
Ein Puffer ist eine wässrige Lösung, die der Änderung des pH -Werts tendenziell widersetzt. Diese Lösung enthält eine Mischung aus einer schwachen Säure und ihrer konjugierten Base oder umgekehrt. Der pH -Wert dieser Lösungen ändert sich geringfügig bei Zugabe einer starken Säure oder einer starken Base.
Die schwache Säure (oder Base) und ihre konjugierte Base (oder Konjugatsäure) sind im Gleichgewicht miteinander. Wenn wir diesem System eine starke Säure hinzufügen, verschiebt sich das Gleichgewicht in Richtung der Säure und bildet mehr Säure unter Verwendung der von der zugesetzten starken Säure freigesetzten Wasserstoffionen. Obwohl wir bei Zugabe der starken Säure einen Anstieg der Wasserstoffionen erwarten, steigt sie nicht so stark an. Wenn wir eine starke Basis hinzufügen, nimmt die Wasserstoffionenkonzentration in ähnlicher Weise um weniger als die für die Menge an zugegebene Menge erwartete Menge ab. Wir können diesen Widerstand gegen den pH -Wert als Pufferkapazität messen. Die Pufferkapazität misst den Widerstand eines Puffers gegenüber pH -Veränderung bei der Zugabe von OH- Ionen (eine Basis). Wir können es in einer Gleichung wie folgt geben:
β = dn/d (pH)
Wenn β eine Pufferkapazität ist, ist DN eine infinitesimale Menge an zusätzlicher Base, und D (pH) ist die resultierende infinitesimale Änderung des pH -Werts.
Bei der Betrachtung der Anwendungen von Puffern sind diese Lösungen erforderlich, um den richtigen pH -Wert für enzymatische Aktivitäten in Organismen zu behalten. Darüber hinaus werden diese in Branchen in Fermentationsprozessen verwendet, wodurch die korrekten Bedingungen für Farbstoffe festgelegt werden, in der chemischen Analyse, der Kalibrierung von pH -Messgeräten usw. kalibrieren usw.
Was ist der Unterschied zwischen pH und Puffer?
PH ist eine logarithmische Skala, die wir verwenden, um die Säure oder die Basizität einer wässrigen Lösung zu bestimmen, während ein Puffer eine wässrige Lösung ist, die der Änderung des pH -Werts tendenziell widersetzt. Dies ist der Hauptunterschied zwischen pH und Puffer. Darüber hinaus ist der pH -Wert eine sehr wichtige Skala in der Chemie. Wir können den pH -Wert einer Lösung mit einem pH -Messgerät oder über experimentelle Methoden messen. Darüber hinaus verwenden wir die pH -Skala, um die Qualität von Wasser, Boden usw. zu bestimmen. Andererseits besteht die Verwendung von Pufferlösungen darin, den richtigen pH -Wert für die enzymatische Aktivität, in Fermentationsprozessen in der Industrie, bei der Festlegung der korrekten Bedingungen für Farbstoffe, in der chemischen Analyse, in der kalibrierten pH -Messgeräte usw. beizubehalten. Wir messen die Pufferkapazität eines Puffer mithilfe einer chemischen Analyse.

Zusammenfassung -PH vs Puffer
PH ist eine grundlegende Skala, die wir in der Chemie verwenden, um die Säure -R -Basizität einer Lösung zu messen. Puffer sind chemische Lösungen, die den Änderungen des pH -Werts widerstehen können. Daher besteht der Unterschied zwischen pH und Puffer darin, dass der pH -Wert eine logarithmische Skala ist, während ein Puffer eine wässrige Lösung ist.
Referenz:
1. „Ph.”Wikipedia, Wikimedia Foundation, 3. August. 2018. Hier verfügbar
2. "Pufferlösung.Wikipedia, Wikimedia Foundation, 27. Juli 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”PH -Skala” von Edward Stevens - eigene Arbeit (CC von 3.0) über Commons Wikimedia


