Unterschied zwischen polyatomischen Ionen und Verbindungen
Der Schlüsselunterschied zwischen polyatomischen Ionen und Verbindungen ist das, dass die Polyatomische Ionen haben entweder eine positive oder negative elektrische Ladung, während die Verbindungen keine elektrische Nettoladung haben.
Ein polyatomisches Ion ist ein Begriff, den wir verwenden, um chemische Spezies zu benennen, die zwei oder mehr Atome enthalten, die eine negative oder positive elektrische Netto -Ladung haben. Die elektrische Ladung dieses Ions ist ein Ergebnis der Anzahl der in jedem Atom vorhandenen Elektronen. Wenn es mehr Elektronen als die Gesamtzahl der Protonen in Atomen gibt, erhält es eine negative Nettoladung und umgekehrt. Verbindungen hingegen sind chemische Spezies ohne elektrische Ladung. Sie haben die gleiche Anzahl von Elektronen und Protonen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind polyatomische Ionen
3. Was sind Verbindungen
4. Seite an Seitenvergleich - Polyatomische Ionen gegen Verbindungen in tabellarischer Form
5. Zusammenfassung
Was sind polyatomische Ionen?
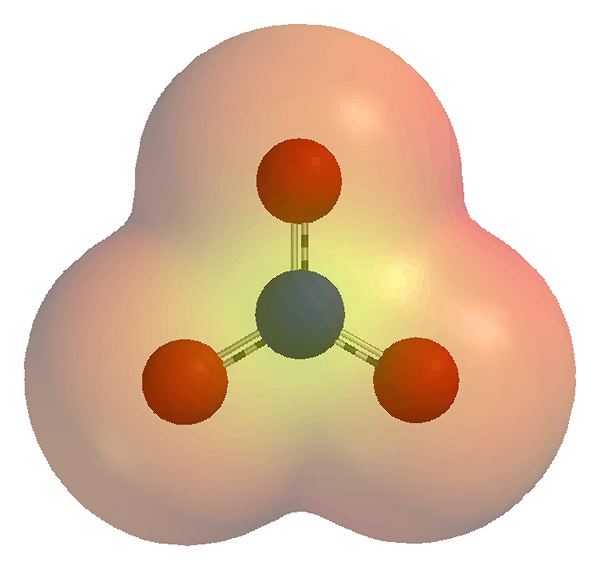
Polyatomische Ionen sind chemische Spezies mit zwei oder mehr Atomen und einer elektrischen Nettoladung. Diese elektrische Ladung kann entweder eine positive Ladung oder eine negative Ladung sein, abhängig von der Anzahl der Elektronen und Protonen, die in der chemischen Spezies vorhanden sind. Ein Synonym für diese Spezies ist „Molekularion“. Die Atome binden kovalent miteinander. Wir können einige Metallkomplexe als polyatomische Ionen betrachten, wenn sie als einzelne Einheit wirken. Im Gegensatz dazu sind monoatomische Ionen einzelne Atome, die eine elektrische Ladung tragen. Wir können diese Ionen in Salzverbindungen, Koordinationsverbindungen und vielen anderen ionischen Verbindungen finden; als Teil der Verbindung.

Abbildung 01: ein Nitration
Einige Beispiele für polyatomische Ionen:
- Acetation (CH3GURREN-)
- Benzoation (C6H5GURREN-)
- Carbonation (CO32-)
- Cyanidion (CN-)
- Hydroxid -Ion (OH-)
- Nitrition (nein2-)
- Ammoniumion (NH4+)
Was sind Verbindungen?
Verbindungen sind chemische Spezies, die identische Moleküle enthalten, aus Atomen von zwei oder mehr chemischen Elementen. Daher tragen diese chemischen Spezies keine elektrische Nettoladung. Daher sind sie neutrale Arten. Die Atome binden entweder kovalente Bindungen, Koordinationsbindungen oder ionischen Bindungen miteinander. Wenn es ein Molekül gibt, das zwei oder mehr Atome desselben Elements enthält, das miteinander verbunden ist, ist es keine Verbindung, da es keine unterschiedlichen Elemente gibt.
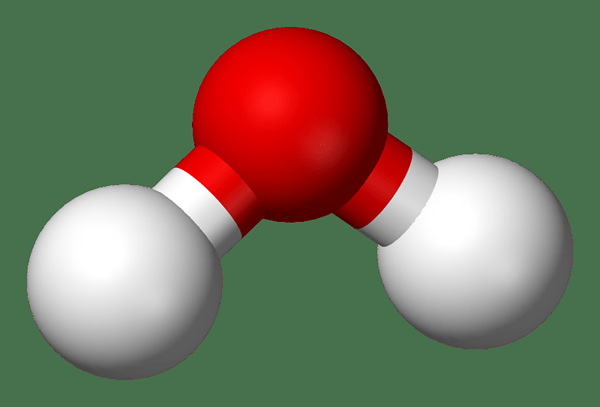
Abbildung 02: ein Wassermolekül
Darüber hinaus gibt es nach der Definition 4 Arten von Verbindungen wie folgt:
- Moleküle mit Kombinationen verschiedener chemischer Elemente
- Ionenverbindungen bestehen aus ionischen Bindungen
- Intermetallische Verbindungen mit metallischen Bindungen
- Koordinationskomplexe bestehen aus Koordinatenbindungen
Wir können eine chemische Formel verwenden, um die chemischen Elemente und das Verhältnis zwischen ihnen in einer Verbindung zu exprimieren. Zum Beispiel ist die chemische Formel des Wassermoleküls H2Ö. Es hat zwei Wasserstoffatome und ein Sauerstoffatom, das Molekül hat jedoch keine elektrische Nettoladung; Somit ist es eine chemische Verbindung.
Was ist der Unterschied zwischen Polyatomionen und Verbindungen?
Polyatomische Ionen sind chemische Spezies mit zwei oder mehr Atomen und einer elektrischen Nettoladung. Sie haben entweder eine positive oder negative elektrische Ladung. Verbindungen sind chemische Spezies, die identische Moleküle enthalten, aus Atomen von zwei oder mehr chemischen Elementen. Sie haben keine elektrische Netto -Ladung. Dies ist der Schlüsselunterschied zwischen Polyatomionen und Verbindungen. Darüber hinaus haben Polyatomionen entweder kovalente Bindungen oder Koordinationsbindungen zwischen den Atomen. Verbindungen können kovalente Bindungen, ionische Bindungen, metallische Bindungen oder Koordinationsbindungen zwischen Atomen aufweisen.
Die folgende Infografik zeigt den Unterschied zwischen Polyatomionen und Verbindungen in tabellarischer Form.

Zusammenfassung -Polyatomische Ionen gegen Verbindungen
Der Schlüsselunterschied zwischen polyatomaren Ionen und Verbindungen besteht darin, dass Polyatomionen entweder eine positive oder negative elektrische Ladung aufweisen, während Verbindungen keine elektrische Netto -Ladung aufweisen. Dies liegt hauptsächlich daran.
Referenz:
1. Helmenstine, Anne Marie, ph.D. „Polyatomische Ionendefinition und Beispiele.”Thoughtco, Jun. 22, 2018. Hier verfügbar
2. Noller, Carl r., et al. "Chemische Verbindung.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 6. Dezember. 2016. Hier verfügbar
Bild mit freundlicher Genehmigung:
1."Nitrat-Ion-Elpot" von Benjah-BMM27-eigener Arbeit, (Public Domain) über Commons Wikimedia
2."Water-3D-Balls" von Benjah-BMM27-eigene Arbeit (Public Domain) über Commons Wikimedia


