Unterschied zwischen Form und Geometrie eines Moleküls
Der Schlüsselunterschied Zwischen Form und Geometrie eines Moleküls ist das Form eines Moleküls ist die Struktur des Moleküls, ausgenommen das einsame Paar am zentralen Atom, während die Geometrie eines Molekül.
Wir verwenden normalerweise die Begriffe - Form und Geometrie eines Moleküls - austauschbar. Dies sind jedoch zwei verschiedene Begriffe für einige Moleküle, die wir kennen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was hat eine Form eines Moleküls
3. Was ist Geometrie eines Moleküls
4. Seite an Seitenvergleich - Form gegen Geometrie eines Moleküls in tabellarischer Form
5. Zusammenfassung
Was hat eine Form eines Moleküls?
Die Form eines Moleküls ist die Struktur des Molekül. Mit anderen Worten, die Form eines Moleküls wird unter Ausnahme der einsamen Elektronenpaare des zentralen Atoms bestimmt. Die Form des Moleküls kann unter Verwendung des VSEPR -Modells (Valenz -Shell -Elektronenpaar -Abstoßungsmodell) vorhergesagt werden.
VSEPR -Modell ist die Theorie, die die Form und Geometrie eines Moleküls bestimmt. Wir können dieses VSPR -Modell verwenden, um eine räumliche Anordnung für Moleküle mit kovalenten Bindungen oder Koordinationsbindungen vorzuschlagen. Die Grundlage dieser Theorie sind die Abstoßungen zwischen Elektronenpaaren in der Valenzhülle von Atomen. Hier finden wir Elektronenpaare in zwei Typen als Bindungspaare und einsame Paare. Zwischen diesen Elektronenpaaren gibt es drei Arten von Abstoßung. Bindungspaar- Einzelpaarabstoßung, Bindungspaar-Bond-Paarabstoßung und einsame Paarpaarabstoßung. Beispielsweise wird die Form des Berylliumchloridmoleküls wie folgt vorhergesagt:
Das zentrale Atom ist sein.
Es hat 2 Valenzelektronen.
Cl Atom kann ein Elektron pro Atom teilen.
Daher ist die Gesamtzahl der Elektronen um das zentrale Atom = 2 (von BE) + 1 × 2 (aus Cl -Atomen) = 4
Daher ist die Anzahl der Elektronenpaare um das Atom = 4/2 = 2
Anzahl der einzelnen Bindungen vorhanden = 2
Anzahl der einsamen Paare vorhanden = 2 - 2 = 0
Daher ist die Geometrie des Becl2 -Moleküls linear.
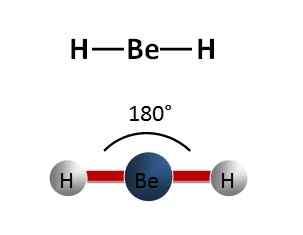
Abbildung 01: Beh2 -Molekül, das der Form des Berylliumchloridmoleküls ähnlich ist
Was ist Geometrie eines Moleküls?
Die Geometrie eines Moleküls ist die Struktur des Moleküls, einschließlich einsamer Elektronenpaare und Bindungselektronenpaare des zentralen Atoms. Daher unterscheidet sich dieser Begriff von der Form eines Moleküls, da die Form eines Moleküls nur unter Verwendung des Bindungselektronenpaares bestimmt wird.

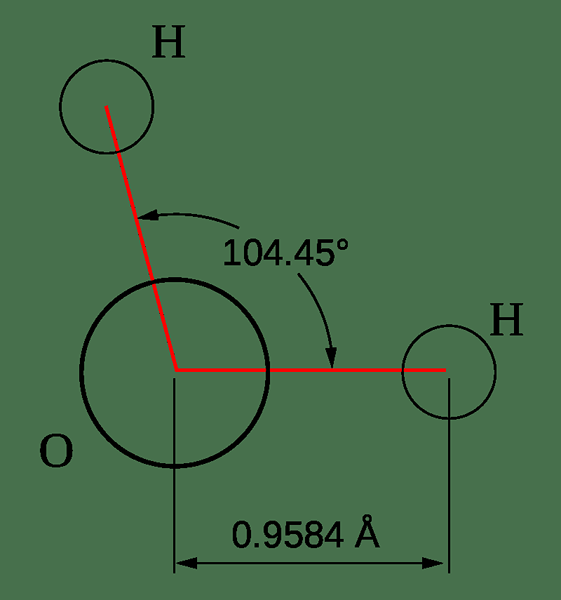
Abbildung 02: Geometrie eines Wassermoleküls
Es gibt verschiedene Methoden zur Bestimmung der Geometrie eines Moleküls, wie verschiedene spektroskopische Methoden, Beugungsmethoden usw.
Was ist der Unterschied zwischen Form und Geometrie eines Moleküls?
Der Schlüsselunterschied zwischen Form und Geometrie eines Moleküls besteht darin des Moleküls. Normalerweise werden die Begriffe Form und Geometrie eines Moleküls synonym verwendet.
Die folgende Infografik fasst die Unterschiede zwischen Form und Geometrie eines Moleküls zusammen.
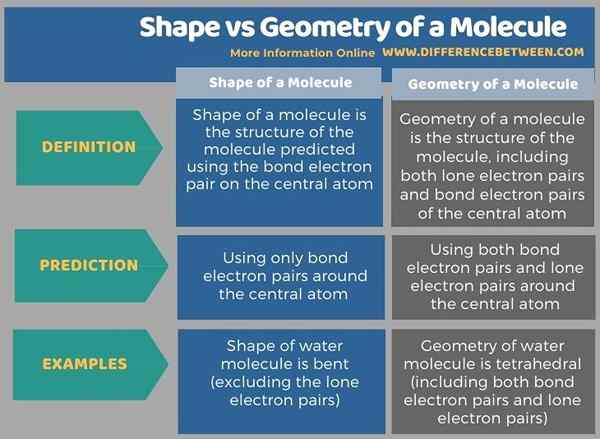
Zusammenfassung -Form gegen Geometrie eines Moleküls
Die Form eines Moleküls ist die Struktur des mit dem Bindelektronenpaares am zentralen Atom vorhergesagten Molekül. Dies ist daher der Schlüsselunterschied zwischen Form und Geometrie eines Moleküls. Normalerweise werden die Begriffe, die Form und die Geometrie eines Moleküls austauschbar verwendet, da beide Strukturen für die meisten Moleküle typischerweise gleich sind, wenn es keine einzelnen Elektronenpaare am zentralen Atom des Moleküls gibt.
Referenz:
1. „Geometrie von Molekülen.”Libretexten, hier verfügbar.
Bild mit freundlicher Genehmigung:
1. "Linear Molecule Ex" von Meeshko - eigene Arbeit (CC BY -SA 4.0) über Commons Wikimedia
2. "Wassermoleküleabmessungen" von Booyabazooka - Bild: Water_Molecule_Dimensions.PNG (CC BY-SA 3.0) über Commons Wikimedia


