Unterschied zwischen Lösung und Kolloid

Der Schlüsselunterschied Zwischen Lösung und Kolloid ist das Die Partikel in einem Kolloid sind oft größer als die gelösten Partikel in einer Lösung.
Eine Mischung ist eine Sammlung verschiedener Substanzen, die sich physisch kombiniert, aber nicht chemisch beitreten. Gemische zeigen unterschiedliche physikalische oder chemische Eigenschaften als die einzelnen Substanzen. Lösungen und Kolloide sind zwei solcher Gemische mit unterschiedlichen Eigenschaften. In diesen Gemischen vermischen sich feste, gasförmige oder flüssige Substanzen in verschiedenen Verhältnissen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Lösung
3. Was ist kolloid
4. Seite für Seitenvergleich - Lösung gegen kolloid in tabellarischer Form
5. Zusammenfassung
Was ist die Lösung?
Eine Lösung ist eine homogene Mischung aus zwei oder mehr Substanzen. Wir nennen es eine homogene Mischung, weil die Zusammensetzung während der gesamten Lösung gleichmäßig ist. Die Komponenten einer Lösung bestehen hauptsächlich aus zwei Arten, Stoffen und dem Lösungsmittel. Das Lösungsmittel löst die gelösten gelösten und bildet eine gleichmäßige Lösung. Normalerweise ist die Lösungsmittelmenge höher als die gelöste Menge.
Alle Partikel in einer Lösung haben die Größe eines Moleküls oder eines Ions, sodass wir sie nicht durch das bloße Auge beobachten können. Die Lösungen können eine Farbe haben, wenn das Lösungsmittel oder die gelösten Stoffe sichtbares Licht absorbieren können. Lösungen sind jedoch in der Regel transparent. Lösungsmittel können in einem flüssigen, gasförmigen oder festen Zustand auftreten. Die häufigsten Lösungsmittel sind Flüssigkeiten. Unter den Flüssigkeiten betrachten wir Wasser als universelles Lösungsmittel, da es viele Substanzen auflösen kann als jedes andere Lösungsmittel. Wir können Gas, feste oder andere flüssige gelöste in flüssigen Lösungsmitteln auflösen. In Gaslösungsmitteln können sich nur Gas gelöscht.

Abbildung 01: verschiedene Lösungen
Trotzdem gibt es eine Grenze für die Anzahl der gelösten Stoffe, die wir zu einer bestimmten Menge an Lösungsmittel hinzufügen können. Die Lösung wird gesättigt, wenn wir dem Lösungsmittel die maximale Menge des gelösten Stoffes hinzufügen. Wenn es eine sehr geringe Menge an gelösten Stoffen gibt, wird die Lösung verdünnt, und wenn in der Lösung eine hohe Menge an gelösten gelösten gelöst ist, wird sie zu einer konzentrierten Lösung. Durch Messung der Konzentration einer Lösung können wir eine Vorstellung von der Menge an gelösten Stoffen in der Lösung bekommen.
Was ist kolloid?
Kolloidale Lösung existiert als homogene Mischung, aber manchmal ist sie heterogen (e.G., Milch, Nebel). Die Partikel in kolloidalen Lösungen haben eine Zwischengröße (größer als Moleküle) im Vergleich zu Partikeln in Lösungen und Suspensionen. Aber wie die Partikel in Lösungen sind sie für das bloße Auge unsichtbar, und wir können nicht mit einem Filterpapier filtern.
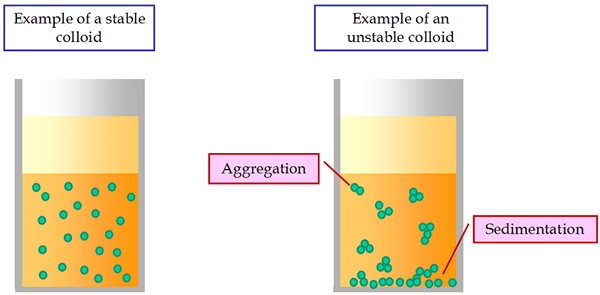
Abbildung 02: Zwei Arten von Kolloiden
Wir nennen die Partikel in einem Kolloid als dispergiertes Material, und das Dispersionsmedium ist analog zum Lösungsmittel in einer Lösung. Gemäß dem verteilten Material und dem Medium gibt es verschiedene Arten von Kolloiden. Wenn beispielsweise ein Gas in einem flüssigen Medium dispergiert, ist das resultierende Kolloid "Schaum" (e.G., Schlagsahne). Wenn sich zwei Flüssigkeiten zusammenschließen, eine Emulsionsform (e).G., Milch). Die Partikel, die sich innerhalb des kolloidalen Mediums verteilen. Kolloidale Lösungen sind durchscheinend oder undurchsichtig. Manchmal können Partikel in einem Kolloid durch Zentrifugation oder Koagulation trennen. Zum Beispiel koagulieren die Proteine in Milch, wenn wir Wärme liefern oder wenn wir eine Säure hinzufügen.
Was ist der Unterschied zwischen Lösung und Kolloid?
Lösungen und Kolloide sind zwei Arten von Gemischen, die zwei oder mehr Substanzen enthalten. Diese Gemische befinden sich im flüssigen Zustand. Der Hauptunterschied zwischen Lösung und Kolloid besteht jedoch darin, dass die Partikel in einem Kolloid häufig größer sind als die gelösten Partikel in einer Lösung. Darüber hinaus sind die Lösungen im Vergleich zu Kolloiden völlig homogen, die auch als heterogenes Gemisch existieren können. Daher ist dies ein weiterer Unterschied zwischen Lösung und Kolloid. Darüber hinaus ist ein weiterer Unterschied zwischen Lösung und Kolloid, dass das Kolloidal entweder undurchsichtig oder durchscheinend ist, Lösungen jedoch transparent sind.

Zusammenfassung - Lösung gegen Kolloid
Sowohl Lösungen als auch Kolloide sind Gemische von zwei oder mehr Substanzen. Der Schlüsselunterschied zwischen Lösung und Kolloid besteht darin, dass die Partikel in einem Kolloid oft größer sind als die gelösten Partikel in einer Lösung.
Referenz:
1. "Lösung.”Wikipedia, Wikimedia Foundation, 21. September. 2018. Hier verfügbar
2. Libretexten. „Kolloide.”Chemistry Libretexten, Libretexte, 9. Januar. 2017. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”217074" von PublicDomainPictures (CC0) über Pixabay
2."ColloidalStability" von Sunkart (CC von 3.0) über Commons Wikimedia


