Unterschied zwischen spontanen und nicht spontanen Reaktionen
Der Schlüsselunterschied Zwischen spontanen und nicht spontanen Reaktionen befindet sich die Spontane Reaktionen haben eine negative Gibbs-freie Energie, während die nicht spontanen Reaktionen eine positive Gibbs-freie Energie haben.
Reaktionen können entweder chemische Reaktionen oder biologische Reaktionen sein. Wir können diese Reaktionen in zwei Kategorien als spontane Reaktionen und nicht-spontane Reaktionen unterteilen. Eine spontane Reaktion tritt ohne externen Einfluss auf. Nicht spontane Reaktionen können jedoch ohne einen externen Einfluss Fortschritte machen können. Lassen Sie uns weitere Details zu diesen Reaktionen diskutieren und den Unterschied zwischen spontanen und nicht spontanen Reaktionen tabellieren.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind spontane Reaktionen
3. Was sind nicht spontane Reaktionen
4. Seite für Seitenvergleich - spontane gegen nicht spontane Reaktionen in tabellarischer Form
5. Zusammenfassung
Was sind spontane Reaktionen?
Spontane Reaktionen sind chemische oder biologische Reaktionen, die ohne den Einfluss eines externen Faktors stattfinden. Darüber hinaus bevorzugen diese Reaktionen, die die Entropie erhöhen und gleichzeitig die Enthalpie eines thermodynamischen Systems verringern. Da diese Reaktionen keinen externen Faktor benötigen, treten sie natürlich auf. Daher bevorzugen diese Reaktionen die Bildung der Produkte unter den Bedingungen, unter denen die Reaktion auftritt. Die freie Energie einer spontanen Reaktion ist ein negativer Wert.
Die meisten spontanen Reaktionen treten schnell auf. Beispiel: Verbrennung von Wasserstoff. Einige Reaktionen treten jedoch extrem langsam auf. Beispiel: Umwandlung von Graphit in Diamanten. Darüber hinaus wird in einigen reversiblen Reaktionen eine Reaktionsrichtung in der anderen Richtung bevorzugt. Beispielsweise wird bei der Bildung von Kohlendioxid und Wasser aus Kohlensäure die Vorwärtsreaktion bevorzugt; Die Bildung von Kohlendioxid und Wasser ist spontan.
H2CO3 ↔ co2 + H2Ö
Was sind nicht spontane Reaktionen?
Nicht spontane Reaktionen sind chemische oder biologische Reaktionen, die nicht ohne den Einfluss eines externen Faktors stattfinden können. Daher werden diese Reaktionen nicht unter den natürlichen Bedingungen unterzogen.

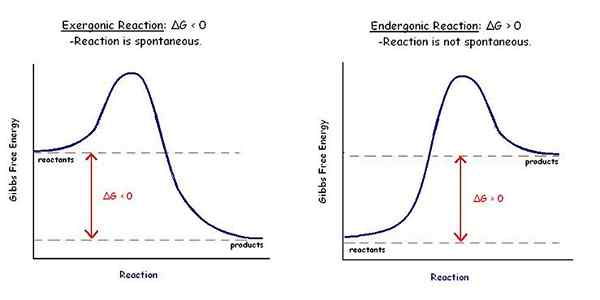
Abbildung 01: Vergleich von spontanen und nicht spontanen Reaktionen
Daher müssen wir einen externen Faktor für diese Reaktionen auf Fortschritte liefern. Beispiel: Wir können Wärme liefern, Druck ausüben, einen Katalysator hinzufügen usw. Darüber hinaus ist die freie Energie von Gibbs für diese Reaktionen positiv.
Fast alle nicht spontanen Reaktionen sind endotherm; Sie geben Energie nach außen frei. Diese Reaktionen begleiten eine Abnahme der Entropie. Bsp. Diese Reaktion tritt jedoch bei sehr hohen Temperaturen auf.
Was ist der Unterschied zwischen spontanen und nicht spontanen Reaktionen?
Spontane Reaktionen sind chemische oder biologische Reaktionen, die ohne den Einfluss eines externen Faktors stattfinden. Sie bevorzugen die Entropie und verringern die Enthalpie eines thermodynamischen Systems. Darüber hinaus ist die freie Energie einer spontanen Reaktion ein negativer Wert. Während die nicht spontanen Reaktionen chemische oder biologische Reaktionen sind, die nicht ohne den Einfluss eines externen Faktors stattfinden können. Sie bevorzugen keine zunehmende Entropie oder abnehmende Enthalpie unter normalen Bedingungen. Darüber hinaus ist die freie Energie einer nicht-spontanen Reaktion ein positiver Wert.

Zusammenfassung -spontane gegen nicht spontane Reaktionen
Alle Reaktionen gehören zu zwei Arten von Reaktionen wie spontanen Reaktionen und nicht spontanen Reaktionen. Der Unterschied zwischen spontanen und nicht spontanen Reaktionen besteht darin, dass spontane Reaktionen eine negative Gibbs-freie Energie aufweisen, während nicht-spontane Reaktionen eine positive Gibbs-freie Energie aufweisen.
Referenz:
1. Libretexten. „11.5: Spontane Reaktionen und freie Energie.”Chemistry Libretexten, Libretexte, 13. Juli 2018. Hier verfügbar
2. Wissenschaft, CK12. „Spontane und nicht spontane Reaktionen.”CK-12 Foundation, CK-12 Foundation, 28. März. 2017. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.'Gibbs Free Energy'by Stephjc - eigene Arbeit, (öffentlich zugänglich) über Commons Wikimedia


