Unterschied zwischen tetraedrischen und oktaedrischen Hohlräumen
Schlüsselunterschied - Tetraedrische gegen oktaedrische Hohlräume
Wenn Sie eng gepackte anorganische Substanzen in Betracht ziehen, gibt es leere Räume, die als Hohlräume bekannt sind. Hohlräume sind nicht besetzt, leere Räume von Einheitszellen in anorganischen Substanzen. Eine Einheitszelle ist eine grundlegende Einheit, die die chemische Anordnung der gesamten Substanz zeigt, die sich aus wiederholten Einheiten zusammensetzt. Die Atome, Moleküle oder Ionen, aus denen das Kristallsystem besteht. In eng gepackten festen Substanzen gibt es zwei Arten von Hohlräumen, die beobachtet werden können. tetraedrische Hohlräume und oktaedrische Hohlräume. Der Schlüsselunterschied Zwischen tetraedrischer und oktaedrischer Leere ist das Tetraedrische Hohlräume sind in Substanzen mit tetraedrischen Kristallsystemen sichtbar, während oktaedrische Hohlräume in Substanzen mit oktaedrischen Kristallsystemen sichtbar sind.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind tetraedrische Hohlräume
3. Was sind oktaedrische Hohlräume
4. Ähnlichkeiten zwischen tetraedrischen und oktaedrischen Hohlräumen
5. Seite an Seitenvergleich - Tetraedrische gegen oktaedrische Hohlräume in tabellarischer Form
6. Zusammenfassung
Was sind tetraedrische Hohlräume?
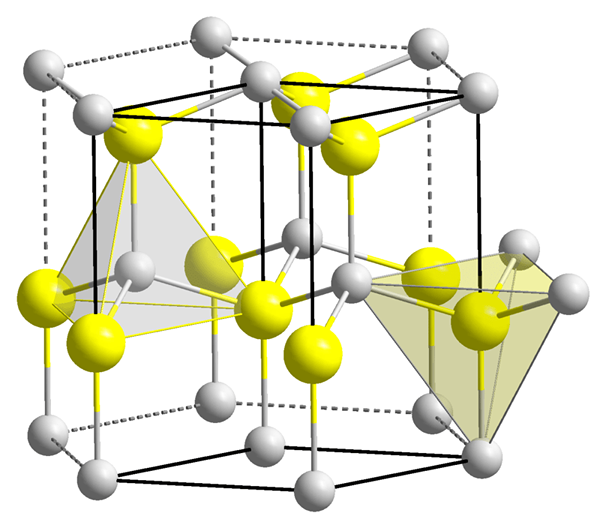
Tetraedrische Hohlräume sind nicht besetzt, leere Räume in Substanzen mit tetraedrischen Kristallsystemen. Daher tritt diese Lücke zwischen vier Bestandteilen auf. Eine tetraedrische Hohlraum. Daher sind zwei Atomschichten an der Bildung einer tetraedrischen Leere beteiligt.
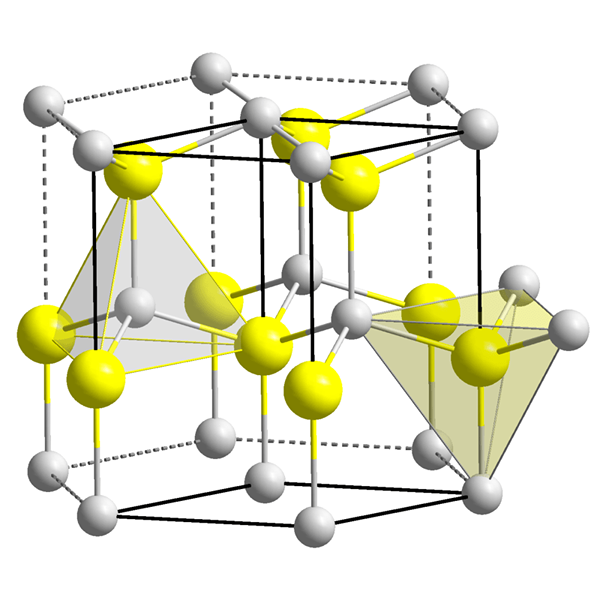
Abbildung 1: Zwei tetraedrische Hohlräume.
Die Form der tetraedrischen Leere ist jedoch nicht tetraedrisch, nur die Anordnung von vier Partikeln um die Hohlraum ist tetraedrisch. Die Formen der Hohlräume sind sehr kompliziert. Das Volumen einer tetraedrischen Leere ist viel kleiner als das eines Atoms (oder eines Kugels), das die Bildung der Hohlräume verursacht. Größer die Größe der Partikel um die Hohlraum, größer die Größe der Hohlräume. Die Koordinationszahl der tetraedrischen Leere beträgt vier. Hier steht die Begriff Koordinationsnummer für die Anzahl der Atome oder Ionen, die sofort die Leere umgeben. Im Kristallsystem gibt es zwei Hohlräume pro Kugel (Atom). Diese Hohlräume und ihre Größen haben einen großen Einfluss auf die materiellen Eigenschaften.
Was sind oktaedrische Hohlräume?
Oktaedrische Hohlräume sind nicht besetzt, leere Räume in Substanzen mit oktaedrischen Kristallsystemen. Zwischen sechs Atomen (oder Kugeln) wird eine oktaedrische Leere gebildet. Dort bilden drei eng gepackte Atome (oder Kugeln) ein gleichseitiges Dreieck und werden über die anderen drei Atome platziert, wodurch sich eine Hohlraum bildet. Hier sind auch zwei Atomschichten an der Bildung der Leere beteiligt.
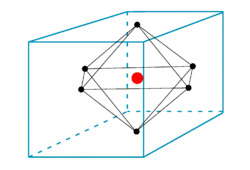
Abbildung 2: Eine oktaedrische Leere in der Mitte der Einheitszelle.
Das Volumen einer oktaedrischen Leere ist im Vergleich zu einer tetraedrischen Leere sehr klein. Wenn eine Einheitszelle einer Substanz (mit einer oktaedrischen Anordnung) berücksichtigt wird, befindet sich in der Mitte der Einheitszelle eine oktaedrische Leere, und die Koordinationszahl dieser Hohlraum beträgt sechs, da sechs Atome sie umgeben. In einem Kristallgitter gibt es eine Hohlraum pro Kugel (oder Atom).
Was sind die Ähnlichkeiten zwischen tetraedrischen und oktaedrischen Hohlräumen?
- Beide sind Hohlräume, die in Kristallgitter vorhanden sind.
- Beide sind kleiner als die Kugeln, die das Kristallgitter aufbauen.
Was ist der Unterschied zwischen tetraedrischen und oktaedrischen Hohlräumen?
Tetraedrische Leere gegen oktaedrische Leere | |
| Tetraedrische Hohlräume sind nicht besetzt, leere Räume in Substanzen mit tetraedrischen Kristallsystemen. | Oktaedrische Hohlräume sind nicht besetzt, leere Räume in Substanzen mit oktaedrischen Kristallsystemen. |
| Kristallsystem | |
| Tetraedrische Hohlräume können in Substanzen mit einer tetraedrischen Anordnung in ihrem Kristallsystem gefunden werden. | Oktaedrische Hohlräume sind in Substanzen mit einer oktaedrischen Anordnung in ihrem Kristallsystem zu finden. |
| Position in der Einheitszelle | |
| Tetraedrische Hohlräume können in Kanten der Einheitszelle beobachtet werden. | Oktaedrische Hohlräume können in der Mitte der Einheitszelle beobachtet werden. |
| Koordinationsnummer | |
| Die Koordinationszahl der tetraedrischen Leere beträgt vier. | Die Koordinationszahl der oktaedrischen Leere beträgt sechs. |
| Anzahl der Hohlräume im Kristallgitter | |
| Es gibt zwei tetraedrische Hohlräume pro Kugel im Kristallgitter. | Es gibt eine oktaedrische Leere pro Kugel im Kristallgitter. |
Zusammenfassung - Tetraedrische gegen oktaedrische Hohlräume
Hohlräume sind leere Räume in Kristallsystemen, die aufgrund der unterschiedlichen Anordnungen von Atomen entstehen. Es gibt zwei Haupttypen von Hohlräumen, die als tetraedrische Leere und oktaedrische Leere bezeichnet werden. Der Unterschied zwischen tetraedrischen und oktaedrischen Hohlräumen besteht darin, dass tetraedrische Leere in Substanzen mit tetraedrischen Kristallsystemen sichtbar ist, während die oktaedrische Leere in Substanzen mit oktaedrischen Kristallsystemen sichtbar ist.
Laden Sie die PDF -Tetraedrisch gegen oktaedrische Hohlräume herunter
Sie können die PDF -Version dieses Artikels herunterladen und ihn für Offline -Zwecke gemäß Citation Note verwenden. Bitte laden Sie die PDF -Version hier den Unterschied zwischen tetraedrischen und oktaedrischen Hohlräumen herunter
Referenz:
1.Maramandansubu folgen. „Hohlräume in Kristallen.”LinkedIn Slideshare, 16. Juni 2013. Hier verfügbar
2.„Tetraedrische Leere und oktaedrische Leere.”StudyLayer.com, 12. März. 2016. Hier verfügbar
Bild mit freundlicher Genehmigung;
1.'Wurtzit Polyedera'by Solid State - eigene Arbeit, (Public Domain) über Commons Wikimedia
2.'Oktaedrisches Kristallfeld' von P. P.WORMER - eigene Arbeit, (CC BY -SA 3.0) über Commons Wikimedia


