Was ist der Unterschied zwischen Guanidin Thiocyanat und Guanidinhydrochlorid
Der Schlüsselunterschied Zwischen Guanidin -Thiocyanat und Guanidinhydrochlorid ist, dass Guanidin -Thiocyanat ein stärkeres Protein -Denaturanten ist, das häufiger bei der RNA -Isolierung verwendet wird, während Guanidinhydrochlorid ein schwächeres Protein -Denaturanten ist, das bei der RNA -Isolierung weniger häufig verwendet wird.
Denaturierung ist der Prozess, bei dem Proteine ihre quartäre Struktur, Tertiärstruktur und Sekundärstruktur verlieren, die normalerweise in ihrem nativen Zustand vorhanden ist. Dies kann durch die Anwendung einiger externer Stress oder Verbindungen wie starker Säure oder Base, konzentriertes anorganisches Salz, organischer Lösungsmittel (Alkohol, Chloroform), Agitation, Strahlung oder Wärme erfolgen. Guanidin -Thiocyanat und Guanidinhydrochlorid sind zwei verschiedene Arten von Protein -Denaturanten.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Guanidin -Thiocyanat
3. Was ist Guanidinhydrochlorid
4. Ähnlichkeiten - Guanidin -Thiocyanat und Guanidinhydrochlorid
5. Guanidin -Thiocyanat gegen Guanidinhydrochlorid in tabellischer Form
6. Zusammenfassung - Guanidin -Thiocyanat gegen Guanidinhydrochlorid
Was ist Guanidin -Thiocyanat?
Guanidin Thiocyanat (GTC) ist ein stärkeres Protein -Denaturierungsmittel, das häufiger bei der RNA -Isolierung verwendet wird. Es ist auch als bekannt als Guanidiniumisothiocyanat (Gitc). Als chaotropes Mittel ist es eine chemische Verbindung, die routinemäßig als allgemeines Protein -Denaturanten verwendet wird. Ein chaotropes Mittel ist ein Molekül in einer Wasserlösung, das das Wasserstoffbrückenbindungsnetz zwischen Wassermolekülen stören kann. Dies wirkt sich auf die Stabilität des nativen Zustands anderer Moleküle in der Lösung aus, wie Makromoleküle wie Proteine und Nukleinsäuren durch Schwächung der hydrophoben Wirkung. Chaotrope Mittel wie Guanidin -Thiocyanat verringern die Ordnung in der Struktur des Proteins, die durch Wassermoleküle sowohl in Massen- als auch in Hydratationsschalen um hydrophobe Aminosäuren gebildet werden. Dies kann zu einer Protein -Denaturierung führen.
Guanidin -Thiocyanat kann verwendet werden, um Viren wie Influenza zu deaktivieren, die 1918 Krankheiten wie die spanische Grippe verursachen. Daher kann es in medizinischen oder Krankenhausaufbauten verwendet werden. Darüber hinaus wird auch Guanidin -Thiocyanat verwendet, um Zellen und Viruspartikel in RNA- und DNA -Extraktionen zu lyse. Hier besteht die Funktion von Guanidin -Thiocyanat darin, die Lysing -Wirkung zu unterstützen und die Aktivität von RNase -Enzymen und DNase -Enzymen durch Denaturierungen zu verhindern. Diese Enzyme würden sonst den Extrakt (RNA oder DNA) schädigen.
Was ist Guanidinhydrochlorid?
Guanidinhydrochlorid (GDNHCL) ist ein schwächeres Protein -Denaturanten, das bei der RNA -Isolierung weniger häufig verwendet wird. Es ist auch als bekannt als Guanidiniumchlorid (GDMCL). Es ist das Hydrochloridsalz von Guanidin. Guanidinhydrochlorid ist chaotrop und einer der Denaturanten, die in den physikalisch -chemischen Untersuchungen zur Proteinfaltung verwendet werden.

Abbildung 01: Guanidinhydrochlorid
Guanidinhydrochlorid kann auch die Enzymaktivität verringern und die Löslichkeit von hydrophoben Molekülen erhöhen. Normalerweise verlieren Proteine bei höheren Konzentrationen von Guanidinhydrochlorid ihre geordnete Struktur. Proteine werden bei dieser Konzentration von Guanidinhydrochlorid in der Regel zufällig gewunden. Bei medizinischen oder Krankenhausaufbauten ist Guanidinhydrochlorid für die Verringerung der Symptome der Muskelschwäche und der einfachen Müdigkeit im Zusammenhang mit dem Eaton-Lambert-Syndrom angezeigt. Darüber hinaus können Nebenwirkungen der Verwendung von Guanidinhydrochlorid Peristaltik, Durchfall und tödliche Knochenmarksuppression umfassen.
Was sind die Ähnlichkeiten zwischen Guanidinthiocyanat und Guanidinhydrochlorid?
- Guanidin -Thiocyanat und Guanidinhydrochlorid sind zwei verschiedene Arten von Protein -Denaturanten.
- Beide Denaturanten haben Guanidin in ihren Strukturen.
- Sie sind chaotrope Agenten.
- Beide Denaturanten können zur RNA -Isolierung verwendet werden.
- Sie werden beide in medizinischen oder Krankenhausaufbauten verwendet.
Was ist der Unterschied zwischen Guanidin Thiocyanat und Guanidinhydrochlorid?
Guanidin -Thiocyanat ist ein stärkeres denaturantes Wirkstoff, das häufiger bei der RNA -Isolierung verwendet wird, während Guanidinhydrochlorid ein schwächeres Protein -Denaturanten ist, das bei der RNA -Isolierung weniger häufig verwendet wird. Dies ist daher der Hauptunterschied zwischen Guanidin -Thiocyanat und Guanidinhydrochlorid. Darüber hinaus ist die chemische Formel von Guanidinthiocyanat c2H6N4S, während die chemische Formel von Guanidinhydrochlorid CH ist5N3.HCl.
Die folgende Infografik stellt die Unterschiede zwischen Guanidin -Thiocyanat und Guanidinhydrochlorid in tabellarischer Form für Seite und Seitenvergleich dar.
Zusammenfassung -Guanidin -Thiocyanat gegen Guanidinhydrochlorid
Guanidin -Thiocyanat und Guanidinhydrochlorid sind zwei verschiedene Arten von Protein -Denaturanten. Beide Denaturanten sind Chaotrope. Guanidin -Thiocyanat ist ein stärkeres denaturantes Wirkstoff, das häufiger bei der RNA -Isolierung verwendet wird, während Guanidinhydrochlorid ein schwächeres Protein -Denaturanten ist, das bei der RNA -Isolierung weniger häufig verwendet wird. Dies fasst also den Unterschied zwischen Guanidin -Thiocyanat und Guanidinhydrochlorid zusammen.
Referenz:
1. „Guanidinium Thiocyanat.”Ein Überblick | Sciencedirect -Themen.
2 “Guanidinhydrochlorid.Nationales Zentrum für Biotechnologieinformationen. Pubchem Compound -Datenbank, u.S. Nationalbibliothek für Medizin.
Bild mit freundlicher Genehmigung:
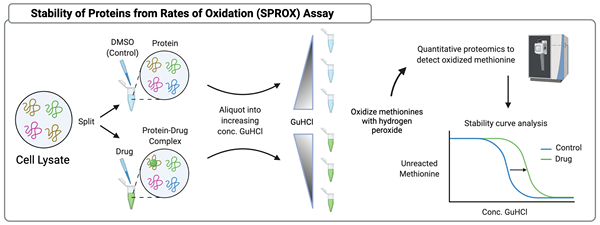
1. "Sprox" von SGOLD626 - eigene Arbeit (CC BY -SA 4.0) über Commons Wikimedia