Unterschied zwischen Affinität und Ionenaustauschchromatographie

Der Schlüsselunterschied Zwischen Affinität und Ionenaustauschchromatographie ist das Wir können die Affinitätschromatographie verwenden, um geladene oder ungeladene Komponenten in einer Mischung zu trennen, während wir Ionenaustauschchromatographie verwenden können, um geladene Komponenten in einer Mischung zu trennen.
Chromatographie ist eine Technik, mit der wir die gewünschten Komponenten in einer Mischung trennen können. Es gibt verschiedene Typen wie Flüssigchromatographie, Gaschromatographie usw. Die Affinitätschromatographie und die Ionenaustauschchromatographie sind zwei Unterkategorien der Flüssigchromatographie. Auch bei diesen Techniken gibt es zwei Phasen. Sie sind nämlich die stationäre Phase und die mobile Phase. Der Zweck dieser Techniken besteht darin, die Komponenten abhängig von der Bindung der Komponenten in der mobilen Phase an der Oberfläche der stationären Phase zu trennen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Affinitätschromatographie
3. Was ist Ionenaustauschchromatographie
4. Seite an Seitenvergleich - Affinität gegen Ionenaustauschchromatographie in tabellarischer Form
5. Zusammenfassung
Was ist Affinitätschromatographie?
Die Affinitätschromatographie ist eine biochemische Technik, mit der wir in Abhängigkeit von den Wechselwirkungen zwischen diesen Komponenten Komponenten in einer Mischung trennen können.
Zu den Interaktionen, die wir in diesem Fall verwenden, gehören die Follower:
- Antigen-Antikörper-Wechselwirkungen
- Enzym-Substrat-Wechselwirkungen
- Rezeptor-Ligand-Wechselwirkungen
- Protein-Nukleinsäure-Wechselwirkungen
In dieser Technik verwenden wir die molekularen Eigenschaften von Molekülen für diese Trennungstechnik. Hier lassen wir die gewünschte Verbindung über Wasserstoffbrücken, Ionenwechselwirkung, Disulfidbrücken, hydrophobe Wechselwirkung usw. mit einer stationären Phase interagieren. Die Moleküle, die nicht mit der stationären Phase interagieren. Somit können wir es von der Mischung trennen. Die gewünschte Verbindung bleibt an der stationären Phase gebunden. Daher können wir es mit einem eluierten Lösungsmittel abnehmen und es eluieren lassen, um es auch zu trennen.

Abbildung 01: Eine chromatographische Säule
Die Affinitätschromatographie ist nützlich bei der Reinigung und Konzentration einer Substanz aus einer Mischung unter Verwendung einer Pufferlösung. Außerdem ist es hilfreich, die unerwünschten Substanzen in einer Mischung zu reduzieren. Bei der Betrachtung des Apparats, den wir für diesen Prozess verwenden, sollten wir eine Spalte mit unserer stationären Phase verwenden. Dann sollten wir die mobile Phase laden, die die Biomoleküle enthält, die wir trennen werden. Lassen Sie sie als nächstes mit der stationären Phase binden. Danach können wir mit einem Waschpuffer die nicht zielgerichteten Biomoleküle trennen, aber die Zielmoleküle sollten eine hohe Affinität für die stationäre Phase haben, um den Trennprozess zu erfüllen.
Was ist Ionenaustauschchromatographie?
Die Ionenchromatographie ist eine Form der Flüssigchromatographie, in der wir Ionensubstanzen analysieren können. Oft verwenden wir es, um anorganische Anionen und Kationen zu analysieren (i.e. Chlorid- und Nitratanionen und Kalium, Natriumkationen). Obwohl es seltener ist, können wir auch organische Ionen analysieren. Darüber hinaus können wir diese Technik zur Reinigung von Proteinen anwenden, da Proteine geladene Moleküle bei bestimmten pH -Werten sind. Hier verwenden wir eine feste stationäre Phase, an die sich die geladenen Partikel befinden können. Zum Beispiel können wir die Harzpolystyrol-Divinylbenzol-Copolymere als feste Unterstützung verwenden.
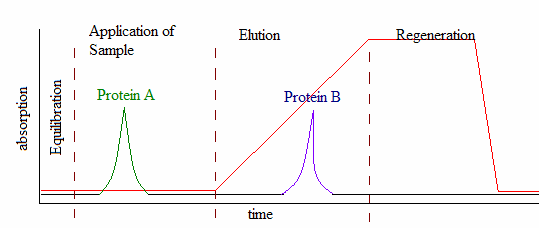
Abbildung 02: Phasen der Ionenaustauschchromatographie
Um dies weiter zu erklären, hat die stationäre Phase feste Ionen wie Sulfatanionen oder quaternäre Aminkationen. Jedes davon sollte mit einer Gegenion (einem Ion mit entgegengesetzter Ladung) assoziieren, wenn wir die Neutralität dieses Systems aufrechterhalten wollen. Wenn die Gegenion ein Kation ist, nennen wir das System als Kationenaustauschharz. Aber wenn die Gegenion ein Anion ist, ist das System ein Anionenaustauschharz.
Es gibt fünf Hauptphasen in einem Ionenaustauschprozess;
- Erstphase
- Adsorption des Ziels
- EINSTELLUNG DER ELIENT
- Ende der Elution
- Regeneration
Was ist der Unterschied zwischen Affinität und Ionenaustauschchromatographie?
Affinitätschromatographie ist eine biochemische Technik, mit der wir in Abhängigkeit von den Wechselwirkungen zwischen diesen Komponenten Komponenten in einer Mischung trennen, während die Ionenchromatographie eine Form der Flüssigchromatographie ist, in der wir Ionensubstanzen analysieren können. Daher besteht der Hauptunterschied zwischen Affinitäts- und Ionenaustauschchromatographie darin, dass wir Ionenaustauschchromatographie nur zur Trennung von ionischen Substanzen verwenden können, während die Affinitätschromatographie sowohl geladene als auch ungeladene Partikel abtrennen kann. Bei der Betrachtung des Arbeitsprinzips besteht der Unterschied zwischen Affinität und Ionenaustauschchromatographie darin, dass die Affinitätschromatographie aufgrund der Tatsache verläuft, dass Zielmoleküle eine hohe Affinität für die stationäre Phase haben. Für die Ionenaustauschchromatographie haben Zielmoleküle jedoch eine entgegengesetzte Ladung für die stationäre Phasenoberfläche.
Die folgende Infografik zeigt den Unterschied zwischen Affinitäts- und Ionenaustauschchromatographie als Vergleich nebeneinander.
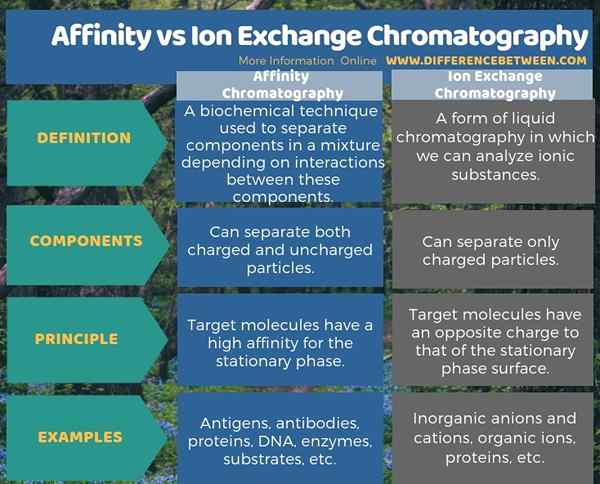
Zusammenfassung -Affinität gegen Ionenaustauschchromatographie
Zusammenfassend sind Affinitäts- und Ionenaustauschchromatographie zwei Formen von flüssigen Chromatographischen Techniken. Der Hauptunterschied zwischen Affinitäts- und Ionenaustauschchromatographie besteht darin, dass wir Affinitätschromatographie verwenden können, um geladene oder ungeladene Komponenten in einer Mischung zu trennen, während wir Ionenaustauschchromatographie verwenden können, um geladene Komponenten in einer Mischung zu trennen.
Referenz:
1. „Affinitätschromatographie.Wikipedia, Wikimedia Foundation, 5. Oktober. 2018. Hier verfügbar
2. Libretexten. „Ionenaustauschchromatographie.”Chemistry Libretextexte, Libretexten, 29. Dezember. 2016. Hier verfügbar
Bild mit freundlicher Genehmigung:
1."Nickelharz" von PDCOOK - eigene Arbeit (CC BY -SA 3).0) über Commons Wikimedia
2."Iex" von Daliak (Public Domain) über Commons Wikimedia


