Unterschied zwischen Ammoniumsulfat und Natriumsulfat
Der Schlüsselunterschied Zwischen Ammoniumsulfat und Natriumsulfat ist das Ammoniumsulfat hat einen scharfen, reizenden Geruch, während Natriumsulfat eine geruchlose Substanz ist.
Ammoniumsulfat und Natriumsulfat enthalten Sulfatanionen, die an verschiedene Kationen gebunden sind: Ammoniumkation und Natriumkation. Daher haben diese Substanzen auch unterschiedliche chemische und physikalische Eigenschaften.
Schlüsselbegriffe
1. Überblick und wichtiger Unterschied
2. Was ist Ammoniumsulfat
3. Was ist Natriumsulfat
4. Seite an Seitenvergleich -Ammoniumsulfat gegen Natriumsulfat in tabellarischer Form
6. Zusammenfassung
Was ist Ammoniumsulfat?
Ammoniumsulfat ist eine anorganische Verbindung mit der chemischen Formel (NH4)2SO4. Diese Substanz enthält ein Ammoniumkation, das mit einem Sulfatanion verbunden ist. Daher hat es zwei Ammoniumkationen pro Sulfatanion. Wir können diese Substanz als anorganisches Sulfatsalz mit vielen wichtigen Verwendungen nennen.
Die Molmasse von Ammoniumsulfat beträgt 132.14 g/mol. Diese Verbindung erscheint als feines, hygroskopisches Granulat oder Kristalle. Darüber hinaus kann der Schmelzpunkt dieser Verbindung zwischen 235 und 280 ° C reichen; Über diesem Temperaturbereich zersetzt sich die Verbindung. Wir können eine Ammoniumsulfatverbindung produzieren, indem wir Ammoniak mit Schwefelsäure behandeln. Für diese Zubereitung können wir eine Mischung aus Ammoniakgas und Wasserdampf in einem Reaktor verwenden. Außerdem müssen wir diesen Reaktor konzentrierte Schwefelsäure aufnehmen, und dann bildet die Reaktion zwischen diesen Komponenten Ammoniumsulfat.
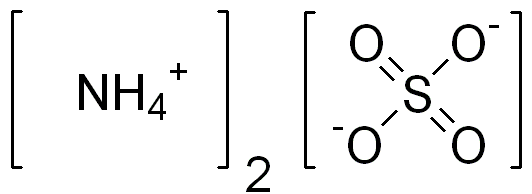
Abbildung 01: Chemische Struktur der Ammoniumsulfat
Bei der Betrachtung der Anwendungen von Ammoniumsulfat können wir es als Dünger hauptsächlich für alkalische Böden verwenden. Darüber hinaus können wir es bei der Herstellung von Insektiziden, Herbiziden, Fungiziden usw. verwenden. Zusätzlich zu diesen verwenden wir diese Verbindung zur Reinigung von Protein durch Niederschlag im Biochemie -Labor. Es ist auch als Lebensmittelzusatz nützlich.
Was ist Natriumsulfat?
Natriumsulfat ist eine anorganische Verbindung mit der chemischen Formel NA2SO4. Diese Verbindung hat mehrere hydratisierte Formen. Unter ihnen ist die häufigste Hydratform die Decahydratform. Alle wasser- und hydratisierten Formen treten als weiße kristalline Feststoff auf. Darüber hinaus ist Natriumsulfat hygroskopisch.

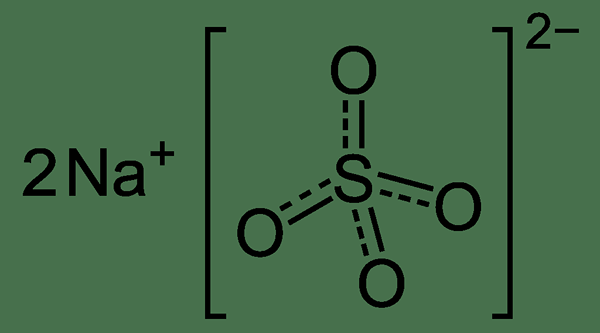
Abbildung 02: Chemische Struktur von Natriumsulfat
Die Molmasse von Natriumsulfat beträgt 142.04 g/mol (wasserfreie Form). Es ist geruchlos und der Schmelzpunkt und die Siedepunkte betragen 884 ° C und 1.429 ° C. Daher kann diese Substanz entweder orthorhombische oder hexagonale Kristallstrukturen haben. Noch wichtiger ist, dass Natriumsulfat sehr stabil ist. Es ist nicht reaktiv gegenüber vielen oxidierenden und reduzierenden Wirkstoffen. Bei hohen Temperaturen kann die Substanz jedoch durch eine Kohlenhilfereduktion in Natriumsulfid umgewandelt werden.
Abgesehen davon ist diese Verbindung ein neutrales Salz. Daher hat die wässrige Lösung dieser Verbindung einen pH -Wert von 7. Zusätzlich zu diesen kann diese Verbindung mit Schwefelsäure reagieren. Bei der Betrachtung der Anwendungen dieser Verbindung ist die Decahydratform nützlich bei der Herstellung von Reinigungsmitteln und vielen anderen Waren. Darüber hinaus ist es im Kraft- und Papierpullen wichtig.
Was ist der Unterschied zwischen Ammoniumsulfat und Natriumsulfat?
Ammoniumsulfat und Natriumsulfat enthalten Kationen und Anionen, die miteinander verbunden sind; Ammoniumkation mit Sulfatanion und Natriumkation mit Sulfatanion gebunden. Wenn wir zwei Proben dieser Verbindungen erhalten, können wir leicht zwischen ihnen unterscheiden, indem wir ihren Geruch spüren. Der Schlüsselunterschied zwischen Ammoniumsulfat und Natriumsulfat besteht darin.
Die folgende Infografik zeigt die Unterschiede zwischen Ammoniumsulfat und Natriumsulfat in tabellarischer Form für Seite für Seitenvergleich.

Zusammenfassung -Ammoniumsulfat gegen Natriumsulfat
Wenn wir zwei Proben von Ammoniumsulfat- und Natriumsulfatverbindungen erhalten, können wir leicht zwischen ihnen unterscheiden, indem wir ihren Geruch spüren. Der Schlüsselunterschied zwischen Ammoniumsulfat und Natriumsulfat besteht darin.
Referenz:
1. "Ammoniumsulfat.” Wikipedia, Wikimedia Foundation, 21. Februar. 2021, hier erhältlich.
Bild mit freundlicher Genehmigung
1. "Natriumsulfat" von Kemikungen - eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Ammoniumsulfat" von Edgar181 - eigene Arbeit (Public Domain) über Commons Wikimedia