Unterschied zwischen Benzol und Cyclohexan
Der Schlüsselunterschied Zwischen Benzol und Cyclohexan ist das die Benzol ist eine aromatische Verbindung, während das Cyclohexan eine nicht-aromatische Verbindung ist.
Der Wissenschaftler Kekule fand die Benzolstruktur 1872. Aufgrund der Aromatizität unterscheidet sich Benzol von anderen aliphatischen Verbindungen. Somit ist es ein separates Studienfeld in der organischen Chemie. Andererseits, obwohl Cyclohexan eine ähnliche Form wie Benzol hat, ist es nicht aromatisch. Cyclohexan ist ein gesättigtes Alkan, das unterschiedliche Eigenschaften hat als Benzol.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Benzol
3. Was ist Cyclohexan
4. Seite an Seitenvergleich - Benzol gegen Cyclohexan in tabellarischer Form
5. Zusammenfassung
Was ist Benzol?
Benzol hat nur Kohlenstoff- und Wasserstoffatome angewendet, um eine planare Struktur zu ergeben. Es hat die molekulare Formel von C6H6. Seine Struktur und einige der wichtigen Eigenschaften sind wie folgt.
- Benzol ist eine farblose Flüssigkeit mit einem süßen Geruch.
- Es ist brennbar und verdunstet schnell, wenn sie freigelegt werden.
- Als Lösungsmittel nützlich, weil es viele nicht Polare Verbindungen auflösen kann.
- Es ist im Wasser leicht löslich.
- Delokalisierung von PI -Elektronen.
Struktur von Benzol
Die Struktur von Benzol ist im Vergleich zu anderen aliphatischen Kohlenwasserstoffen einzigartig. Daher hat Benzol einzigartige Eigenschaften. Alle Kohlenstoffe in Benzol haben drei SP2 Hybridisierte Orbitale. Zwei sp2 Hybridisierte Orbitale von Kohlenstoffüberlappung mit SP2 Hybridisierte Orbitale benachbarte Kohlenstoffe auf beiden Seiten. Andere sp2 Hybridisierte Orbital überlappt sich mit dem S -Orbital von Wasserstoff, um eine σ -Bindung zu bilden.
Auch die Elektronen in P -Orbitalen von Kohlenstofflappen mit den P -Elektronen von Kohlenstoffatomen in beiden Seiten bilden PI -Bindungen. Diese Überlappung der Elektronen erfolgt in allen sechs Kohlenstoffatomen und erzeugt daher ein System von PI -Bindungen, die sich über den gesamten Kohlenstoffring ausbreiten. Wir sagen daher, dass diese Elektronen delokalisiert werden. Die Delokalisierung der Elektronen bedeutet, dass es keine abwechselnden Doppel- und Einzelbindungen wechseln. Daher sind alle C-C-Bindungslängen gleich, und die Länge zwischen Einzel- und Doppelbindungslängen ist. Infolge der Delokalisierung ist Benzolring stabil und zögert daher, im Gegensatz zu anderen Alkenen Additionsreaktionen zu unterziehen.
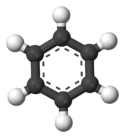
Abbildung 01: Stick- und Ballmodell für Benzol
Die Benzolquellen umfassen Naturprodukte oder verschiedene synthetisierte Chemikalien. Natürlich kommt es in Petrochemikalien wie Rohöl oder Benzin vor. In Bezug auf die synthetischen Produkte ist Benzol in einigen Kunststoffen, Schmierstoffe, Farbstoffen, synthetischen Gummi, Reinigungsmitteln, Medikamenten, Zigarettenrauch und Pestiziden vorhanden. Benzol wird beim Verbrennen von überdurchschnittlichen Materialien freigesetzt. Daher enthalten auch Automobilabgase und Fabrikemissionen Benzol. Vor allem ist es krebserregend, daher kann die Exposition gegenüber hohen Benzolspiegeln Krebs verursachen.
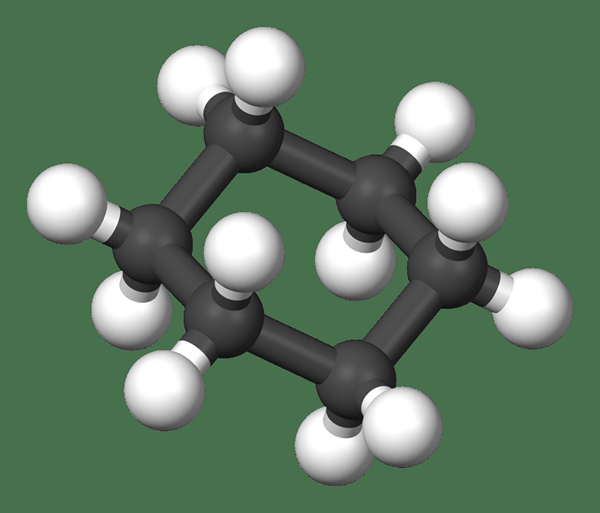
Was ist Cyclohexan?
Cyclohexan ist ein zyklisches Molekül mit der Formel von C6H12. Obwohl es eine ähnliche Anzahl von Kohlenstoffen wie Benzol hat, ist Cyclohexan ein gesättigtes Molekül. Daher gibt es keine Doppelbindungen zwischen Kohlenstoffen wie in Benzol. Außerdem ist es eine farblose Flüssigkeit mit einem milden süßen Geruch.

Abbildung 02: Ball- und Stickmodell für Cyclohexan
Darüber hinaus können wir diese Verbindung über die Reaktion zwischen Benzol und Wasserstoff produzieren. Da dies ein Cycloalkan ist, ist es etwas unreaktiv. Außerdem ist es unpolar und hydrophobisch. Daher ist dies als unpolares Lösungsmittel in den Laboranwendungen nützlich. Darüber hinaus ist Cyclohexan eines der stabilsten Cycloalkan. So erzeugt es im Verbrennen der geringsten Wärme im Vergleich zu anderen Cycloalkanen.
Was ist der Unterschied zwischen Benzol und Cyclohexan?
Benzol ist eine organische Verbindung mit der chemischen Formel C6H6 und eine planare Struktur, während Cyclohexan ein zyklisches Molekül mit der Formel von C ist6H12. Der Schlüsselunterschied zwischen Benzol und Cyclohexan besteht darin, dass Benzol eine aromatische Verbindung ist, während Cyclohexan eine nicht-aromatische Verbindung ist. Es liegt daran, dass es keine Doppelbindungen zwischen Kohlenstoffatomen im Cyclohexanring gibt. Ein weiterer wichtiger Unterschied zwischen Benzol und Cyclohexan besteht darin, dass das Benzol ein ungesättigtes Molekül ist, während Cyclohexan ein gesättigtes Molekül ist. Es liegt daran, dass Benzol mit SP Kohlenstoffatome im Ring hat2 Hybridisierung, während Cyclohexan Kohlenstoffatome im Ring mit SP hat3 Hybridisierung.
Die folgende Infografik des Unterschieds zwischen Benzol und Cyclohexan zeigt mehr Unterschiede zwischen den beiden.

Zusammenfassung -Benzol gegen Cyclohexan
Benzol und Cyclohexan sind beide sechsgliedrige Ringstrukturen. Sie unterscheiden sich jedoch gemäß der chemischen Bindung zwischen Kohlenstoffatomen; Somit die Geometrie der Moleküle. Da die Bindung zwischen Kohlenstoffatomen die Aromatizität von Molekülen bestimmt, können wir betonen, dass der Schlüsselunterschied zwischen Benzol und Cyclohexan als; Benzol ist eine aromatische Verbindung, während Cyclohexan eine nicht-aromatische Verbindung ist.
Referenz:
1. "Benzol.Wikipedia, Wikimedia Foundation, 27. September. 2018. Hier verfügbar
2. „Cyclohexan.”Wikipedia, Wikimedia Foundation, 10. Oktober. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”Benzol-aromatisch-3d-Balls“ von Benjah-BMM27-eigener Arbeit, (Public Domain) über Commons Wikimedia
2.”Cyclohexan-Vorsitzender-3D-Balls” (Public Domain) über Commons Wikimedia


