Unterschied zwischen Kohlenstoff und Diamant
Der Schlüsselunterschied Zwischen Kohlenstoff und Diamant ist das Kohlenstoff ist ein chemisches Element, während Diamond ein Allotrop von Kohlenstoff ist.
Kohlenstoff ist ein chemisches Element mit der Atomzahl 6 und dem chemischen Symbol c. Es kommt in der Natur in verschiedenen Strukturen vor, die wir Allotrope von Kohlenstoff bezeichnen. Diese Strukturen enthalten nur Kohlenstoff als chemisches Element, aber die räumliche Anordnung der Kohlenstoffatome unterscheidet sich voneinander. Diamond ist auch eine Art Allotrope. Die physikalischen Eigenschaften von Allotropen unterscheiden sich auch voneinander.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Kohlenstoff
3. Was ist Diamant
4. Seite an Seitenvergleich - Carbon gegen Diamant in tabellarischer Form
5. Zusammenfassung
Was ist Kohlenstoff?
Kohlenstoff ist ein chemisches Element mit der Atomzahl 6 und dem chemischen Symbol c. Es handelt. Gemäß der Elektronenkonfiguration von Kohlenstoff ([He] 2s2 2p2) Ein Kohlenstoffatom kann vier kovalente chemische Bindungen bilden. Darüber hinaus hat dieses Element Isotope (Atome desselben Elements mit unterschiedlichen Neutronen). Das häufigste und stabilste Isotop von Kohlenstoff ist 12 ° C während 13C ist ein stabiles, aber weniger häufiges Isotop; 14C hingegen ist ein radioaktives Isotop.
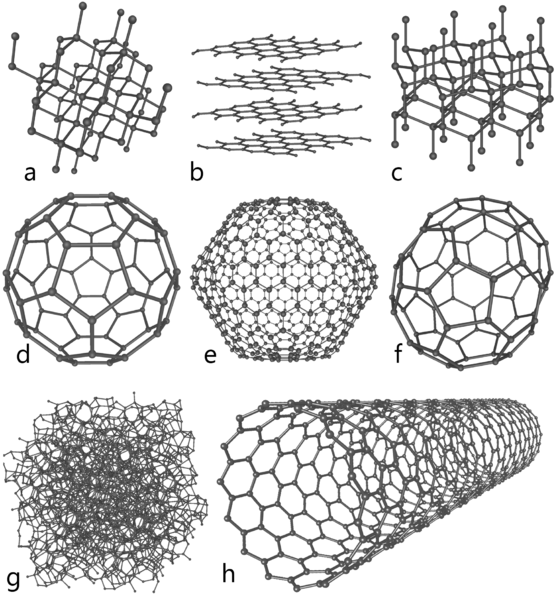
Abbildung 01: Kohlenstoffallotrope
Allotrope von Kohlenstoff sind die verschiedenen strukturellen Formen von Kohlenstoff, die nur Kohlenstoffatome, aber unterschiedliche räumliche Anordnungen haben. Dies sind die natürlich vorkommenden Kohlenstoffformen. Die häufigsten Beispiele sind Diamant und Graphit. Obwohl diese beiden Strukturen nur aus Kohlenstoffatomen bestehen, haben sie aufgrund der Unterschiede in der räumlichen Anordnung unterschiedliche physikalische Eigenschaften. Zum Beispiel ist Diamond transparent, während Graphit undurchsichtig ist. Darüber hinaus werden einige andere chemische Tatsachen über Kohlenstoff wie folgt aufgeführt:
- Die Atomzahl ist 6
- Massenzahl ist 12.011
- Gruppe 14 und Periode 2
- P -Blockelement
- Reaktiver Nichtmetall
- Bei Standardtemperatur und Druck tritt es im Festkörper auf
- Der Sublimationspunkt beträgt 3642 ° C
- Triple Point ist 4600 K, 10.800 kPa
- Der häufigste Oxidationszustand ist +4
Was ist Diamant?
Diamond ist ein Allotrop von Kohlenstoff. Es ist eine feste Form von Kohlenstoff, die eine dreidimensionale Form hat. Darüber hinaus wird jedes Kohlenstoffatom über kovalente chemische Bindung mit vier anderen Kohlenstoffatomen befestigt. Und diese Kristallstruktur wird als „Diamond Cubic“ -Struktur bezeichnet. Darüber hinaus weist diese Verbindung unter allen natürlichen Materialien die höchste Härte und thermische Leitfähigkeit auf. Daher ist Diamond in Branchen zum Schneiden und Polieren von Werkzeugen üblich.

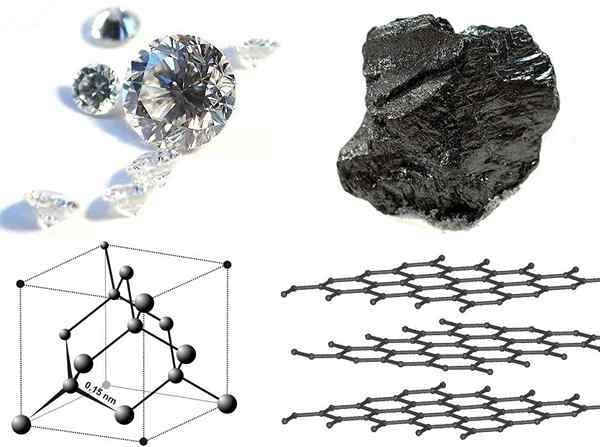
Abbildung 02: Diamond vs Graphit
Einige wichtige Fakten über Diamond sind wie folgt:
- Fällt in die Kategorie der einheimischen Mineralien
- Wiederholungseinheit ist Kohlenstoff
- Formelmasse ist 12.01 g/mol
- Farbe ist typischerweise gelb, braun oder grau bis farblos
- Fraktur ist unregelmäßig/ungleichmäßig
- Darüber hinaus ist sein Mineralstreifen farblos
Was ist der Unterschied zwischen Kohlenstoff und Diamant?
Kohlenstoff ist ein chemisches Element mit Atomzahl 6 und chemischem Symbol C, während Diamond das stärkste Allotrop von Kohlenstoff ist. Der Hauptunterschied zwischen Kohlenstoff und Diamant besteht darin, dass Kohlenstoff ein chemisches Element ist, während Diamant ein Allotrop von Kohlenstoff ist. Darüber hinaus hängt das Erscheinungsbild von Kohlenstoff von der Art des Allotrops ab, e.G Graphit hat eine dunkle Farbe und ist undurchsichtig, während Diamond transparent ist und typischerweise gelb, braun oder grau bis farblos erscheint. Obwohl die meisten Kohlenstoffloschen eine geringere Festigkeit haben, sind Diamond die stärksten Materialien, die auf der Erde natürlich auftreten.
Die folgende Tabelle zeigt den Unterschied zwischen Kohlenstoff und Diamant.

Zusammenfassung -Carbon vs Diamond
Carbon hat viele häufige Allotröme, während die stärkste Struktur unter ihnen Diamant ist. Der Hauptunterschied zwischen Kohlenstoff und Diamant besteht daher darin, dass Kohlenstoff ein chemisches Element ist, während Diamant ein Allotrop von Kohlenstoff ist.
Referenz:
1. "Kohlenstoff.”Wikipedia, Wikimedia Foundation, 26. April. 2019, hier erhältlich.
2. "Diamant.Geologie.com, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Acht Carbon -Allope von Carbon" von Michael Ströck (Mstroeck) - (CC BY -SA 3.0) über Commons Wikimedia
2. "Diamond und Graphite2" von Diamond_and_Graphit.JPG: Benutzer: Itubderivative Arbeit: MaterialScientist (Diskussion) - Diamond_and_Graphit.JPGFILE: Graphit-TN19A.JPG (CC BY-SA 3.0) über Commons Wikimedia


