Unterschied zwischen Enthalpie und Entropie
Der Schlüsselunterschied Zwischen Enthalpie und Entropie befindet sich das Enthalpie ist die Wärmeübertragung in einem konstanten Druck, während die Entropie eine Vorstellung von der Zufälligkeit eines Systems gibt.
Für die Studienzwecke in der Chemie teilen wir das Universum als System und Umgebung in zwei. Der Teil, den wir studieren werden, ist das System jederzeit und der Rest ist umgeben. Enthalpie und Entropie sind zwei Begriffe, die die Reaktionen in einem System und in der Umgebung beschreiben. Sowohl Enthalpie als auch Entropie sind thermodynamische Zustandsfunktionen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Enthalpie
3. Was ist Entropie
4. Seite an Seite Vergleich - Enthalpie gegen Entropie in tabellarischer Form
5. Zusammenfassung
Was ist Enthalpie?
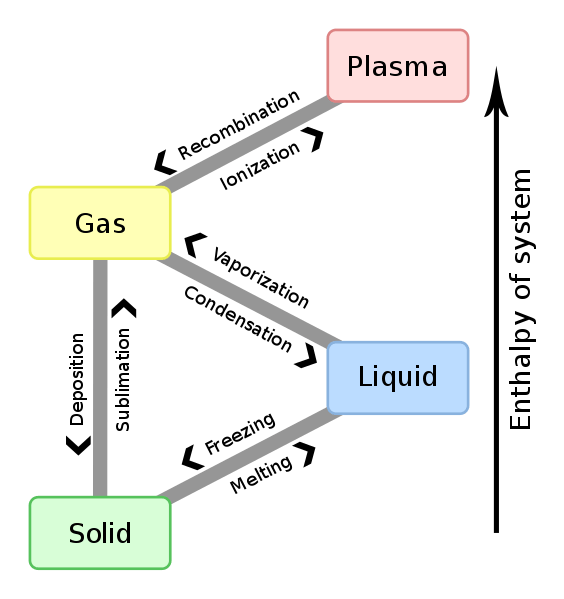
Wenn eine Reaktion stattfindet, kann sie Wärme absorbieren oder weiterentwickeln, und wenn wir die Reaktion bei konstantem Druck durchführen, nennen wir sie die Enthalpie der Reaktion. Wir können jedoch nicht die Enthalpie von Molekülen messen. Daher müssen wir die Änderung der Enthalpie während einer Reaktion messen. Wir können die Enthalpieänderung (∆H) für eine Reaktion in einer bestimmten Temperatur und zum Druck durch Subtrahieren der Enthalpie von Reaktanten von der Enthalpie von Produkten erhalten. Wenn dieser Wert negativ ist, ist die Reaktion exotherm. Wenn der Wert positiv ist, ist die Reaktion endotherm.

Abbildung 01: Beziehung zwischen Enthalpieveränderung und Phasenänderung
Die Änderung der Enthalpie zwischen jedem Paar von Reaktanten und Produkten ist unabhängig vom Weg zwischen ihnen. Darüber hinaus hängt die Enthalpieänderung von der Phase der Reaktanten ab. Zum Beispiel beträgt die Enthalpieänderung, wenn die Sauerstoff- und Wasserstoffgase zur Herstellung von Wasserdampf reagieren, -483.7 kj. Wenn dieselben Reaktanten jedoch auf Flüssigkeitswasser reagieren, beträgt die Enthalpieänderung -571.5 kj.
2H2 (g) +o2 (g) → 2H2O (g); ∆H = -483.7 kj
2H2 (g) +o2 (g) → 2H2O (l); ∆H = -571.7 kj
Was ist Entropie?
Einige Dinge passieren spontan, andere nicht. Zum Beispiel fließt Wärme von einem heißen Körper zu einem kühleren. Wenn eine Änderung auftritt, bleibt die Gesamtenergie konstant, wird jedoch unterschiedlich ausgedehnt. Wir können die Richtung der Änderung durch die Energieverteilung bestimmen. Eine Veränderung ist spontan, wenn sie im Universum als Ganzes zu größerer Zufälligkeit und Chaos führt. Wir können den Grad an Chaos, Zufälligkeit oder Energieverteilung durch eine Zustandsfunktion messen; Wir nennen es als Entropie.
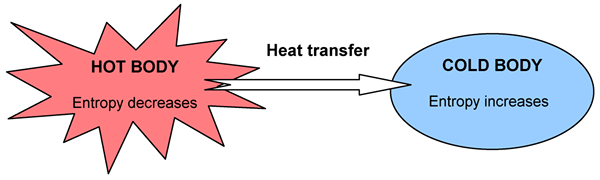
Abbildung 02: Ein Diagramm, das die Änderung der Entropie durch Wärmeübertragung zeigt
Das zweite Gesetz der Thermodynamik hängt mit der Entropie zusammen und sagt: „Die Entropie des Universums nimmt in einem spontanen Prozess zu.Die Entropie und die erzeugte Wärmemenge beziehen sich gegenseitig durch das Ausmaß, in dem das System Energie verwendete. Tatsächlich hängt die Menge der Entropieveränderung oder zusätzliche Störung durch eine bestimmte Wärme -Q -Menge von der Temperatur ab. Wenn es bereits sehr heiß ist, führt ein bisschen zusätzliche Wärme nicht viel mehr Störung, aber wenn die Temperatur sehr niedrig ist, führt die gleiche Wärmemenge zu einer dramatischen Erhöhung der Störung. Daher können wir es wie folgt schreiben: (wobei DS in der Entropie geändert wird, DQ in der Wärme verändert und T ist die Temperatur.
ds = dq/t
Was ist der Unterschied zwischen Enthalpie und Entropie?
Enthalpie und Entropie sind zwei verwandte Begriffe in der Thermodynamik. Der Hauptunterschied zwischen Enthalpie und Entropie besteht darin, dass Enthalpie die Wärmeübertragung in einem konstanten Druck erfolgt, während die Entropie eine Vorstellung von der Zufälligkeit eines Systems ergibt. Darüber hinaus bezieht sich Enthalpy auf das erste Gesetz der Thermodynamik, während die Entropie auf das zweite Gesetz der Thermodynamik bezieht. Ein weiterer wichtiger Unterschied zwischen Enthalpie und Entropie besteht darin, dass wir Enthalpie verwenden können, um die Energieänderung des Systems nach der Reaktion zu messen, während wir Entropie verwenden können, um den Grad der Störung des Systems nach der Reaktion zu messen.
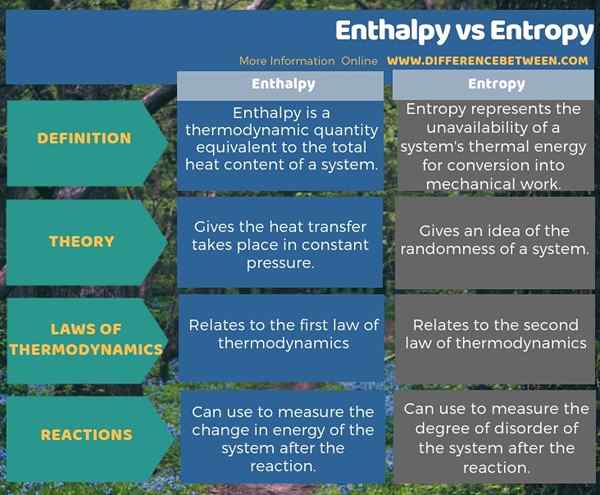
Zusammenfassung -Enthalpie gegen Entropie
Enthalpie und Entropie sind thermodynamische Begriffe, die wir häufig mit chemischen Reaktionen verwenden. Der Hauptunterschied zwischen Enthalpie und Entropie besteht darin, dass Enthalpie die Wärmeübertragung in einem konstanten Druck erfolgt, während die Entropie eine Vorstellung von der Zufälligkeit eines Systems ergibt.
Referenz:
1. Libretexten. „Enthalpie.”Chemistry Libretexten, National Science Foundation, 26. November. 2018. Hier verfügbar
2. Drake, Gordon W.F. "Entropie.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 7. Juni 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1."Phasenwechsel - en" von F L a n k e r, Penubag - eigene Arbeit, (Public Domain) über Commons Wikimedia
2."Entropie heiß zu kalt" von Ibrahim Dincer und Yunus a. Cengel - Entropy 2001, 3 (3), 116-149; doi: 10.3390/e3030116 http: // www.MDPI.com/1099-4300/3/3/116, (cc von 3.0) über Commons Wikimedia


