Unterschied zwischen Ausgleich und Neutralisation
Der Schlüsselunterschied zwischen Ausgleich und Neutralisierung ist das Die Ausgleich bezieht sich auf das Ausgleich der Atome einer chemischen Reaktionsgleichung, während die Neutralisation das Ausgleich der Säure oder Basizität ist, um eine neutrale Lösung zu erhalten.
Obwohl die Begriffe Equalization und Neutralisation ähnlich klingen, unterscheiden sie sich in Bedeutung und Anwendung voneinander. Beide Begriffe beziehen sich jedoch auf den Ausgleichsprozess chemischer Komponenten.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Ausgleich
3. Was ist Neutralisation
4. Seite für Seitenvergleich -Ausgleich gegen Neutralisation in tabellarischer Form
5. Zusammenfassung
Was ist Ausgleich?
Ausgleich ist die Technik, die Atome einer chemischen Reaktionsgleichung auszugleichen. Hier müssen wir die Anzahl der Atome in der Reaktantenseite bis zur Anzahl der Atome in der Produktseite ausgleichen. Dies bedeutet, dass die Atomizität vor und nach der chemischen Reaktion gleich sein muss. Zu diesem Zweck können wir stöchiometrische Koeffizienten vor Reaktanten und Produkten verwenden (ein stöchiometrischer Koeffizient ist eine Zahl, die vor dem Symbol chemischer Spezies in der Gleichung für eine chemische Reaktion erscheint. Diese Werte sind unitlose Werte).
Die folgenden Schritte helfen uns, eine chemische Gleichung für eine einfache chemische Reaktion auszugleichen.
- Schreiben Sie die unausgeglichene Gleichung auf. (E.G. C3H8 + Ö2 ⟶ co2 + H2Ö)
- Bestimmen Sie die Zahlen jedes Atoms sowohl auf der Reaktantenseite als auch auf der Produktseite. (In der Reaktantenseite gibt es 8 Wasserstoffatome, 3 Kohlenstoffatome und 2 Sauerstoffatome. Auf der Produktseite gibt es 2 Wasserstoffatome, 3 Sauerstoffatome und ein Kohlenstoffatom).
- Speichern Sie Wasserstoff und Sauerstoffatome zum Schluss.
- Verwenden Sie stöchiometrische Koeffizienten, um einzelne Elemente auszugleichen. (Verwenden Sie den stöchiometrischen Koeffizienten „3“ vor CO2) e.G. C3H8 + Ö2 ⟶ 3CO2 + H2Ö
- Gleiche die Anzahl der Wasserstoffatome ausgleichen. (Es gibt 8 Wasserstoffatom auf der Reaktantenseite, aber nur 2 auf der Produktseite. Wir sollten also den stöchiometrischen Koeffizienten 4 vor H verwenden2O) e.G. C3H8 + Ö2 ⟶ 3co2 + 4H2Ö
- Gleiche die Anzahl der Sauerstoffatome ausgleichen. E.G. C3H8 + 5Ö2 ⟶ 3co2 + 4H2Ö
Was ist Neutralisation?
Eine Neutralisationsreaktion ist eine chemische Reaktion zwischen einer Säure und einer Base, die eine neutrale Lösung erzeugt. Eine neutrale Lösung hat immer pH 7. Diese Reaktion beinhaltet die Kombination von H+-Ionen und OH-Ionen zur Bildung von Wassermolekülen.
Wenn der endgültige pH-Wert eines Säure- und Basenreaktionsgemisches 7 beträgt, bedeutet dies, dass die gleichen Mengen an H+und OH-Ionen hier reagiert haben (um ein Wassermolekül zu bilden, sind ein H+-Ion und ein OH-Ionen erforderlich). Die reagierten Säuren und Basen können entweder stark oder schwach sein. Die Reaktionen variieren je nach Tatsache.

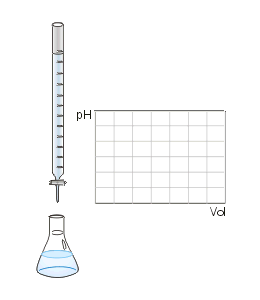
Abbildung 01: Eine stark säurebeständige Base-Neutralisationstitration
Es gibt vier verschiedene Arten von Neutralisationsreaktionen: starke Reaktionen mit säurestarken Basen, starke Reaktionen mit säurweicher Basen, schwache Säurewak-Basenreaktionen und schwache Reaktionen mit Säurewak-Basen. Diese Reaktionen werden je nach Stärke der Säure und der Base in unterschiedlichen Graden neutralisiert.
Was ist der Unterschied zwischen Ausgleich und Neutralisation?
Der Schlüsselunterschied zwischen Ausgleich und Neutralisation besteht darin, dass die Ausgleich sich auf das Gleichgewicht der Atome einer chemischen Reaktionsgleichung bezieht, während die Neutralisation das Ausgleich der Säure oder Basizität ist, um eine neutrale Lösung zu erhalten. Darüber hinaus beinhaltet die Equalization die Verwendung der Anzahl der Atome bei Reaktanten und Produkten und die Verwendung der Oxidationszustände von Atomen, während die Neutralisation die Festigkeit der an der Reaktion beteiligten Säuren und Basen bestimmt.
Die folgende Infografik fasst den Unterschied zwischen Ausgleich und Neutralisation zusammen.
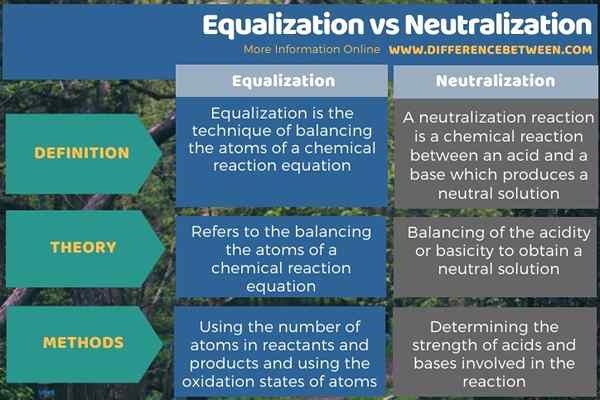
Zusammenfassung -Ausgleich gegen Neutralisation
Obwohl der Begriff Equalization und Neutralisation ähnlich klingen, unterscheiden sie sich in Definition und Anwendung voneinander. Der Schlüsselunterschied zwischen Ausgleich und Neutralisation besteht darin, dass die Ausgleich sich auf die Ausgleich der Atome einer chemischen Reaktionsgleichung bezieht, während die Neutralisation die Säure oder Basizität ausbalanciert, um eine neutrale Lösung zu erhalten.
Bild mit freundlicher Genehmigung:
2. "Titolazion" von Luigi Chiesa - Draw von Luigi Chiesa (Public Domain) über Commons Wikimedia


