Unterschied zwischen Gefrierpunkt -Depression und Siedepunkterhöhung
Schlüsselunterschied - Einfrieren Punktdepression gegen Kochpunkterhöhung
Die Gefrierpunkt -Depression führt zu einer Lösung, um bei einer niedrigeren Temperatur zu frieren als der Gefrierpunkt des reinen Lösungsmittels aufgrund der Zugabe von gelösten Stoffen. Die Erhöhung des Siedepunkts führt dazu. deshalb, die Schlüsselunterschied Zwischen dem Gefrierpunkt -Depression und der Erhöhung des Siedepunkts ist das Die Die Gefrierpunkt -Depression verringert den Gefrierpunkt einer Lösung, während die Erhöhung des Siedepunkts den Siedepunkt einer Lösung erhöht.
Gefrierpunkt -Depression und Siedepunkt Erhebung sind kolligative Eigenschaften der Materie. Dies bedeutet, dass sie nur von der Menge der gelösten Stoffe abhängen, nicht von der Art des gelösten Stoffes.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Gefrierpunktdepression
3. Was ist die Erhöhung des Siedepunkts
4. Seite an Seitenvergleich - Gefrierpunkt -Depression im Vergleich zur Erhöhung der Siedepunkt in tabellarischer Form
5. Zusammenfassung
Was ist Gefrierpunktdepression?
Die Gefrierpunktdepression ist die Abnahme des Gefrierpunkts eines Lösungsmittels aufgrund der Zugabe eines gelösten Stoffes in das Lösungsmittel. Es ist ein kolligatives Eigentum. Dies bedeutet, dass die Gefrierpunktdepression nur von der Menge der gelösten Stoffe abhängt, nicht von der Art des gelösten Stoffes. Bei der Einfrierpunktkrise nimmt der Gefrierpunkt des Lösungsmittels auf einen niedrigeren Wert als der des reinen Lösungsmittels ab. Die Gefrierpunktdepression ist der Grund, warum Meerwasser auch bei 0 ° C im flüssigen Zustand bleibt (der Gefrierpunkt von reinem Wasser). Die Gefrierpunktdepression kann wie unten angegeben werden.
ΔtF = Tf (Lösungsmittel) - Tf (Lösung)
Oder
ΔtF = KFM
In diesem,
- ΔtF ist die Gefrierpunktdepression,
- Tf (Lösungsmittel) ist der Gefrierpunkt von reinem Lösungsmittel
- Tf (Lösung) ist der Gefrierpunkt der Lösung (Lösungsmittel + gelöste Stoffe)
- KF ist die Gefrierpunkt -Depression konstant
- M ist die Molalität der Lösung.
Der zugesetzte gelöste gelöste sollte jedoch ein nicht flüchtiger gelöster Stoff sein, wenn nicht der gelöste Stoff den Gefrierpunkt des Lösungsmittels nicht beeinflusst, da er leicht flüchtig wird. Nicht nur für Lösungen, sondern auch dieses Konzept kann auch verwendet werden, um die Änderungen des Gefrierpunkts solider Mischungen zu erklären. Die fein pulverisierte feste Verbindung hat einen niedrigeren Gefrierpunkt als die reine feste Verbindung, wenn Verunreinigungen vorhanden sind (Feststoffmischung).
Der Gefrierpunkt ist die Temperatur, bei der der Dampfdruck eines Lösungsmittels und der Dampfdruck die feste Form dieses Lösungsmittels gleich ist. Wenn diesem Lösungsmittel ein nichtflüchtiger gelöster gelöster gelöster zugesetzt wird, nimmt der Dampfdruck des reinen Lösungsmittels ab. Dann kann die feste Form des Lösungsmittels mit dem Lösungsmittel auch bei niedrigeren Temperaturen im Gleichgewicht bleiben als der normale Gefrierpunkt.
Was ist die Erhöhung des Siedepunkts?
Die Erhöhung des Siedepunkts ist die Erhöhung des Siedepunkts eines Lösungsmittels aufgrund der Zugabe eines gelösten Stoffes in das Lösungsmittel. Hier ist der Siedepunkt der Lösung (nach Zugabe von gelösten gelösten) höher als der des reinen Lösungsmittels. Daher ist die Temperatur, bei der die Lösung zu kochen beginnt.

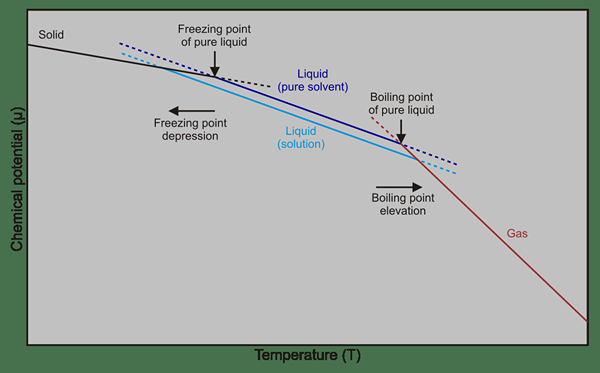
Abbildung 01: Gefrierpunkt- und Siedepunktunterschiede zwischen reinem Lösungsmittel und Lösungen (Lösungsmittel + gelöste Stoffe)
Der zugesetzte gelöste gelöste sollte jedoch ein nichtflüchtiger gelöster gelöster sein, sonst wird der gelöste gelöste sich im Lösungsmittel verflüchtet, anstatt sich aufzulösen, anstatt sich aufzulösen. Die Erhöhung der Siedepunkt ist auch eine kolligative Eigenschaft, so dass sie nur von der Menge der gelösten gelösten Stoffe abhängt (nicht von der Art des gelösten Stoffes).
ΔtB = TB (Lösungsmittel) - TB (Lösung)
Oder
ΔtB = KBM
In diesem,
- ΔtB Ist die Erhöhung der Siedepunkte
- TB (Lösungsmittel) ist der Siedepunkt von reinem Lösungsmittel
- TB (Lösung) ist der Siedepunkt der Lösung (Lösungsmittel + gelöste Stoffe)
- KB Ist die Erhöhung der Siedepunktkonstante
- M ist die Molalität der Lösung
Ein häufiges Beispiel für dieses Phänomen ist der Siedepunkt einer wässrigen Salzlösung. Eine Salzlösung kocht bei höheren Temperaturen als 100 ° C (Siedepunkt von reinem Wasser).
Was ist der Unterschied zwischen Gefrierpunkt -Depression und Siedepunkterhöhung?
Gefrierpunktpunkt gegen Siedepunkterhöhung | |
| Die Gefrierpunktdepression ist die Abnahme des Gefrierpunkts eines Lösungsmittels aufgrund der Zugabe eines gelösten Stoffes in das Lösungsmittel. | Die Erhöhung des Siedepunkts ist die Erhöhung des Siedepunkts eines Lösungsmittels aufgrund der Zugabe eines gelösten Stoffes in das Lösungsmittel. |
| Temperatur | |
| Die Gefrierpunktdepression verringert den Gefrierpunkt einer Lösung. | Die Erhöhung der Siedepunkt erhöht den Siedepunkt einer Lösung. |
| Prinzip | |
| Gefrierpunkt -Depression führt zu einer Lösung, um bei einer niedrigeren Temperatur als das reine Lösungsmittel einzufrieren. | Erhöhungspunkterhöhung führt dazu, dass eine Lösung bei einer höheren Temperatur als das reine Lösungsmittel kochen kann. |
| Gleichung | |
| Die Gefrierpunktdepression wird durch ΔT gegebenF = Tf (Lösungsmittel) - Tf (Lösung) oder δtF = KFM. | Erhöhung des Siedepunkts ΔTB = TB (Lösungsmittel) - TB (Lösung) oder δtB = KBM. |
Zusammenfassung -Einfrieren Punktdepression gegen Kochpunkterhöhung
Gefrierpunkt -Depression und Siedepunkt Erhebung sind zwei wichtige kolligative Eigenschaften von Materie. Der Unterschied zwischen Gefrierpunkt -Depression und Siedepunkterhöhung besteht darin, dass die Gefrierpunktdepression den Gefrierpunkt einer Lösung verringert, während die Erhöhung des Siedepunkts den Siedepunkt einer Lösung erhöht.
Referenz:
1.Helmenstine, Anne Marie. „Welche Erhöhung des Siedepunkts ist und wie es funktioniert.”Thoughtco. Hier verfügbar
2.„Kochpunkthöhe.Wikipedia, Wikimedia Foundation, 13. März. 2018. Hier verfügbar
3."Gefrierpunkterniedrigung.”Chemistry Libretexte, Libretexte, 19. Februar. 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.'Gefrierpunkt-Depression und Siedepunkt Höhe von Tomas Erderivative Arbeit (CC BY-SA 3.0) über Commons Wikimedia


