Unterschied zwischen Halogen- und Metallhalogenid

Der Schlüsselunterschied Zwischen Halogen- und Metallhalogenid ist das Ein Halogen ist ein chemisches Element der Gruppe 17, während Metallhalogenid eine Verbindung ist, die ein Metall und ein Halogen enthält.
Metallhalogenide sind ionische oder kovalente Verbindungen von Halogenen. Ein Halogen ist ein chemisches Element und alle Elemente in der Gruppe 17 der Periodenzüchter sind im Allgemeinen als Halogene bezeichnet.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Halogen
3. Was ist Metallhalogenid
4. Seite an Seitenvergleich - Halogen gegen Metall Halogenid in tabellarischer Form
5. Zusammenfassung
Was ist Halogen?
Halogene sind chemische Elemente der Gruppe 17 in der Periodenzüchtertabelle. Die Gruppe enthält fünf chemische Elemente, darunter Fluor (F), Chlor (CL), Brom (BR), Jod (I) und Astatine (at). Oft verwenden wir das Symbol X, um einen Halogen zu symbolisieren. Der Begriff Halogen bezieht sich auf „Salzproduktion“. Das bedeutet; Diese chemischen Elemente neigen dazu, Salze bei der Reaktion von NG mit Metallen zu bilden. Eine Reaktion zwischen einem Halogen und einem Metall erzeugt eine breite Palette von Salzverbindungen. Die Halogengruppe enthält Elemente, die in verschiedenen Phasen der Materie existieren. Zum Beispiel sind Fluor und Chlor Gase, während Brom eine Flüssigkeit ist und Jod bei Raumtemperatur ein Feststoff ist.

Abbildung 01: Chlor, Brom und Jod
Die Gruppe von Halogenen in der Periodenzüchtungstabelle, die Reaktivität abnimmt, die Größe eines Atoms steigt, die Elektronegativität nimmt ab, die Phase der Materie ändert sich von einem Gas zu Feststoff usw. Bei der Betrachtung der Verwendung der Halogene sind sie als Desinfektionsmittel nützlich, wichtig für Halogenlampen, nützlich als Zutaten in einigen Medikamenten usw.
Was ist ein Metallhalogenid?
Metallhalogenide sind ionische oder kovalente Verbindungen von Metallen und Halogenen. Einige kovalente Metallhalogenidverbindungen treten entweder als diskrete Moleküle oder als polymere Strukturen auf. Alle Halogene neigen dazu, mit Metallen zu reagieren und Metallhalogenide zu bilden.
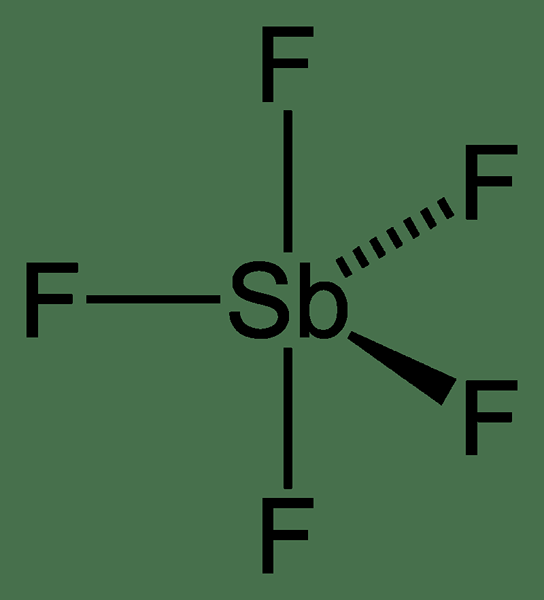
Abbildung 02: Struktur des Metallhalogenid -Antimonfluorids
Theoretisch können wir über die Reaktion zwischen den chemischen Elementen ein Metallhalogenid produzieren, aber diese Art der Reaktion ist praktisch sehr exotherm. Daher können wir einige andere Methoden wie Neutralisationsreaktion von Metalloxiden und Hydroxiden verwenden.
Bei der Betrachtung der Eigenschaften sind ionische Metallhalogenide hochstabil; So haben sie tendenziell hohe Schmelz- und Siedepunkte. Diese Verbindungen lösen sich jedoch frei in Wasser auf. Einige Verbindungen sind ebenfalls entflüssig. Aber sie sind in organischen Lösungsmitteln schlecht löslich. Darüber hinaus haben diskrete Metallhalogenidmoleküle vergleichsweise niedrige Schmelz- und Siedepunkte.
Was ist der Unterschied zwischen Halogen- und Metallhalogenid?
Der Schlüsselunterschied zwischen Halogen und Metallhalogenid besteht darin, dass ein Halogen ein chemisches Element der Gruppe 17 ist, während Metallhalogenid eine Verbindung mit Metall und Halogen ist. Mit anderen Worten, ein Halogen ist ein chemisches Element, während Metallhalogenid eine chemische Verbindung ist.
Darüber hinaus besteht ein weiterer Unterschied zwischen Halogen und Metallhalogenid darin, dass in verschiedenen Phasen der Materie ein Halogen existieren kann solide Phase.

Zusammenfassung - Halogen gegen Metallhalogenid
Zusammenfassend lässt sich sagen. Grundsätzlich ist Halogen ein chemisches Element, während Metallhalogenid eine chemische Verbindung ist.
Referenz:
1. "Halogen.”Wikipedia, Wikimedia Foundation, 30. Juni 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Halogenen" von w. Oelen - Wissenschaft lebend gemacht: Chemie/Elem - Halogenstransferred von EN.Wikipedia to Commons von Nutzern: тizinus фмйлесуда Verwenden Sie CommonShelper (CC BY-SA 3).0) über Commons Wikimedia
2. "Pantimony-Pentafluorid-2D" (Public Domain) über Commons Wikimedia


