Unterschied zwischen hartem Wasser und schwerem Wasser

Schlüsselunterschied - hartes Wasser gegen schweres Wasser
Der wichtigste Unterschied zwischen hartem Wasser und schwerem Wasser ist ihre Zusammensetzung als beide Typen, „hartes Wasser“ und „schweres Wasser“ beziehen sich auf das Wasser mit zwei Wasserstoffatomen und einem Sauerstoffatom im Wassermolekül. Wenn wir das betrachten molekulare Zusammensetzung von schwerem Wasser, Es Enthält mehr Deuteriumatome als Wasserstoffatome. Die molekulare Zusammensetzung der hartes Wasser ist gleich wie das normale Wasser, aber seines Mineralzusammensetzung (Magnesium -mg und Calcium - CA) ist relativ höher als das weiche Wasser.
Was ist schweres Wasser?
Ein Wassermolekül enthält zwei Wasserstoffatome und ein Sauerstoffatom. Wasserstoff hat drei Isotope; Protium (99.98%), Deuterium und Tritium. Protium hat ein Elektron und ein Neutron. Deuterium hat neben dem Elektron und dem Proton ein Neutron im Kern zusätzlich. Deuterium ist so doppelt so schwerer als das am häufigsten vorkommende Wasserstoffatom.
Schweres Wasser enthält einen großen Anteil an Deuteriumatomen als das übliche Wasserstoffatom. Daher ist sein Molekulargewicht und die Dichte höher als das normale Wasser. Es wird gesagt, dass die Dichte von schwerem Wasser 11 -mal höher ist als die des normalen Wassers.
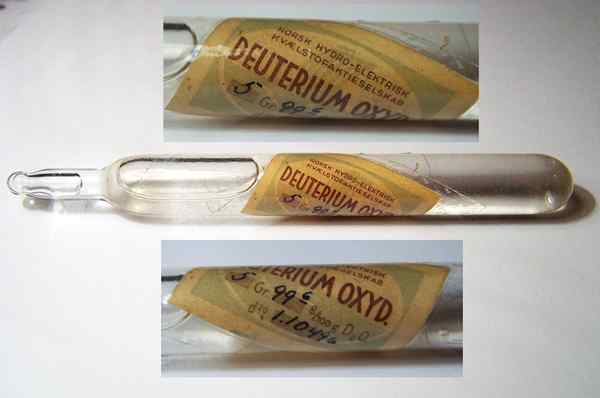
Eine historische Probe von „schwerem Wasser“, gepackt in einer versiegelten Kapsel.
Was ist hartes Wasser?
Im Allgemeinen enthält Wasser eine gewisse Menge Mineralien wie Magnesium, Kalzium und Kalium. Hartwasser enthält jedoch mehr Mineralien, insbesondere Magnesium (Mg) und Calcium (CA) als normales Wasser (weiches Wasser). Aus dieser Tatsache ist die Härte des harten Wassers größer als die Härte des normalen Wassers. Dies geschieht, wenn das Oberflächenwasser durch den Boden in die Grundwasserschicht fließt, indem die Mineralien im frei fließenden Wasser gelöst werden.
Hartes Wasser wirkt sich nicht auf die menschliche Gesundheit aus, sondern führt zu so vielen zusätzlichen Problemen, wie z. 
Was ist der Unterschied zwischen hartem Wasser und schwerem Wasser?
Definition von hartem Wasser und schwerem Wasser
Schweres Wasser: Schweres Wasser ist Wasser, das einen erheblichen Anteil an Deuteriumatomen enthält, der in Kernreaktoren verwendet wird
Hartes Wasser: Hartwasser ist Wasser, das eine maßgebliche Menge an gelösten Salzen von Kalzium und Magnesium enthält.
Eigenschaften von hartem Wasser und schwerem Wasser
Komposition
Schweres Wasser: Schweres Wasser enthält einen großen Anteil an Deuterium (ein zusätzliches Neutron im Kernatome) als das normale Wasser. Es enthält sowohl Wasserstoffatome als auch Deuteriumatome, die die Wassermoleküle mit der molekularen Formel als D bilden2O (Deuteriumoxid) und HDO (Wasserstoffdeuteriumoxid).
Hartes Wasser: In der molekularen Ebene ähnelt die Zusammensetzung von hartem Wasser der von normalem Wasser (H2Ö). Aber es enthält mehr Mineralien; Magnesium und Kalzium als das normale Trinkwasser.
Physikalische und chemische Eigenschaften
Schweres Wasser: Physikalische und chemische Eigenschaften von schwerem Wasser ähneln dem normalen Wasser, hat aber einen Wert mit hoher Dichte. Das Molekulargewicht des schweren Wassers zeigt keine signifikante Veränderung, da das einzelne Sauerstoffatom etwa 89% zum Molekulargewicht beiträgt. Die biologischen Eigenschaften von schwerem Wasser unterscheiden sich vom normalen Wasser.
Hartes Wasser: Härte ist die Haupteigenschaft, die sich erheblich von normalem Wasser unterscheidet.
USGS -Klassifizierung der Wasserhärte
| Härte / MGL-1 | Art des Wassers |
| 0-60 | Weiches Wasser |
| 61-120 | Mäßig hartes Wasser |
| 121-180 | Hartes Wasser |
| < 180 | Sehr hartes Wasser |
Die empfohlene Grenze der Härte im Trinkwasser beträgt 80-100 mGL-1
Gesundheitseffekt
Schweres Wasser: Eine gewisse Menge Deuterium ist im menschlichen Körper vorhanden, aber eine große Menge an Deuterium verursacht schädliche gesundheitliche Auswirkungen im menschlichen Körper. Es kann sogar zum Tod führen.
Hartes Wasser: Hartes Wasser verursacht keine gesundheitlichen Auswirkungen auf den menschlichen Körper, aber es verursacht einige andere Probleme wie das Blockieren von Wasserrohren und das Verlassen von Mineralablagerungen an Heizungen, Kochausrüstung und Badböden. Um diese durch das harten Wasser verursachten Probleme zu überwinden, werden die Mineralien entfernt. Dies wird als Erweichen bezeichnet. Die am häufigsten verwendete wirksame Methode ist die Ionenaustauschharze als Enthärter.
Bild mit freundlicher Genehmigung: "Dripping Faucet 1" von Benutzer: Dschwen - eigene Arbeit. (CC BY-SA 2.5) über Wikimedia Commons "Deuteriumoxid Norsk" von Alchemist-HP (Talk) (www.Pse-Mendelejew.de) - eigene Arbeit. (Fal) über Commons


