Unterschied zwischen Hexan und N-Hexan
Der SchlüsselunterschiedeE zwischen Hexan und N-Hexan ist das Hexane hat verzweigte Strukturen.
Organische Moleküle sind Moleküle, die aus Kohlenstoffen bestehen. Kohlenwasserstoffe sind organische Moleküle, die nur aus Kohlenstoff- und Wasserstoffatomen bestehen. Kohlenwasserstoffe können aromatisch oder aliphatisch sein. Sie sind hauptsächlich in wenige Typen als Alkane, Alkene, Alkine, Cycloalkane und aromatische Kohlenwasserstoffe unterteilt. Hexan und N-Hexan sind Alkane oder auf andere Weise, die als gesättigte Kohlenwasserstoffe bezeichnet werden. Sie haben die höchste Anzahl von Wasserstoffatomen, die ein Molekül aufnehmen kann. Alle Bindungen zwischen Kohlenstoffatomen und Wasserdingen sind einzelne Bindungen. Daher ist die Bindungsrotation zwischen allen Atomen zulässig. Sie sind die einfachste Art von Kohlenwasserstoffen. Gesättigte Kohlenwasserstoffe haben die allgemeine Formel von CNH2N+2. Diese Bedingungen unterscheiden sich für die Cycloalkane leicht, da sie zyklische Strukturen haben.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Hexan?
3. Was ist N-Hexan
4. Nebenseitiger Vergleich - Hexan gegen N -Hexan in tabellarischer Form
5. Zusammenfassung
Was ist Hexan??
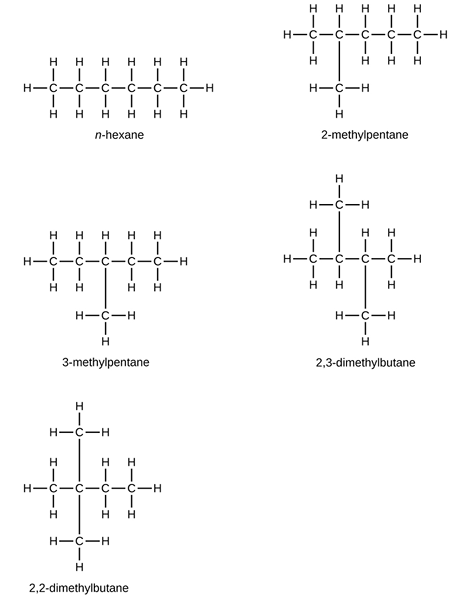
Wie oben erwähnt, ist ein Kohlenwasserstoff ein gesättigtes Alkan. Es hat sechs Kohlenstoffatome; Daher hat die Formel von C6H14. Die Molmasse von Hexan beträgt 86.18 g Mol–1. Hexan ist der gebräuchliche Name, der verwendet wird, um alle Moleküle mit dieser Formel anzuzeigen. Es gibt eine Reihe von strukturellen Isomeren, die wir für diese Formel entsprechen können, aber in der IUPAC-Nomenklatur verwenden wir Hexan speziell, um ein unverzweigtes Molekül zu erhalten, und es ist auch als N-Hexan bekannt. Andere strukturelle Isomere sind wie methylierte Moleküle von Pentan und Butan. Sie sind als Isohexan und Neohexan bekannt. Sie haben die folgenden Strukturen.

Aus diesen Hexanstrukturen sind 2-Methylpentan, 3-Methylpentan und 2,3-Dimethylbutan Beispiele für Isohexan, während 2,2-Dimethylbutane ein Beispiel für ein Neohexan ist.
Hexan wird hauptsächlich im Rohöl -Raffinerierungsprozess hergestellt. Hexan wird extrahiert, wenn das Öl bei 65-70 ° C kocht. Da Hexan -Isomere etwas ähnliche Siedepunkte haben, verdampfen sie im gleichen Temperaturbereich. Ihre Schmelzpunkte sind jedoch unterschiedlich. Hexan ist in flüssiger Form bei Raumtemperatur und hat einen Geruch wie Benzin. Es ist eine farblose Flüssigkeit. Hexan löst sich leicht in Wasser auf. Bei Raumtemperatur verdampft es langsam in die Atmosphäre. Hexandampf kann explosiv sein und Hexan selbst ist sehr brennbar. Hexan ist ein unpolares Lösungsmittel und wird als Lösungsmittel im Labor verwendet.
Nicht nur reines Hexan wird als Lösungsmittel verwendet, sondern es gibt auch verschiedene Arten von Lösungsmitteln, die mit Hexan hergestellt werden. Abgesehen davon wird Hexane verwendet, um Lederprodukte, Klebstoffe, für Textilherstellung, Reinigungsprodukte usw. herzustellen, usw. Hexan wird verwendet, um unpolare Substanzen wie Öl und Fett bei der Analyse von Wasser und Boden zu extrahieren.
Was ist N-Hexan?
n -hexan oder normales Hexan ist die ungezügelte Struktur von Hexan mit der molekularen Formel C6H14. Der Siedepunkt von N-Hexan ist 68.7 ÖC, während der Schmelzpunkt –95 beträgt.3 ÖC. N-Hexan wird beim Extrahieren von Öl aus Samen wie Saflor, Sojabohnen und Baumwolle verwendet.
Was ist der Unterschied zwischen Hexan und N-Hexan?
Hexan ist eine Mischung der Verbindungen mit der Formel C6H14. Hexane hat verzweigte Strukturen. N-Hexan ist ein strukturelles Isomer von Hexan. Darüber hinaus hat N-Hexane einen höheren Siedepunkt im Vergleich zu anderen Hexanen. Insgesamt fallen ihre Siedepunkte jedoch in einen kleinen Temperaturbereich. Zusätzlich hat N-Hexan einen beträchtlichen Dampfdruck bei Raumtemperatur.
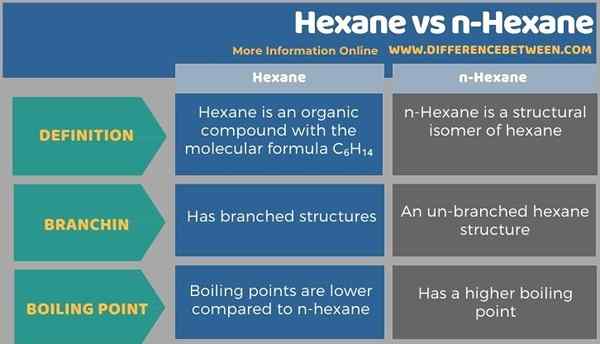
Zusammenfassung -Hexan gegen N -Hexan
N-Hexan ist ein strukturelles Isomer von Hexan. Der wichtigste Unterschied zwischen Hexan und N-Hexan besteht darin, dass Hexan verzweigte Strukturen hat, während N-Hexan eine ungezügelte Hexanstruktur ist.
Bild mit freundlicher Genehmigung:
1. "CNX Chem 20 01 EX1 15 IMG" von OpenStax - (CC von 4.0) über Commons Wikimedia


