Unterschied zwischen Wasserstoffbindungsspender und Akzeptor
Der Schlüsselunterschied Zwischen Wasserstoffbindungsspender und Akzeptor ist das Wasserstoffbrückenbindungsspender enthält das Wasserstoffatom, das an der Wasserstoffbrückenbindungsbildung beteiligt ist, während der Akzeptor der Wasserstoffbrückenbindung einsame Elektronenpaare enthält.
Eine Wasserstoffbindung ist eine schwache Bindung zwischen zwei Molekülen, die sich aus einer elektrostatischen Anziehungskraft zwischen einem Proton in einem Molekül und einem elektronegativen Atom in der anderen ergeben. Diese beiden Verbindungen, die an der Wasserstoffbindungsbildung beteiligt sind, werden als Wasserstoffbrückenbindungsspender und Akzeptor bezeichnet.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Wasserstoffbrückenbindungsspender
3. Was ist Wasserstoffbrückenbindungsakzeptor
4. Seite an Seitenvergleich - Wasserstoffbrückenbindungsspender gegen Akzeptor in tabellarischer Form
5. Zusammenfassung
Was ist Wasserstoffbrückenbindungsspender?
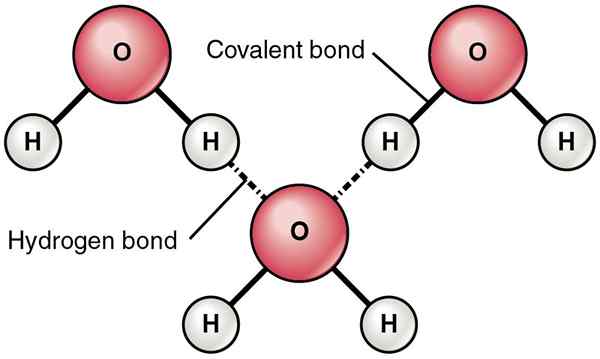
Wasserstoffbrückenbindungsspender ist die chemische Verbindung, die Protonen enthält, die gespendet werden sollen. Hier sind Protonen Wasserstoffatome. Der Wasserstoffbrückenbindungsspender sollte diese Wasserstoffatome enthalten, die kovalent an sich selbst gebunden sind. Zum Beispiel hat Wasser zwei Wasserstoffatome, die direkt über kovalente chemische Bindungen am Sauerstoffatom gebunden sind. Daher kann es Wasserstoffbrückenbindungen mit anderen Molekülen bilden.

Abbildung 01: Wasserstoffbrückenbindungen zwischen Wassermolekülen
Obwohl Aldehyde und Ketone Wasserstoffatome enthalten, haben sie keine Wasserstoffatome direkt an die Sauerstoffatome gebunden. Daher sind sie keine Wasserstoffbrückenspender.
Was ist Wasserstoffbrückenbindungsakzeptor?
Wasserstoffbrückenbindungsakzeptor ist die chemische Verbindung, die die einzigen Elektronenpaare enthält, die an der Wasserstoffbrückenbindungsbildung beteiligt sind. Diese Verbindung sollte ein elektronegativeres Atom (elektronegativer als Wasserstoff) mit einzigen Elektronenpaaren enthalten. Dann kann es Protonen von einem Spender anziehen. Darüber hinaus sind die elektronegativen Atome, die normalerweise an der Wasserstoffbrückenbindung beteiligt sind, Sauerstoff, Stickstoff und Fluor.
Was ist der Unterschied zwischen Wasserstoffbrückenspender und Akzeptor?
Eine Wasserstoffbrücke bildet sich zwischen einem Wasserstoffspender und einem Akzeptor. Der Schlüsselunterschied zwischen Wasserstoffbrückenbindungsspender und Akzeptor besteht darin. Ein weiterer Unterschied zwischen Wasserstoffbrückenspender und Akzeptor besteht darin, dass der Wasserstoffbrückenbindungsspender Wasserstoffatome direkt über kovalente Bindungen an die Verbindung enthalten muss.

Zusammenfassung -Wasserstoffbindungsspender gegen Akzeptor
Grundsätzlich ist eine Wasserstoffbindung eine Bindung, die zwischen einem Wasserstoffspender und einem Akzeptor bildet. Der wichtigste Unterschied zwischen Wasserstoffbrückenendonor und Akzeptor besteht darin, dass der Wasserstoffbrückenbindungsspender das Wasserstoffatom enthält, das an der Wasserstoffbrückenbindungsbildung beteiligt ist, während der Akzeptor der Wasserstoffbrückenbindung einsame Elektronenpaare enthält.
Referenz:
1. „Wasserstoffbrücke.”Chemistry Libretexten, Libretexte, 5. Juni 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "210 Wasserstoffbrückenbindungen zwischen Wassermolekules -01" vom OpenStax College - Anatomy & Physiology, Connexions -Website. 19. Juni 2013 (CC von 3.0) über Commons Wikimedia