Unterschied zwischen Hydrolyse und Dehydration

Hydrolyse gegen Dehydration
Wasser ist sehr wichtig für das Überleben der Lebewesen. Es hat viele Verwendungen. Wenn Wasser nicht in ausreichenden Mengen ist, betrifft es viele wichtige Reaktionen im Körper.
Hydrolyse
Dies ist eine Reaktion, bei der eine chemische Bindung unter Verwendung eines Wassermoleküls gebrochen wird. Während dieser Reaktion wird ein Wassermolekül in ein Proton und ein Hydroxidion aufgeteilt. Dann werden diese beiden Ionen zu zwei Teilen des Moleküls hinzugefügt, in denen die Bindung gebrochen ist. Zum Beispiel finden Sie ein Ester. Die Esterbindung ist zwischen -co und -o.
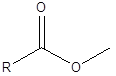
In der Hydrolyse trägt das Proton aus dem Wasser zur -o -Seite, und das Hydroxid -Ion fügt die -co -Seite hinzu. Daher bilden sich aufgrund der Hydrolyse ein Alkohol und eine Carboxsäure, die bei der Bildung des Esters die Reaktanten waren.
Hydrolyse ist wichtig, um die Polymere, die durch Kondensationspolymerisation hergestellt wurden. Kondensationspolymerisierungen sind eine Art chemischer Reaktion, bei der kleine Moleküle zusammenkommen, um ein großes einzelnes Molekül zu bilden. Die Reaktion findet innerhalb von zwei funktionellen Gruppen in den Molekülen statt. Andere charakteristische Merkmale einer Kondensationsreaktion ist, dass während der Reaktion ein kleines Molekül wie Wasser verloren geht. Hydrolyse ist also der reversible Prozess der Kondensationspolymerisation. Das obige Beispiel zeigt eine Hydrolyse eines organischen Moleküls.
Die meisten Hydrolysereaktionen von organischen Molekülen müssen mit starken Säuren und Basen katalysiert werden. Wenn jedoch ein Salz einer schwachen Säure oder einer schwachen Basis in Wasser gelöst ist, wird auch hydrolyse gemacht. Wasser ionisiert und auch das Salz dissoziiert zu einem Kation und Anion. Wenn beispielsweise Natriumacetat in Wasser gelöst wird, reagiert Acetat mit Protonen und bilden Essigsäure, während Natrium mit Hydroxylionen interagiert.
In lebenden Systemen sind Hydrolysereaktionen sehr häufig. Im Verdauungssystem findet dies statt, um die Lebensmittel zu verdauen, die wir einnehmen. Die Erzeugung von Energie aus ATP ist auch auf eine Hydrolysereaktion der Pyrophosphatverbindungen zurückzuführen. Die meisten dieser biologischen Hydrolysereaktionen sind mit Enzymen katalysiert.
Dehydration
Dehydration ist der Zustand, unter dem der normale Wasserniveau nicht erforderlich ist. Wenn sich dies auf biologische Systeme bezieht, wird dies durch einen schweren Verlust der Körperflüssigkeit (zum Beispiel Blut) verursacht. Es gibt drei Arten von Dehydration als hypotonisch, hypertonisch und isotonisch. Da der Elektrolytespiegel den Wasserstand direkt beeinflusst, ist es wichtig, den Elektrolytbilanz innerhalb des Körpers aufrechtzuerhalten, um den osmotischen Gleichgewicht aufrechtzuerhalten.
Dehydration kann auf verschiedene Arten verursacht werden. Überschüssige Urinübergang, Durchfall, Blutverlust aufgrund von Unfällen und übermäßiges Schwitzen sind einige der gängigen Wege. Dehydration kann Kopfschmerzen, verringerten Blutdruck, Schwindel, Ohnmacht verursachen. In extremem Zustand der Dehydration verursacht es Bewusstlosigkeit und Tod.
Dehydration kann durch Trinken ausreichend Wasser verhindert werden. Wenn viel Wasser aus dem Körper verloren geht, sollte es wiedergegeben werden (orale Rehydratisierung, Injektion usw.).
| Was ist der Unterschied zwischen Hydrolyse und Dehydration? • Dehydration ist der Zustand, dass weniger Wasserbetrag als der normale Niveau ist. • Hydrolyse ist eine Reaktion, bei der eine chemische Bindung unter Verwendung eines Wassermoleküls gebrochen wird. • Dehydration beeinflusst die Hydrolysereaktionen, da für die Hydrolysereaktionen Wasser vorhanden sein sollten. |


