Unterschied zwischen Markovnikov und Anti-Markovnikov-Regel
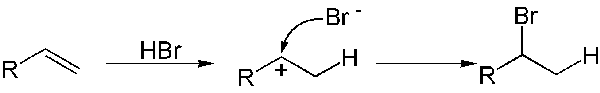
Schlüsselunterschied - Markovnikov gegen Anti -Markovnikov -Regel
In den frühen 1870er Jahren stellte ein russischer Chemiker namens Wladimir Markonikov eine Regel ab, die auf einer Reihe empirischer Beobachtungen basiert. Die Regel wurde als die Regel des Markovnikov veröffentlicht. Die Markovnikovs Regel hilft, die resultierende Formel von Alkan vorherzusagen, wenn eine Verbindung mit der allgemeinen Formel von HX (HCL, HBR oder HF) oder H2O wird zu einem asymmetrischen Alken (wie Propan) hinzugefügt. Es ist möglich, die Neben- und Hauptprodukte umzukehren, wenn die Reaktionsbedingungen geändert werden, und Dieser Prozess wird als Anti-Markovnikov-Addition bezeichnet. Der Schlüsselunterschied Zwischen Markovnikov-Regel und der Anti-Markovnikov-Regel wird unten erläutert.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Markovnikov -Regel
3. Was ist Anti-Markovnikov-Regel
4. Seite an Seite Vergleich - Markovnikov gegen Anti -Markovnikov -Regel in tabellarischer Form
5. Zusammenfassung
Was ist Markovnikov -Regel?
Die Definition der Markovnikov -Regel ist, wenn die Zugabe von Protizensäure mit der Formel von HX (wobei x = Halogen) oder h2O (als H-OH angesehen) an ein Alken, Wasserstoff hält sich mit der größeren Anzahl von Wasserstoffatomen an den doppelt gebundenen Kohlenstoff an, während sich der Halogen (x) an den anderen Kohlenstoff befindet. Daher wird diese Regel oft als "Die Reichen werden reicher" interpretiert. Die Regel kann unter Verwendung der Reaktion von Propen mit Hydrobromensäure (HBR) wie folgt veranschaulicht werden.
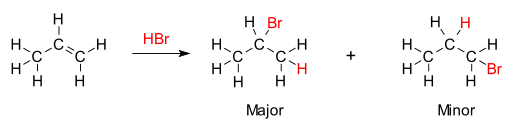
Abbildung 01: Markovnikovs Regel wird durch die Reaktion von Propen mit Hydrobromensäure veranschaulicht
Die gleiche Regel wird angewendet, wenn ein Alken mit Wasser zu Alkohol reagiert. Die Hydroxylgruppe (-OH) trägt zum doppelt gebundenen Kohlenstoff mit der größeren Anzahl von C-C-Bindungen bei. Laut Markovnikov -Regel hat das Hauptprodukt, wenn ein HX zu einem Alken hinzugefügt wird. Daher ist dieses Produkt stabil. Es ist jedoch immer noch möglich, ein weniger stabiles Produkt zu bilden, oder wir nennen es ein kleines Produkt, in dem H -Atom -Bindungen zu einer stärker ersetzten Position der C = C.
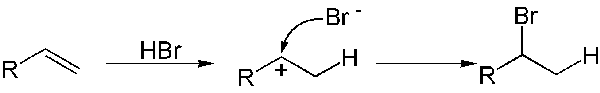
Abbildung 02: Wasserstoffbromidzugang zu einem Alken
Der Mechanismus der Zugabe von HX zu einem Alken kann in zwei Schritten erklärt werden (siehe Abb. 02). Erstens die Zugabe eines Protons (h+) wird stattfinden, wenn die C = C -Doppelbindung von Alken mit H reagiert+ von HX (in diesem Fall ist es HBR), um eine Kohlensäure -Zwischenprodukt zu bilden. Dann findet die Reaktion eines Elektrophils und eines Nucleophils statt, um eine neue kovalente Bindung zu bilden. In unserem Fall Br- Reagiert mit Carbonation Intermediate, was positiv verantwortlich ist, um das Endprodukt zu bilden.
Was ist Anti-Markovnikov-Regel?
Anti-Markovnikov-Regel erklärt das Gegenteil der ursprünglichen Aussage von Markovnikovs Regel. Wenn HBR in Gegenwart von Peroxid zu einem Alken hinzugefügt wird, ist H-Atombindungen zu doppelt gebundenem Kohlenstoff mit weniger C-H. Dieser Effekt ist auch als bekannt als Kharash -Effekt oder Peroxideffekt. Die Addition der Anti-Markovnikov findet auch statt, wenn Reaktanten ultraviolettes Licht ausgesetzt sind. Dies ist das genaue Gegenteil der Markovnikov -Regel. Die Anti-Markovnikov-Regel ist jedoch nicht der genaue umgekehrte Prozess von Markovnikov Addition, da die Mechanismen dieser beiden Reaktionen völlig unterschiedlich sind.
Die Markovnikov-Reaktion ist ein ionischer Mechanismus, während die Anti-Markovnikov-Reaktion ein frei-radikaler Mechanismus ist. Der Mechanismus findet als Kettenreaktion statt und hat drei Schritte. Der erste Schritt ist der Ketteninitiationsschritt, bei dem photochemische Dissoziation von HBR oder Peroxid stattfindet, um BR- und H-freie Radikale zu bilden. Im zweiten Schritt greift BR freie Radikale das Alken -Molekül an, um zwei mögliche bromoalkylfreie Radikale zu bilden. 2 ° frei Radikal ist stabiler und wird überwiegend gebildet.
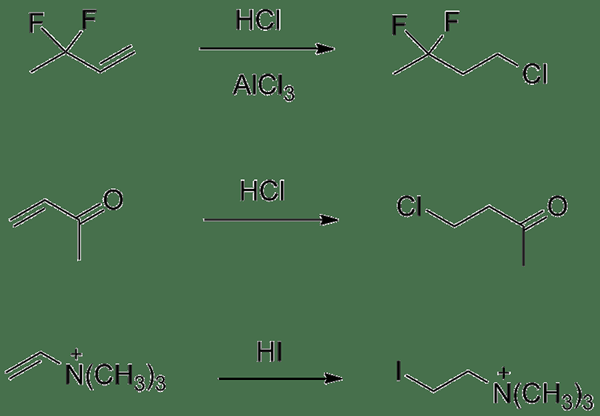
Abbildung 3: Anti-Markovnikov-Additionsbeispiele
Während des letzten Schritts reagiert das stabilere Bromoalkyl-freie Radikal mit HBR Anti-Markovnikov-Produkt sowie ein weiteres bromfreies Radikal, das die Kettenreaktion kontinuierlich kontinuierlich. Im Gegensatz zu HBR, HCL und HI führen nicht zu Anti-Markovnikov-Produkten. Es liegt daran. Obwohl die H-I-Bindung viel schwächer ist, ist die Bildung von i2 wird als C-I-Bindung in relativ instabiler bevorzugt.
Was ist der Unterschied zwischen Markovnikov und Anti -Markovnikov -Regel?
Markovnikov gegen Anti -Markovnikov -Regel | |
| Die Markovnikov -Regel erklärt, wann die Zugabe von Protizensäure mit der Formel von HX (wobei x = Halogen) oder h2O (als H-OH angesehen) an ein Alken, Wasserstoff hält sich mit der größeren Anzahl von Wasserstoffatomen an den doppelt gebundenen Kohlenstoff an, während sich der Halogen (x) an den anderen Kohlenstoff befindet. | Die Anti-Markovnikov-Regel erklärt, wann HBR in Gegenwart von Peroxid, H-Atombindungen zu doppelt gebundenem Kohlenstoff mit weniger C-H-Bindungen, zu einem Alken hinzugefügt wird, während BR-Bindungen an den anderen Kohlenstoff mit mehr C-H |
| Mechanismus | |
| Ionenmechanismus | Freier Radikalmechanismus |
| Reaktanten | |
| HCl, HBR, HI oder H2Ö | Nur HBR (nicht HCl oder HI unterziehen sich dieser Additionsreaktion) |
| Mittel/Katalysator | |
| Es ist kein Medium erforderlich | Peroxid oder Ultraviolett müssen vorhanden sein |
Zusammenfassung - Markovnikov gegen Anti-Markovnikov-Regel
Markovnikov und Anti-Markovnikov sind zwei Arten von Additionsreaktionen zwischen HX (HBR, HBR, HI und H2O) und Alkene. Markovnikov -Reaktion tritt auf, wenn die Zugabe von HX zu einem Alken, wobei H -Bindung an weniger substituiertes Kohlenstoffatom der Doppelbindung, während X -Bindung an das andere doppelt gebundene Kohlenstoffatom durch einen ionischen Mechanismus Bindung zu. Die Anti-Markovnikov-Reaktion findet statt, wenn HBR (nicht HCl, HI oder H2O) zu einem Alken hinzuge. Dies ist der Unterschied zwischen Markovnikov und Anti-Markovnikov-Regel.
Laden Sie die PDF von Markovnikov gegen Anti-Markovnikov-Regel herunter
Sie können die PDF -Version dieses Artikels herunterladen und ihn für Offline -Zwecke gemäß Citation Note verwenden. Bitte laden Sie den Unterschied zwischen Markovnikov und Anti Markovnikov die PDF -Version hier herunter
Referenz:
1.Frederick a. Bettelheim, William H. Brown, Mary K. Campbell und Shawn O. Farrell. (2012). Einführung in allgemeine, organische und Biochemie, Cengage Learning Publications.
2.Murthy, c. P. (2008). Universitätschemie (vol. 1). New Age International
3.Bhagi, A und Raj, G. (2010), Krishna's i.A.S. Chemie, Krishna Prakashan Media.
Bild mit freundlicher Genehmigung:
1.'Markovnikovrulepropenehbr' von V8rik (talk) - eigene Arbeit, (CC BY -SA 3.0) über Commons Wikimedia
2.'HBR -Addition'By Eschenmoser - eigene Arbeit (Public Domain) über Commons Wikimedia
3."Anti -Markovnikov -Beispiele" von Mfomich - eigene Arbeit (Public Domain) über Commons Wikimedia


