Unterschied zwischen Methan und Propan
Methan gegen Propan
Methane und Propan sind die ersten und dritten Mitglieder der Alkane -Familie. Ihre molekularen Formeln sind ch4 und C3H8 bzw. Der Schlüsselunterschied zwischen Methan und Propan ist ihre chemische Struktur; Methan enthält nur ein Kohlenstoffatom und vier Wasserstoffatome, während Propan drei Kohlenstoffatome mit acht Wasserstoffatomen enthält. Ihre chemischen und physikalischen Eigenschaften variieren aufgrund dieses Unterschieds.
Was ist Methan?
Methan, auch bekannt als Carbane, Erdgas, Sumpfgas, Kohlenstoff -Tetrahydrid, oder Wasserstoffkarbid, ist das kleinste Mitglied der Alkane -Familie. Seine chemische Formel ist ch4 (Vier Wasserstoffatome sind an ein Kohlenstoffatom gebunden). Es ist ein wichtiger Bestandteil von Erdgas. Methan ist ein farbloses, geruchlosem und geschmackloser Gas. Es kann leicht entzündet werden, da sein Dampf leichter ist als die Luft.
Methan kann natürlich unter dem Boden und unter dem Meeresboden gefunden werden. Das atmosphärische Methan wird als Treibhausgas angesehen. Methan bricht in CH zusammen3- mit Wasser in der Atmosphäre.
Was ist Propan?
Propan ist das dritte Mitglied der Alkane -Familie. Seine molekulare Formel ist c3H6, und die molekulare Masse entspricht 44.10 g · mol–1. Es existiert als Gas bei Standardtemperatur und -druck, kann aber zu einer transportablen Flüssigkeit komprimieren. Propan existiert natürlich nicht, wird jedoch aus dem Erdöl-Raffinerierungsprozess und als Nebenprodukt der Erdgasverarbeitung erhalten.
Propan ist eine farblose, geruchlose, ungiftige und brennbare gasförmige Substanz, und zur Identifizierung von Leckagen wird ein kommerzieller Geruchsgeruch hinzugefügt.
Was ist der Unterschied zwischen Methan und Propan?
Eigenschaften von Methan und Propan
Molekulare Struktur:
Methan: Die molekulare Formel von Methan ist CH4, und es ist ein Beispiel für ein tetraedrisches Molekül mit vier äquivalenten C-H-Bindungen (Sigma-Bindungen). Seine Struktur ist unten angegeben.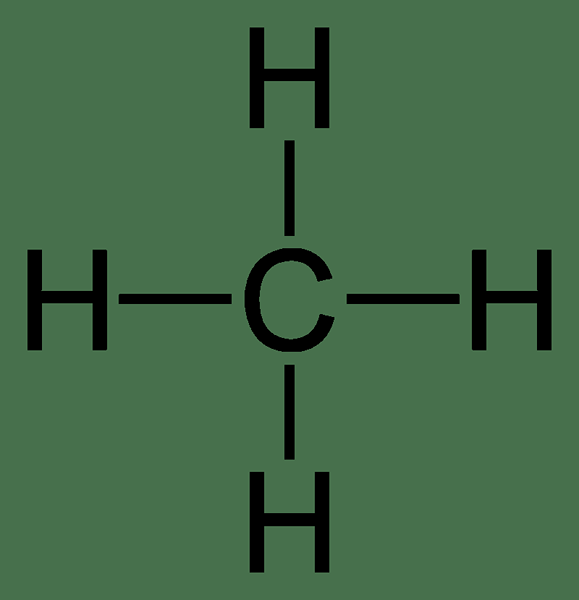
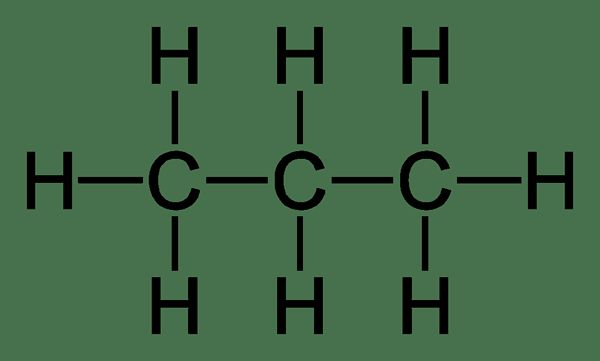
Propan: Die molekulare Formel von Ethan ist c3H8, und seine Struktur ist unten angegeben.
Chemische Eigenschaften:
Verbrennung:
Methan: Methanbrand mit einer hellblauen nicht leuchtenden Flamme, die Kohlendioxid und Wasser in Gegenwart von überschüssiger Luft oder Sauerstoff erzeugt. Es ist eine sehr exotherme Reaktion; Somit ist es ein ausgezeichneter Kraftstoff.
CH4(g) +2o2 → co2 + 2H2O +890 kJ/mol
Es verbrennt teilweise in Kohlenmonoxid (CO) -gas in Gegenwart von unzureichender Luft oder Sauerstoff.
2ch4(g) +3o2 → 2co +2h2O +Energie
Propan: Propan brennt auch auf ähnliche Weise wie die anderen Alkane. Es brennt in Gegenwart von überschüssigem Sauerstoff, der Wasser und Kohlendioxid produziert.
C3H8 + 5o2 → 3co2 + 4H2O +2220 kJ/mol
In Abwesenheit eines ausreichenden Sauerstoffs für den Verbrennungsprozess verbrennt es unvollständig in Kohlenmonoxid und/oder Rußkohlenstoff.
2 c3H8 + 9o2 → 4co2 + 2co +8h2O +Wärme
ODER
C3H8 + 9o2 → 3c + 4H2O +Wärme
Die Propanverbrennung ist viel sauberer als die Verbrennung von Benzin, aber nicht so sauber wie der von Erdgas.
Reaktionen:
Methan: Methan zeigt Substitutionsreaktionen mit Halogenen. Bei diesen Reaktionen werden ein oder mehrere Wasserstoffatome durch eine gleiche Anzahl von Halogenatomen ersetzt und genannt “Halogenierung.Es reagiert mit Chlor (CL) und Brom (BR) in Gegenwart von Sonnenlicht.
Wenn eine Mischung aus Methan und Dampf durch ein erhitztes (1000 K) Nickel geleitet wird, das auf der Aluminiumoxidoberfläche getragen wird, kann es Wasserstoff erzeugen.
Propan: Propan zeigt auch Halogenierungsreaktionen unter besonderen Bedingungen, die in verschiedenen Anteilen unterschiedliche Produkte erzeugen.
CH3-CH2-CH3 + Cl2 → CH3-CH2-CH2Cl (45%) + CH3-CHCL-CH3 (55%)
CH3-CH2-CH3 + Br2 → CH3-CH2-CH2Br (3%) + CH3-CHBR-CH3 (97%)
Verwendung von Methan und Propan
Methan: Methan wird in vielen industriellen chemischen Prozessen (als Kraftstoff, Erdgas, verflüssigtes Erdgas) verwendet und als gekühlte Flüssigkeit transportiert.
Propan: Propan wird im Allgemeinen als Kraftstoff in Motoren, Öfen, tragbaren Öfen, Oxy-Gas-Fackeln, Warmwasserbereiter, Wäschetrocknern und zum Erhitzen in Häusern verwendet. Es ist eines der verflüssigen Erdölgase wie Butan, Propylen und Butylen.
Definitionen:
Exotherme Reaktion: Eine exotherme Reaktion ist eine chemische Reaktion, die Energie durch Licht oder Wärme fördert.
Substitutionsreaktionen: Die Substitutionsreaktion ist eine chemische Reaktion, die die Verschiebung einer funktionellen Gruppe in einer chemischen Verbindung beinhaltet und durch eine andere funktionelle Gruppe ersetzt wird.
Referenzen: „Reaktion von Propan mit Sauerstoff!”Thecolt84„ Reaktionen von Alkenen “Michigan State University Bild mit freundlicher Genehmigung:„ Propan “von Holger87 - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia „Methan“ (öffentlich zugänglich) über Commons Wikimedia

