Unterschied zwischen Orbitaldiagramm und Elektronenkonfiguration
Der Schlüsselunterschied Zwischen Orbital -Diagramm und Elektronenkonfiguration ist das Das Orbital -Diagramm zeigt die Elektronen in Pfeilen und zeigt den Spin von Elektronen an. Die Elektronenkonfiguration zeigt jedoch keine Details zum Spin von Elektronen an.
Das Orbital -Diagramm zeigt die Anordnung der Elektronen, die durch die Elektronenkonfiguration angegeben sind. Die Elektronenkonfiguration enthält die Details zur Verteilung der Elektronen in den Orbitalen des Atoms. Aber das Orbitaldiagramm zeigt auch den Dreh der Elektronen. Dies ist der grundlegende Unterschied zwischen Orbital -Diagramm und Elektronenkonfiguration.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Orbital -Diagramm
3. Was ist die Elektronenkonfiguration
4. Seite für Seitenvergleich - Orbital -Diagramm gegen Elektronenkonfiguration in tabellarischer Form
6. Zusammenfassung
Was ist Orbital -Diagramm?
Das Orbital -Diagramm ist eine Art von Diagramm, die die Verteilung der Elektronen in den Orbitalen eines Atoms zeigt und den Spin dieser Elektronen anzeigt. Es ist eine Art Notation, die zeigt, welche Orbitale gefüllt sind und welche teilweise gefüllt sind. Hier verwenden wir Pfeile, um Elektronen darzustellen. Die Richtung der Pfeilspitze (nach oben oder unten) zeigt den Dreh des Elektrons an.
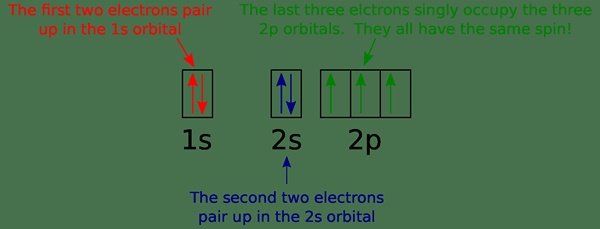
Abbildung 01: Orbitaldiagramm für Stickstoff
Ein Orbital kann maximal zwei Elektronen haben. Gemäß dem Pauli -Ausschlussprinzip können zwei Elektronen im selben Atom nicht die gleiche Quantennummer -Menge haben. Dies bedeutet, dass die Spin -Quantenzahl unterschiedlich ist, auch wenn alle anderen Quantenzahlen gleich sind, ist die Spinquantenzahl unterschiedlich. Die beiden Elektronen im selben Orbital haben entgegengesetzte Spin. Das obige Bild zeigt ein Beispiel für ein Orbitaldiagramm.
Was ist die Elektronenkonfiguration?
Die Elektronenkonfiguration ist eine Möglichkeit, die Elektronen eines Atoms zu arrangieren, indem die Verteilung dieser Elektronen in den Orbitalen angezeigt wird. Zuvor wurde die Elektronenkonfiguration unter Verwendung des Bohr -Modells des Atoms entwickelt. Dies ist für kleine Atome mit weniger Elektronen genau, aber wenn wir große Atome mit einer großen Anzahl von Elektronen berücksichtigen, müssen wir die Quantentheorie zur Bestimmung der Elektronenverteilung verwenden.
Gemäß der Quantenmechanik ist eine Elektronenschale der Zustand mehrerer Elektronen, die dieselbe Hauptquantennummer teilen, und wir nennen die Schale mit der für den Energieniveau angegebenen Nummer und der Art des Umlaufbahn, das wir in Betracht ziehen, e.G., 2s bezieht sich auf das S -Orbital der Elektronenschale der 2. Energieniveau. Darüber hinaus gibt es ein Muster, das die maximale Anzahl von Elektronen beschreibt, die eine Elektronenschale enthalten kann. Hier hängt diese maximale Zahl von der azimutalen Quantenzahl ab, l. Weiter beziehen sich die Werte L = 0, 1, 2 und 3 auf die Orbitale der S-, P, D und F. Die maximale Anzahl von Elektronen, die eine Schale enthalten kann = 2 (2L+1). Daher können wir die folgende Tabelle entwickeln;
| Orbital | Maximale Anzahl der Elektronen 2 (2L+1) |
| L = 0 ist s Orbital | 2 |
| L = 1 ist p Orbital | 6 |
| L = 2 ist D Orbital | 10 |
| L = 3 ist f Orbital | 14 |

Bei der Betrachtung der Notation der Elektronenkonfiguration müssen wir die Abfolge der Quantenzahlen verwenden. Beispielsweise beträgt die Elektronenkonfiguration für das Wasserstoffatom 1s1. Hier besagt diese Notation, dass Wasserstoffatome ein Elektron im S -Orbital der ersten Elektronenschale haben. Für Phosphor beträgt die Elektronenkonfiguration 1s22s22p63s23p3. Das bedeutet; Das Phosphoratom hat 3 Elektronenschalen mit 15 Elektronen gefüllt.
Was ist der Unterschied zwischen Orbital -Diagramm und Elektronenkonfiguration?
Das Orbital -Diagramm zeigt die Anordnung der Elektronen, die durch die Elektronenkonfiguration angegeben sind. Der Hauptunterschied zwischen Orbitaldiagramm und Elektronenkonfiguration besteht darin, dass das Orbital -Diagramm die Elektronen in Pfeilen zeigt, die den Spin von Elektronen anzeigen. In der Zwischenzeit zeigt die Elektronenkonfiguration keine Details zum Spin von Elektronen an. Darüber hinaus verwenden Orbital -Diagramme im Notationsmuster Pfeile, um Elektronen darzustellen, während die Elektronenkonfiguration Elektronen mit Zahlen anzeigt.
Nachfolgend finden Sie eine Zusammenfassung der Differenz zwischen Orbital -Diagramm und Elektronenkonfiguration.
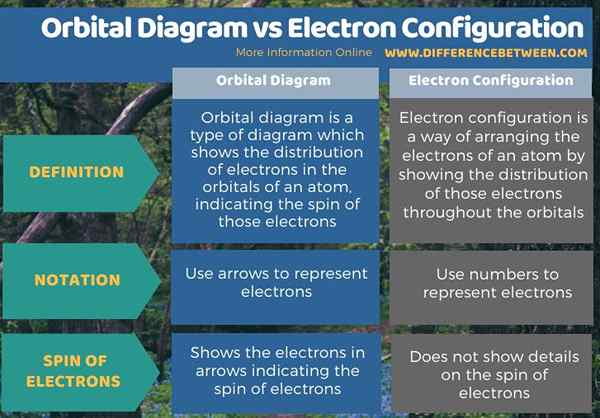
Zusammenfassung -Orbital -Diagramm gegen Elektronenkonfiguration
Der Hauptunterschied zwischen Orbitaldiagramm und Elektronenkonfiguration besteht darin, dass das Orbitaldiagramm die Elektronen in Pfeilen zeigt, die den Spin von Elektronen angeben, während die Elektronenkonfiguration keine Details zum Spin von Elektronen zeigt.
Referenz:
1. “1.4: Elektronenkonfiguration und Orbitaldiagramme.Chemie -Libretexten, Libretexten, 26. September. 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
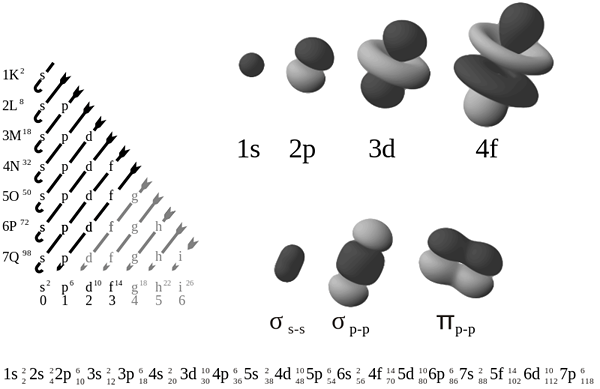
1. "Orbital Diagramm Stickstoff" von CK -12 Foundation (Raster), Adrignola (Vektor) - Datei: High School Chemistry.PDF, Seite 327 (Public Domain) über Commons Wikimedia
2. "Elektronenorbitale" von Patricia.FIDI - eigene Arbeit von Patricia.Fidi und Lt Paul - Ursprünglich aus PL: Grafika: Orbitale.PNG, Autor PL: Wikipedysta: Chemmix.Dieses W3C-nicht genannte Vektorbild wurde mit Inkscape (Public Domain) über Commons Wikimedia erstellt


