Unterschied zwischen Oxid und Dioxid
Der Schlüsselunterschied Zwischen Oxid und Dioxid ist das Oxid ist eine Verbindung mit einer oder mehreren Sauerstoffatomen, die mit einem anderen chemischen Element kombiniert werden, während Dioxid ein Oxid ist, das zwei Sauerstoffatome in seinem Molekül enthält.
Der Begriff Oxid ist ein allgemeiner Begriff, der das Vorhandensein von Sauerstoffatomen in einer Verbindung beschreibt. Hier existiert das Sauerstoffatom (en) in Kombination mit einem anderen chemischen Element; Meistens Metalle und Nichtmetalle. Nach der Anzahl der Sauerstoffatome in der Verbindung können wir sie als Monoxid, Dioxid, Trioxid usw. nennen, usw. Daher ist Dioxid ein Oxid, das zwei Sauerstoffatome pro Molekül enthält.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Oxid
3. Was ist Dioxid
4. Seite für Seitenvergleich -Oxid gegen Dioxid in tabellarischer Form
5. Zusammenfassung
Was ist Oxid?
Oxid ist eine Verbindung mit einer oder mehreren Sauerstoffatomen, die mit einem anderen chemischen Element kombiniert werden. Das „Oxid“ hier ist das zweiwertige Anion (o2-). Typischerweise enthalten Metalloxide dieses Dianion, in dem sich das Sauerstoffatom im Oxidationszustand von -2 befindet. Mit Ausnahme von leichten Inertgasen (einschließlich Helium, Neon, Argon und Krypton) kann Sauerstoff mit allen anderen Elementen Oxide bilden.
Bei der Bildung eines Oxids können Metalle und Nichtmetalle ihre niedrigsten und höchsten Oxidationszustände zeigen. Einige Oxide sind ionische Verbindungen; Alkali -Metalle, Alkali -Erdmetalle und Übergangsmetalle bilden diese ionischen Oxide. Andere Verbindungen haben eine kovalente Natur; Metalle mit hohen Oxidationszuständen können kovalente Oxide bilden. Darüber hinaus bilden Nichtmetalle kovalente Oxidverbindungen.
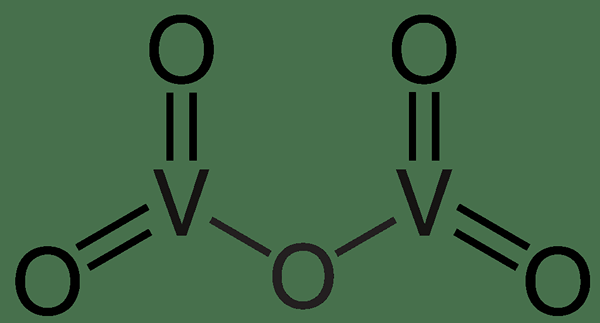
Abbildung 01: Vanadium (v) Oxid
Im obigen Bild hat das Vanadium -Metallatom eine Valenz von 5 (Gesamtvalenz für zwei Vanadiumatome). Daher ist fünf Sauerstoffatome (mit einer Valenz von 2 pro Sauerstoffatom), die an sie gebunden sind.
Darüber hinaus reagieren einige organische Verbindungen auch mit Sauerstoff (oder Oxidationsmitteln), um Oxide zu produzieren, e.G. Aminoxide, Phosphinoxide, Sulfoxide usw. Darüber hinaus bestimmt die Anzahl der Sauerstoffatome in der Verbindung, ob es sich um ein Monoxid, ein Dioxid oder ein Trioxid handelt.
Nach ihren Eigenschaften ist es auch möglich, sie als saure, grundlegende, neutrale und amphotere Oxide zu kategorisieren. Saures Oxid kann mit Basen reagieren und Salze bilden. Ex: Schwefeltrioxid (SO3). Basisoxide reagieren mit Säuren und bilden Salze. Ex: Natriumoxid (Na2o). Neutral zeigt weder saure noch grundlegende Eigenschaften; So bilden sie keine Salze, wenn sie mit Säuren oder Basen reagieren. Beispiel: Kohlenmonoxid (CO). Amphoterische Oxide haben sowohl saure als auch grundlegende Eigenschaften; Daher reagieren sie sowohl mit Säuren als auch mit Basen, um Salze zu bilden. Ex: Zinkoxid (ZnO).
Was ist Dioxid?
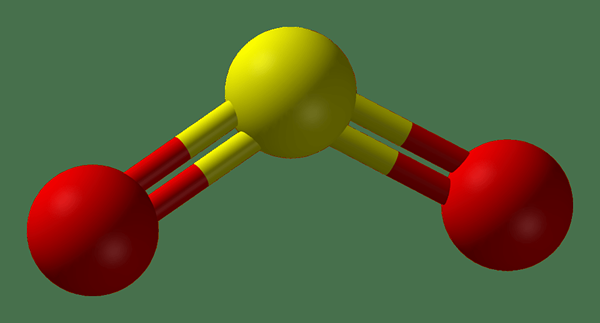
Dioxid ist ein Oxid, das zwei Sauerstoffatome in seinem Molekül enthält. Ein Molekül sollte ein chemisches Element mit einer Valenz von 4 enthalten, um ein Dioxid zu bilden. Es liegt daran, dass ein Sauerstoffatom eine Valenz von 2 zeigt. Zum Beispiel beträgt bei Kohlendioxid die Valenz von Kohlenstoff 4.

Abbildung 02: Kugel- und Stickstruktur des Schwefeldioxids
Einige Beispiele für Dioxide
- Kohlendioxid (CO2)
- Stickstoffdioxid (Nein2)
- Sauerstoff (o2)
- Quarz oder Siliziumdioxid (SiO2)
Was ist der Unterschied zwischen Oxid und Dioxid?
Dioxid ist eine Art Oxid. Der Schlüsselunterschied zwischen Oxid und Dioxid besteht darin, dass Oxid jede Verbindung mit einem oder mehreren Sauerstoffatomen ist, die mit einem anderen chemischen Element kombiniert werden, während Dioxid ein Oxid ist, das zwei Sauerstoffatome in seinem Molekül enthält. Bei der Betrachtung der Valenz von Oxiden beträgt die Valenz von Sauerstoff 2 und die Valenz anderer Elemente kann variieren; Für Dioxide beträgt die Valenz von Sauerstoff jedoch 2 und die Valenz eines anderen Elements im Wesentlichen 4. Wir können dies auch als einen Unterschied zwischen Oxid und Dioxid betrachten.

Zusammenfassung -Oxid gegen Dioxid
Oxid ist ein allgemeiner Begriff, den wir verwenden, um jede Verbindung mit Sauerstoffatomen in Kombination mit einem anderen Element zu benennen. Darüber hinaus können wir nach der Anzahl der Sauerstoffatome sie als Monoxid, Dioxid, Trioxid usw. nennen, usw. Der Schlüsselunterschied zwischen Oxid und Dioxid besteht darin, dass Oxid jede Verbindung mit einem oder mehreren Sauerstoffatomen ist, die mit einem anderen chemischen Element kombiniert werden, während Dioxid ein Oxid ist, das zwei Sauerstoffatome in seinem Molekül enthält.
Referenz:
1."Oxid.” Wikipedia, Wikimedia Foundation, 2. Juni 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Vanadium (v) Oxid" von Kemikungen - eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Schwefel-Dioxid-3D-Balls" von Ben Mills-eigene Arbeit (Public Domain) über Commons Wikimedia