Unterschied zwischen Phenyl und Benzyl

Phenyl gegen Benzyl
Sowohl Phenyl als auch Benzyl werden von Benzol abgeleitet und von Studenten der Chemie häufig verwirrt. Phenyl ist ein Kohlenwasserstoffmolekül mit der Formel C6H5, Während Benzyl C ist6H5CH2; ein zusätzliches ch2 Gruppe am Benzolring befestigt.
Phenyl
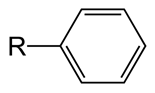
Phenyl ist ein Kohlenwasserstoffmolekül mit der Formel C6H5. Dies wird daher von Benzol abgeleitet, weshalb ähnliche Eigenschaften wie Benzol aufweist. Dies unterscheidet sich jedoch von Benzol aufgrund des Mangels eines Wasserstoffatoms in einem Kohlenstoff. Das Molekulargewicht von Phenyl beträgt also 77 g mol-1. Phenyl wird als pH -Wert abgekürzt. Normalerweise wird Phenyl an eine andere Phenylgruppe, Atom oder ein anderes Molekül gebunden (dieser Teil wird als Substituent -R -Gruppe wie in der Abbildung bezeichnet). Die Kohlenstoffatome von Phenyl werden sp2 wie in Benzol hybridisiert. Alle Kohlenstoffe können drei Sigma -Bindungen bilden. Zwei der Sigma -Bindungen werden mit zwei benachbarten Kohlenstoffen gebildet, so dass es zu einer Ringstruktur führt. Die andere Sigma -Bindung wird mit einem Wasserstoffatom gebildet. In einem Kohlenstoff wird jedoch im Ring die dritte Sigma -Bindung eher mit einem anderen Atom oder Molekül als mit einem Wasserstoffatom gebildet. Die Elektronen in P -Orbitalen überlappen sich miteinander, um die delokalisierte Elektronenwolke zu bilden. Daher hat Phenyl ähnliche C-C-Bindungslängen zwischen allen Kohlenstoffen, unabhängig davon, ob es sich um wechselnde Einzel- und Doppelbindungen handelt. Diese C-C-Bindungslänge beträgt ungefähr 1.4 Å. Der Ring ist planar und hat einen Winkel von 120 ° zwischen Bindungen um einen Kohlenstoff. Aufgrund der Substituentengruppe von Phenyl, der Polarität und anderen chemischen oder physikalischen Eigenschaften ändern sich. Wenn der Substituent Elektronen an die delokalisierte Elektronenwolke des Rings spendet, werden diese als Elektronenspendegruppen bezeichnet (e.G. -Och3, NH2). Wenn der Substituent Elektronen aus der Elektronenwolke anzieht, ist es als Elektronenentzugs Substituent bekannt. (E.G. -NEIN2, -Cooh). Phenylgruppen sind aufgrund ihrer Aromatizität stabil, sodass sie nicht leicht Oxidationen oder Reduktionen unterzogen werden. Darüber hinaus sind sie hydrophob und unpolar.
Benzyl
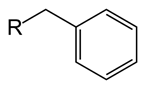
Die Formel von Benzyl ist c6H5CH2. Dies ist auch ein Derivat von Benzol. Im Vergleich zu Phenyl hat Benzyl ein CH2 Gruppe am Benzolring befestigt. Ein weiterer molekularer Teil (R -Gruppe, wie im Bild dargestellt) kann an der Benzylgruppe durch Bindung an die CH angeschlossen werden2 Kohlenstoffatom. Die Benzylgruppe wird als „BN“ abgekürzt. Das Molekulargewicht der Benzylgruppe beträgt 91 g mol-1. Da es einen Benzolring gibt, ist die Benzylgruppe aromatisch. In organischen Chemie -Mechanismen kann die Benzylgruppe entweder als radikaler Carbokation (C) gebildet werden6H5CH2+) oder ein Carbanion (c6H5CH2-). Beispiel. Es gibt eine höhere Stabilisierung dieser Zwischenprodukte im Vergleich zum Alkylradikal oder Kation. Die Reaktivität der benzylischen Position ist ähnlich der der Allylposition. Benzylgruppen werden häufig in der organischen Chemie als Schutzgruppen verwendet, insbesondere zum Schutz von Carboxylsäure- oder Alkoholfunktionsgruppen.
Was ist der Unterschied zwischen Phenyl und Benzyl?
• Molekulare Formel von Phenyl ist c6H5 Während in Benzyl es c ist, ist es C6H5CH2.
• Benzyl hat zusätzliche CH2 Gruppe im Vergleich zu Phenyl.
• In Phenyl ist der Benzolring direkt an einem Substituentenmolekül oder einem Atom befestigt, aber in Benzyl, das CH2 Gruppe stellt die Verbindung mit einem anderen Molekül oder einem Atom her.

