Unterschied zwischen primärer und sekundärer Valenz
Der Schlüsselunterschied Zwischen primärer und sekundärer Valenz ist das Primärvalenz ist der Oxidationszustand des zentralen Metallatoms eines Koordinierungskomplexes.
Die Begriffe Primär- und Sekundärvalenz fallen in die Koordinationschemie. Die Valenz ist die Kombination eines Elements, insbesondere gemessen an der Anzahl der Wasserstoffatome, die es verdrängen oder sich miteinander verbinden kann.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist die primäre Wertigkeit
3. Was ist Sekundärvalenz
4. Seite für Seitenvergleich - Primär -VS -sekundäre Valenz in tabellarischer Form
5. Zusammenfassung
Was ist die primäre Wertigkeit?
Primärvalenz ist der Oxidationszustand des zentralen Metallatoms eines Koordinationskomplexes. Ein Koordinierungskomplex ist eine komplizierte Verbindung, die ein Metallion in der Mitte hat, das von mehreren Atomen oder Atomengruppen umgeben ist. Diese umgebenden chemischen Arten werden Liganden bezeichnet. Das zentrale Metallatom bindet abhängig von der Elektronenkonfiguration dieses Atoms eine bestimmte Anzahl von Liganden. Die Anzahl der Liganden, die an das zentrale Metallatom bindet, wird als Koordinationsnummer bezeichnet.
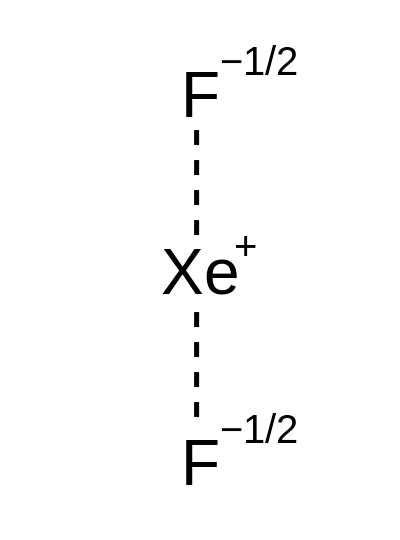
Außerdem hat das zentrale Metallatom seinen eigenen Oxidationszustand. Wir können den Oxidationszustand unter Verwendung der chemischen Formel des Komplexes berechnen. Wenn wir die elektrische Nettoladung des Komplexes, die Ladungen und die Anzahl der an das Metallatom befestigten Liganden kennen, können wir den Oxidationszustand leicht berechnen. Mit anderen Worten, die primäre Valenz ist die Anzahl der Liganden, die wir benötigen, um die Ladung auf dem Metallion zu erfüllen.
Was ist Sekundärvalenz
Sekundärvalenz ist die Koordinationsnummer des zentralen Metallatoms eines Koordinierungskomplexes. Die Koordinationsnummer ist die Anzahl der Liganden, die am zentralen Metallatom angebracht sind. Betrachten wir ein Beispiel, um sowohl primäre als auch sekundäre Valences zu verstehen. Im Koordinierungskomplex k4[Fe (CN)6] Das zentrale Metallatom ist Eisen (Fe).

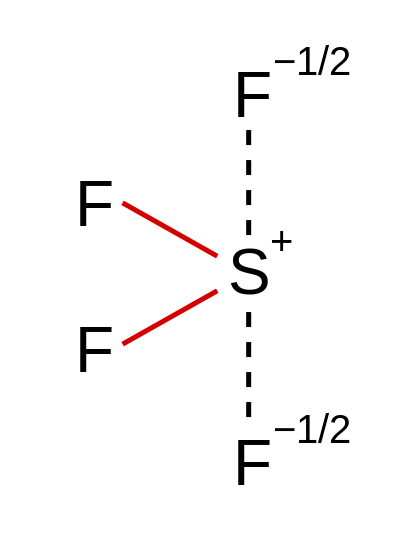
Abbildung 02: Die Koordinationszahl von Schwefel in dieser Koordinationsverbindung beträgt vier
Wir können die primäre Wertigkeit wie unten berechnen:
- Die Ladung des Kaliumliganden beträgt immer +1.
- Die Ladung des Cyanidliganden (CN) beträgt immer -1.
- Es gibt vier Kaliumliganden, die +4 Ladung entsprechen.
- Es gibt sechs Cyanid (CN) -Liganden, die -6 -Ladung reichen.
- Dann können wir den Oxidationszustand von Fe wie folgt berechnen:
Die Gesamtladung des Komplexes = 0
0 = [(Ladung des Kaliumliganden) x 4] + [Ladung des FE -Ions] + [(Ladung des Cyanidliganden) x 6]
0 = [(+1) x 4] + [Ladung des Fe Ion] + [(-1) x 6]
0 = 4 + [Ladung des Fe Ion] - 6
Ladung des FE Ion = +2
Oxidationszustand von Fe = +2
Was ist der Unterschied zwischen primärer und sekundärer Valenz?
Die Begriffe Primär- und Sekundärvalenz fallen unter den Bereich der Koordinationschemie. Hier besteht der Hauptunterschied zwischen primärer und sekundärer Valenz darin, dass die primäre Valenz der Oxidationszustand des zentralen Metallatoms eines Koordinationskomplexes ist. Die sekundäre Valenz ist jedoch die Koordinationszahl des zentralen Metallatoms eines Koordinationskomplexes. Darüber hinaus ist die primäre Valenz die Anzahl der Liganden, die wir die Ladung des Metallions erfüllen müssen, während die sekundäre Valenz die Anzahl der Liganden ist, die am zentralen Metallatom befestigt sind.
Die folgende Infografik fasst den Unterschied zwischen primärer und sekundärer Valenz zusammen.
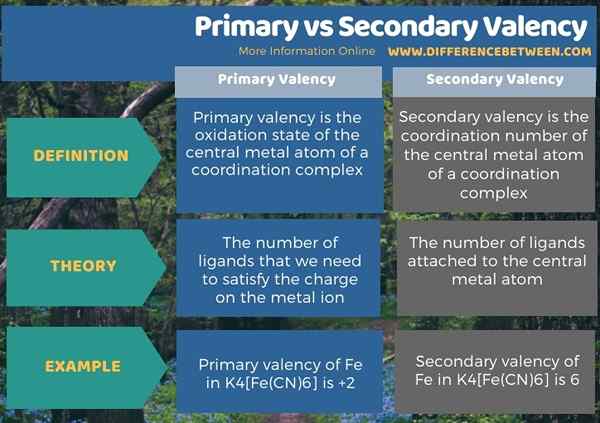
Zusammenfassung -Primär -VS -Sekundärvalenz
Die Begriffe Primär- und Sekundärvalenz fallen in die Koordinationschemie. Der Hauptunterschied zwischen primärer und sekundärer Valenz besteht darin, dass die primäre Valenz der Oxidationszustand des zentralen Metallatoms eines Koordinationskomplexes ist. Während die sekundäre Valenz die Koordinationszahl des zentralen Metallatoms eines Koordinierungskomplexes ist.
Referenz:
1. "Übergangsmetalle.Koordinationskomplexe und Liganden, hier erhältlich.
2. „Orbital Hybridisierung.Wikipedia, Wikimedia Foundation, 14. November. 2019, hier erhältlich.
3. „Grenzlose Chemie.”Lumen, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Di Xeno" von Officer781 - eigene Arbeit (öffentlich zugänglich) über Commons Wikimedia
2. "Tetra Sulf" von Officer781 - eigene Arbeit (Public Domain) über Commons Wikimedia


