Unterschied zwischen Schottky -Defekt und Frenkelfehler
Der Schlüsselunterschied Zwischen Schottky -Defekt und Frenkelfehler ist das Schottky -Defekt reduziert die Dichte eines Kristalls, während der Frenkelfehler die Dichte eines Kristalls nicht beeinflusst. Abgesehen von dem oben genannten Schlüsselunterschied besteht ein weiterer wichtiger Unterschied zwischen Schottky -Defekt und Frenkelfehler darin, dass der Schottky -Defekt eine Verringerung der Masse des Kristalls verursacht, während der Frenkelfehler die Masse des Kristalls nicht beeinflusst.
Der Begriff Kristallgitter beschreibt die symmetrische Anordnung der Atome eines Kristalls. Der Schottky -Defekt und der Frenkelfehler sind zwei Formen von Punktfehlern, die in einem Kristallgitter auftreten. Ein Punktfehler ist ein leerer Punkt, der aufgrund des Verlustes eines Atoms aus dem Kristallgitter erzeugt wird. Diese Defekte verursachen Unregelmäßigkeiten von Kristallgitter.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Schottky -Defekt?
3. Was ist Frenkelfehler
4. Seite an Seitenvergleich - Schottky Defekt gegen Frenkel -Defekt in tabellarischer Form
5. Zusammenfassung
Was ist Schottky -Defekt??
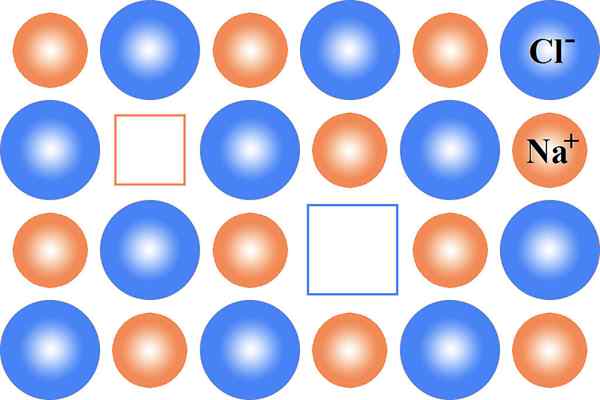
Schottky -Defekt ist eine Form des Punktfehlers, die sich aufgrund des Verlustes eines Atoms in stöchiometrischen Einheiten des Kristallgitters bildet. Dieser Punktfehler bekam seinen Namen, nachdem der Wissenschaftler Walter H. Schottky. Wir können diesen Defekt entweder in ionischen oder nichtionischen Kristallen beobachten. Dieser Defekt entsteht, wenn ein Baustein das Kristallgitter verlässt.

Abbildung 01: Schottky -Defekt in NaCl
Obwohl das Gitter ein Atom verliert, wirkt es sich nicht auf das Ladungsbetrag des Gitters aus, da die Atome eine stöchiometrische Einheit des Gitters hinterlassen. Eine stöchiometrische Einheit enthält entgegengesetzt geladene Atome in gleichen Verhältnissen.
Wenn dieser Defekt auftritt, reduziert er die Dichte des Kristallgitters. Diese Form von Punktdefekten ist in ionischen Verbindungen häufig. Wenn es in nichtionischen Kristallen auftritt, nennen wir es einen Leerstandsfehler. In den meisten Fällen tritt dieser Defekt in Kristallgitter mit Atomen mit fast gleichen Größen auf. Ex: NaCl -Gitter, KBR -Gitter usw.
Was ist Frenkelfehler?
Frenkelfehler ist eine Form des Punktfehlers, bei dem der Defekt aufgrund des Verlusts eines Atoms oder eines kleinen Ions aus dem Kristallgitter auftritt. Dieser Verlust schafft einen freien Punkt im Gitter. Synonyme für diesen Defekt sind Frenkelstörungen und Frenkelpaare. Der Defekt bekam seinen Namen, nachdem der Wissenschaftler Yakov Frenkel.
Wenn ein kleines Ion das Kristallgitter verlässt, handelt es sich um ein Kation (ein positiv geladenes Ion). Dieses Ion nimmt einen Ort in der Nähe des freien Punktes ein. Daher wirkt sich dieser Defekt nicht auf die Dichte des Kristallgitters aus. Das liegt daran, dass das Atom oder die Ionen das Gitter nicht vollständig verlassen. Diese Form von Punktfehlern ist in ionischen Gitter üblich. Im Gegensatz zu Schottky -Defekt tritt dieser Defekt in Gitter mit Atomen oder Ionen auf, die unterschiedliche Größen haben.
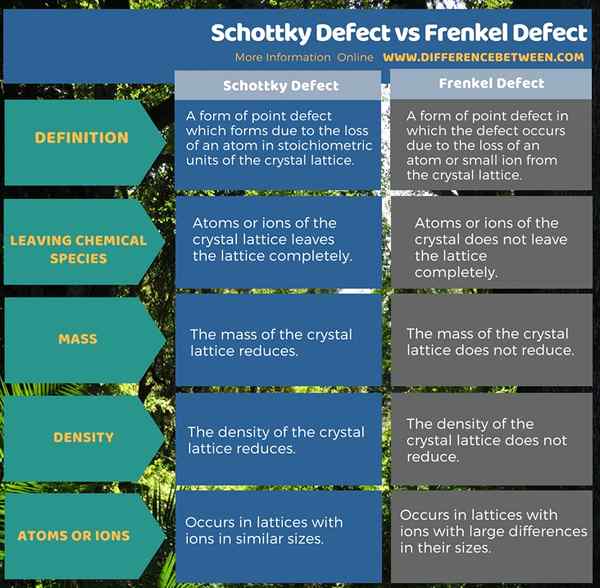
Was ist der Unterschied zwischen Schottky -Defekt und Frenkelfehler?
Schottky -Defekt ist eine Form des Punktfehlers, die sich aufgrund des Verlustes eines Atoms in stöchiometrischen Einheiten des Kristallgitters bildet. Frenkelfehler ist eine Form des Punktfehlers, bei dem der Defekt aufgrund des Verlusts eines Atoms oder eines kleinen Ions aus dem Kristallgitter auftritt. Der Schottky -Defekt reduziert die Dichte des Kristallgitters, während der Frenkelfehler die Dichte des Kristallgitters nicht beeinflusst.
Zusammenfassung -Schottky -Defekt gegen Frenkelfehler
Punktdefekte sind Defekte in Kristallgitter, die aufgrund des Verlusts von Atomen oder Ionen aus dem Gitter auftreten und somit einen freien Punkt bilden. Schottky -Defekt und Frenkelfehler sind zwei Formen von Punktfehlern. Der Unterschied zwischen Schottky -Defekt und Frenkelfehler besteht darin, dass Schottky -Defekt die Dichte eines Kristalls verringert, während der Frenkelfehler die Dichte eines Kristalls nicht beeinflusst.
Referenz:
1. „Schottky Defekt.Wikipedia, Wikimedia Foundation, 12. Mai 2018. Hier verfügbar
2. „Kristallfehler - Punktdefekte.Leiter und Isolatoren. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.'NaCl - Schottky Defekt'by Vladvd - eigene Arbeit, (CC BY -SA 3.0) über Commons Wikimedia


