Was ist der Unterschied zwischen adiabatischer und reversibler adiabatischer Prozess
Der Schlüsselunterschied zwischen adiabatischer und reversibler adiabatischer Prozess ist, dass das adiabatische System in adiabatischen Prozessen isoliert ist und keine Wärmeübertragungen zulässt, während ein reversibler adiabatischer Prozess Wärmeübertragung beinhaltet.
Adiabatische Prozesse sind thermodynamische Prozesse, bei denen keine Nettowärmeübertragung aufgrund von Reaktionsbedingungen auftritt. Reversibler adiabatischer Prozess beinhaltet auch keine Wärmeübertragung. Hier ist die übertragene Wärme direkt proportional zur Entropieänderung des Systems, und die Entropieänderung ist Null, was wiederum die Wärmeübertragung Null macht.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist adiabatischer Prozess
3. Was ist reversibler adiabatischer Prozess (isentropischer Prozess)
4. Adiabatischer vs reversibler adiabatischer Prozess in tabellarischer Form
5. Zusammenfassung -adiabatischer VS reversibler adiabatischer Prozess
Was ist adiabatischer Prozess?
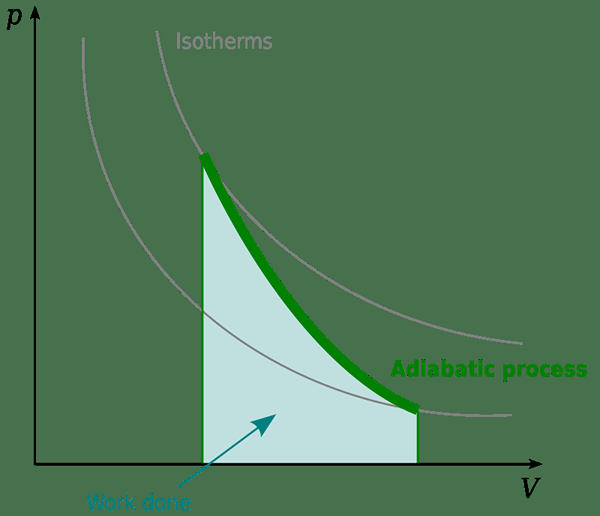
Der adiabatische Prozess kann als eine Änderung eines Systems definiert werden, bei dem keine Wärme in oder aus dem System übertragen wird. Hauptsächlich wird die Wärmeübertragung auf zwei Arten gestoppt. Eine Methode besteht darin, eine thermisch isolierte Grenze zu verwenden, damit keine Wärme eingeben oder beenden. Zum Beispiel ist eine Reaktion, die in einem Dewar -Kolben auftritt. Eine andere Methode Ein adiabatischer Prozess kann stattfinden, wenn ein Prozess sehr schnell stattfindet. Daher bleibt keine Zeit mehr, die Wärme ein- und auszusteigen.

In der Thermodynamik zeigen wir die adiabatischen Änderungen durch DQ = 0. In diesen Fällen besteht eine Beziehung zwischen Druck und Temperatur. Daher unterliegt das System aufgrund des Drucks unter adiabatischen Bedingungen Veränderungen. Dies geschieht bei der Bildung von Wolken und in groß angelegten Konvektionsströmen. In höheren Höhen gibt es einen geringeren atmosphärischen Druck. Wenn sich die Luft erwärmt, neigt es dazu, nach oben zu gehen. Da der Luftdruck von außen niedrig ist, wird das steigende Luftpaket versuchen, sich zu erweitern. Bei der Erweiterung funktionieren die Luftmoleküle und dies wirkt sich auf ihre Temperatur aus. Aus diesem Grund reduziert sich die Temperatur beim Aufstieg.
Nach der Thermodynamik bleibt die Energie im Paket konstant, kann jedoch um die Expansionsarbeit umgewandt oder seine Temperatur aufrechterhalten werden. Es gibt keinen Wärmeaustausch mit außen. Das gleiche Phänomen gilt auch für die Luftkompression (e.G., ein Kolben). In dieser Situation steigt die Temperatur, wenn das Luftpaket komprimiert wird. Diese Prozesse werden als adiabatische Erwärmung und Kühlung bezeichnet.
Was ist reversibler adiabatischer Prozess (isentropischer Prozess)?
Ein reversibler adiabatischer Prozess wird auch als isentropischer Prozess bezeichnet. Spontane Prozesse erhöhen die Entropie des Universums. In diesem Fall kann entweder die Systementropie oder die umgebende Entropie zunehmen. Ein isentropischer Prozess tritt auf, wenn die Systementropie konstant bleibt. Ein reversibler adiabatischer Prozess ist ein Beispiel für einen isentropischen Prozess. Darüber hinaus sind die konstanten Parameter in einem isentropischen Prozess Entropie, Gleichgewicht und Wärmeenergie.
Diese Arten von Prozessen sind idealisierte thermodynamische Prozesse, die adiabatisch sind, aber die Wärmeübertragung ist reibungslos, was bedeutet.
Was ist der Unterschied zwischen adiabatischer und reversibler adiabatischer Prozess?
Der adiabatische Prozess kann als eine Änderung eines Systems definiert werden, bei dem keine Wärme in oder aus dem System übertragen wird. Ein reversibler adiabatischer Prozess wird auch als isentropischer Prozess bezeichnet. Der Schlüsselunterschied zwischen adiabatischer und reversibler adiabatischer Prozess besteht darin, dass das adiabatische System in adiabatischen Prozessen isoliert ist und keine Wärmeübertragungen zulässt, während der reversible adiabatische Prozess Wärmeübertragung beinhaltet vom System.
Die folgende Infografik zeigt die Unterschiede zwischen adiabatischer und reversibler adiabatischer Prozess in tabellarischer Form für Seite für Seitenvergleich.
Zusammenfassung -adiabatischer VS reversibler adiabatischer Prozess
Adiabatische Prozesse sind thermodynamische Prozesse, bei denen aufgrund der Reaktionsbedingungen keine Nettowärmeübertragung auftritt. Der Schlüsselunterschied zwischen adiabatischer und reversibler adiabatischer Prozess besteht darin, dass das adiabatische System in adiabatischen Prozessen isoliert ist und keine Wärmeübertragungen zulässt, während reversibler adiabatischer Prozess Wärmeübertragung beinhaltet das System.
Referenz:
1. “Adiabatischer Prozess - Definition, Gleichung, reversibler adiabatischer Prozess, Beispiel, Unterschiede, Video und FAQs.Byju, 4. August. 2021.
Bild mit freundlicher Genehmigung:
1. "Adiabatic" von Benutzer: Stännered - Bild: adiabatisch.PNG (CC BY-SA 3.0) über Commons Wikimedia


