Unterschied zwischen Acetaldehyd und Aceton
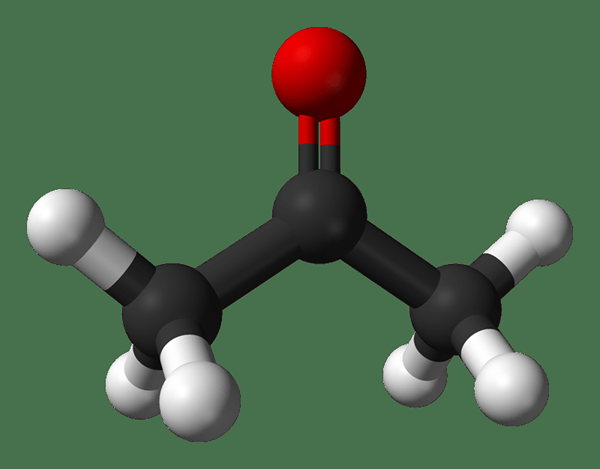
Schlüsselunterschied - Acetaldehyd gegen Aceton
Sowohl Acetaldehyd als auch Aceton sind kleine organische Moleküle, aber es gibt einen Unterschied zwischen ihnen, basierend auf ihren funktionellen Gruppen. Mit anderen Worten, sie sind zwei verschiedene Carbonylverbindungen mit unterschiedlichen chemischen und physikalischen Eigenschaften. Aceton ist das kleinste Mitglied der Ketongruppe, während Acetaldehyd das kleinste Mitglied der Aldehydgruppe ist. Der Schlüsselunterschied Zwischen Acetaldehyd und Aceton ist das Anzahl der Kohlenstoffatome in der Struktur; Aceton hat drei Kohlenstoffatome, Aber Acetaldehyd hat nur zwei Kohlenstoffatome. Der Unterschied in der Anzahl der Kohlenstoffatome und zwei verschiedene funktionelle Gruppen führen zu vielen anderen Unterschieden in ihren Eigenschaften.
Was ist Aceton?
Aceton ist das kleinste Mitglied der Ketone Group, auch bekannt als Propanon. Es ist eine farblose, flüchtige, brennbare Flüssigkeit, die als Lösungsmittel verwendet wird. Die meisten organischen Lösungsmittel lösen sich nicht in Wasser auf, aber Aceton ist mit Wasser mischbar. Es wird sehr oft für Reinigungszwecke im Labor und als Hauptwirkstoff in Nagellackentfernerflüssigkeiten und in Farbverdünner verwendet. 
Was ist Acetaldehyd?
Acetaldehyd, auch bekannt als als Ethanal ist das kleinste Mitglied der Aldehyde Group. Es ist eine farblose, brennbare Flüssigkeit mit einem starken erstickenden Geruch. Es gibt viele industrielle Verwendungen wie die Herstellung von Essigsäure, Parfums, Medikamenten und einigen Aromen.
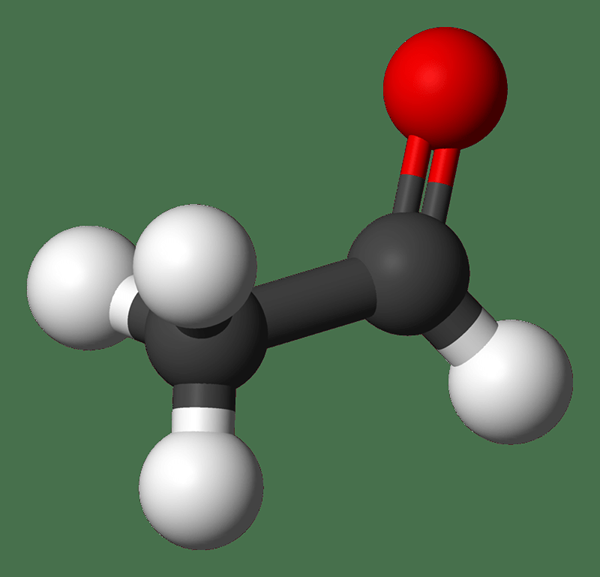
Was ist der Unterschied zwischen Acetaldehyd und Aceton?
Struktur und allgemeine Eigenschaften von Acetaldehyd und Aceton
Aceton: Die molekulare Formel von Aceton C3H6Ö. Es ist das einfachste Mitglied der Ketone -Familie. Es ist eine flüchtige, brennbare Flüssigkeit mit stechendem Geruch.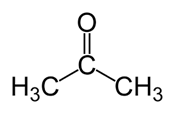
Acetaldehyd: Die molekulare Formel von Acetaldehyd C2H4Ö. Es ist das einfachste und eines der wichtigsten Mitglieder der Aldehydfamilie. Es ist eine farblose, flüchtige, brennbare Flüssigkeit bei der Raumtemperatur.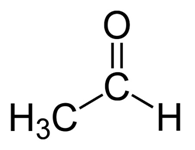
Vorkommen von Acetaldehyd und Aceton
Aceton: Im Allgemeinen ist Aceton im menschlichen Blut und im Urin vorhanden. Es wird auch während des normalen Stoffwechsels im menschlichen Körper erzeugt und entsorgt. Wenn Menschen Diabetiker haben, wird es in größeren Mengen im menschlichen Körper produziert.
Acetaldehyd: Acetaldehyd ist natürlich in verschiedenen Pflanzen (Kaffee), Brot, Gemüse und reifem Obst vorhanden. Außerdem kommt es in Zigarettenrauch, Benzin und Dieselabgasen vor. Außerdem ist es ein Zwischenprodukt im Stoffwechsel von Alkohol.
Verwendung von Acetaldehyd und Aceton
Aceton: Aceton wird hauptsächlich als organisch.
Acetaldehyd: Aceton wird zur Herstellung von Essigsäure, Parfums, Farbstoffen, Geschmacksmitteln und Medikamenten verwendet.
Eigenschaften von Acetaldehyd und Aceton
Identifikation
Aceton: Aceton liefert ein positives Ergebnis für den Iodoformtest. Daher kann es leicht von Acetaldehyd unter Verwendung eines Iodoformtests unterschieden werden.
Acetaldehyd: Acetaldehyd verleiht dem einen silbernen Spiegel "Tollens Reagenz" Während Ketone für diesen Test kein positives Ergebnis liefern. Weil es nicht leicht oxidieren kann. Chromsäuretest und Fehings Reagenz können auch verwendet werden, um Acetaldehyd zu identifizieren.
Reaktivität
Die Reaktivität von Carbonylgruppen (Aldehyde und Ketonen) ist hauptsächlich auf die Carbonylgruppe (C = O) zurückzuführen.
Aceton: Im Allgemeinen sind Alkylgruppen Elektronenspendegruppen. Aceton hat zwei Methylgruppen und verringert die Polarisation der Carbonylgruppe. Daher macht es die Verbindung weniger reaktiv. Zwei an beiden Seiten der Carbonylgruppe gebunden. Daher ist Aceton weniger reaktiv als Acetaldehyd.
Acetaldehyd: Im Gegensatz dazu hat Acetaldehyd nur eine Methylgruppe und ein Wasserstoffatom, das an die Carbonylgruppe gebunden ist. Wenn die Methylgruppe Elektronen spendet, zieht Wasserstoffatom Elektronen zurück. Dies macht das Molekül mehr polarisierter und macht das Molekül reaktiver. Im Vergleich zu Aceton hat Acetaldehyd weniger stearische Wirkungen, und andere Moleküle können sich leicht nähern. Aus diesen Gründen ist Acetaldehyd reaktiver als Aceton.


