Unterschied zwischen Säurebasenreaktion und Niederschlagsreaktion
Der Schlüsselunterschied Zwischen der Säure -Basen -Reaktion und der Niederschlagsreaktion ist das Die Reaktionen der Säurebasen umfassen die Neutralisation einer Säure von einer Base oder umgekehrt, während Niederschlagsreaktionen die Bildung eines Niederschlags nach Abschluss der Reaktion umfassen.
Es gibt verschiedene Arten von chemischen Reaktionen wie Kombinationsreaktionen, Zersetzung, Einzelverschiebung und doppelte Verschiebungsreaktionen, Verbrennung, Redoxreaktionen usw. Säurebasis und Niederschlagsreaktionen sind solche zwei Arten.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist eine Säurebasenreaktion
3. Was ist eine Niederschlagsreaktion
4. Seite an Seitenvergleich - Säurebasenreaktion gegenüber Niederschlagsreaktionsreaktionsreaktion
5. Zusammenfassung
Was ist eine Säurebasenreaktion?
Eine Säurebasenreaktion ist eine chemische Reaktion, bei der eine Säure mit einer Base reagiert oder umgekehrt. Hier tritt eine Neutralisation auf; Säure neutralisiert die Base oder umgekehrt; Daher können wir es auch als Neutralisationsreaktion bezeichnen. Darüber hinaus sind das Endprodukt dieser Reaktionen Salze aus Säureanionen und Kationen der Basis sowie Wassermoleküle. Bei dieser Reaktion können Bindungsunterbrechungen und Bindungsbildung auftreten.
Darüber hinaus kann die Säurebasenreaktion auf zwei Arten auftreten: Wenn die Reaktion zwischen einer starken Säure und einer starken Base auftritt, ist es im Wesentlichen eine quantitative Reaktion. Das bedeutet; Die Reaktion erfolgt, bis Säure und/oder Base vollständig verbraucht sind. Wenn jedoch die Reaktion zwischen einer schwachen Säure und/oder einer schwachen Base auftritt, wird ein Gleichgewicht stattfinden. Diese Art von Reaktion ist jedoch nicht quantitativ, da eine schwache Säure oder eine schwache Base eine Pufferlösung ist.
Zum Beispiel ist die Reaktion zwischen HCl und NaOH quantitativ, da HCL eine starke Säure ist und NaOH eine starke Basis ist.
HCl(aq) + Na (OH)(aq) → h2O + NaCl(aq)
Die Reaktion zwischen Adenin und Wasserstoffphosphat ist jedoch nicht quantitativ, da Wasserstoffphosphat eine schwache Säure ist. Dann ist das Gleichgewicht wie folgt:
AH+HPO42– ⇌ a- + H2Po–4
Was ist eine Niederschlagsreaktion?
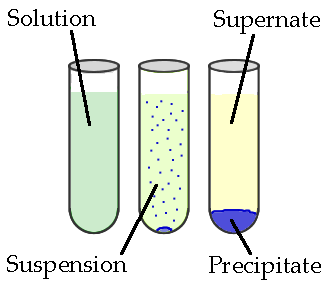
Eine Niederschlagsreaktion ist eine Art chemischer Reaktion, bei der sich ein Niederschlag am Ende der Reaktion bildet. Hier sind die Reaktanten zwei lösliche Salze. Diese Salze verbinden sich miteinander, um ein unlösliches Salz zu ergeben, den wir den Niederschlag nennen. Ferner kann der Niederschlag auf zwei verschiedene Arten existieren: als Suspension oder feste Masse, die auf den Boden des Behälters sinkt.

Wenn es sich um eine Suspension handelt, können wir es durch Zentrifugation, Dekantierung oder Filtration vom Reaktionsgemisch trennen. Die verbleibende Flüssigkeit nach der Trennung des Niederschlags wird als Überstand bezeichnet.
Was ist der Unterschied zwischen der Reaktion der Säurebasen und der Niederschlagsreaktion?
Säurebasen- und Niederschlagsreaktionen sind zwei Arten von chemischen Reaktionen. Der Schlüsselunterschied zwischen der Reaktion der Säurebasen und der Niederschlagsreaktion besteht darin, dass die Säurebasenreaktionen die Neutralisation einer Säure von einer Base oder umgekehrt umfassen, während Niederschlagsreaktionen die Bildung eines Niederschlags nach Abschluss der Reaktion umfassen. Der Prozess einer Säurebasenreaktion umfasst die Kombination von Anionen und Kationen zur Bildung von Salz und Wasser, während der Prozess der Niederschlagsreaktion die Bildung eines unlöslichen Salzes aus löslichen Salzen umfasst.

Zusammenfassung -Säurebasenreaktion gegen Niederschlagsreaktion
Zusammenfassend lässt sich sagen. Der Schlüsselunterschied zwischen der Reaktion der Säurebasen und der Niederschlagsreaktion besteht darin, dass die Säurebasenreaktionen die Neutralisation einer Säure von einer Base oder umgekehrt umfassen, während Niederschlagsreaktionen nach Abschluss der Reaktion die Bildung eines Niederschlags umfassen.
Referenz:
1. Helmenstine, Anne Marie. „Definition der Niederschlagsreaktion.”Thoughtco, Jan. 22, 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Chemisches Niederschlagsdiagramm" von Zabmilenko - eigene Arbeit (Public Domain) über Commons Wikimedia


