Unterschied zwischen Amid und Peptidbindung
Der Schlüsselunterschied Zwischen Amid und Peptidbindung ist das Eine Amidbindung bildet zwischen einer Hydroxylgruppe und einer Aminogruppe von zwei Molekülen, während sich eine Peptidbindung zwischen zwei Aminosäuremolekülen während der Bildung einer Peptidkette bildet.
Amidbindungen und Peptidbindungen sind biochemische Bindungen, die zwischen einem Kohlenstoffatom und einem Stickstoffatom von zwei getrennten Molekülen bilden. Normalerweise bilden sich diese Bindungen zwischen zwei Aminosäuremolekülen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was sind Amidbindungen
3. Was sind Peptidbindungen?
4. Seite an Seitenvergleich - Amid gegen Peptidbindung in tabellarischer Form
5. Zusammenfassung
Was sind Amidbindungen?
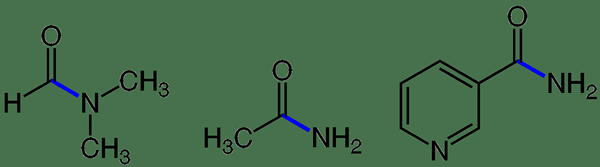
Amidbindungen sind eine Art kovalenter Bindung, die ein Amid als Endprodukt bildet. Es gibt drei Haupttypen von Amiden als Carboxamide, Sulfonamide und Phosphoramide. Die einfachsten Amide sind jedoch Derivate von Ammoniak.

Abbildung 01: verschiedene Amidbindungen
Amide werden im Allgemeinen als sehr schwache Basen im Vergleich zu Aminen eingestuft. Daher zeigen diese Substanzen keine Säure-Basis-Eigenschaften im Wasser. Eine Peptidbindung ist eine Art Amidbindung. Hier bildet sich die Amidbindung, wenn die Carboxsäurgruppe von einer Aminosäure mit der Amingruppe einer anderen Aminosäure reagiert. Eine kovalente Bindung bildet sich durch Entfernen eines Wassermoleküls. Daher ist es eine Kondensationsreaktion.
Was sind Peptidbindungen??
Eine Peptidbindung ist eine Art kovalente Bindung, die zwischen zwei Aminosäuren bildet. Eine Peptidbindung bildet sich zwischen einem Kohlenstoffatom einer Aminosäure und dem Stickstoffatom der Aminosäure, das bei der Entfernung eines Wassermoleküls auftritt. Bei der Betrachtung der Grundstruktur von Aminosäure besteht es aus einem zentralen Kohlenstoffatom, das an eine Carboxylgruppe, eine Aminogruppe, ein Wasserstoffatom und eine Alkylgruppe gebunden ist. Im Allgemeinen unterscheiden sich Aminosäuren gemäß der Struktur der Alkylgruppe voneinander.
Während der Bildung einer Peptidbindung tritt eine Kondensationsreaktion zwischen zwei Aminosäuren auf. Hier reagiert die Carbonsäure einer Aminosäure mit der Amingruppe einer anderen Aminosäure, wobei ein Wassermolekül freigelassen wird. Die -OH -Gruppe der Carboxylsäuregruppe bildet ein Wassermolekül, das sich mit einem Wasserstoff aus der Amingruppe kombiniert.
Wir können die Peptidbindung als -konh -Bindung abkürzen, weil die Bindung, die sich bildet, diese vier Atome umfasst. Wenn zwei Aminosäuren durch eine Peptidbindung aneinander binden, ist das Endprodukt ein Dipeptid. Wenn jedoch mehrere Aminosäuren miteinander binden, bildet sich ein Oligopeptid. Wenn eine hohe Anzahl von Aminosäuren durch Peptidbindungen miteinander bindet, ist das komplexe Molekül ein Polypeptid.
Eine Peptidbindung kann Hydrolysereaktionen durchlaufen. Die Hydrolyse bricht die Bindung ab und trennt die beiden Aminosäuren. Obwohl der Prozess sehr langsam ist, kann die Hydrolyse in Gegenwart von Wasser auftreten.
Was ist der Unterschied zwischen Amid und Peptidbindung?
Amid- und Peptidbindungen sind biochemische Bindungen. Der Schlüsselunterschied zwischen Amid und Peptidbindung besteht darin, dass eine Amidbindung zwischen einer Hydroxylgruppe und einer Aminogruppe von zwei Molekülen bildet.
Die folgende Infografik fasst den Unterschied zwischen Amid und Peptidbindung zusammen.
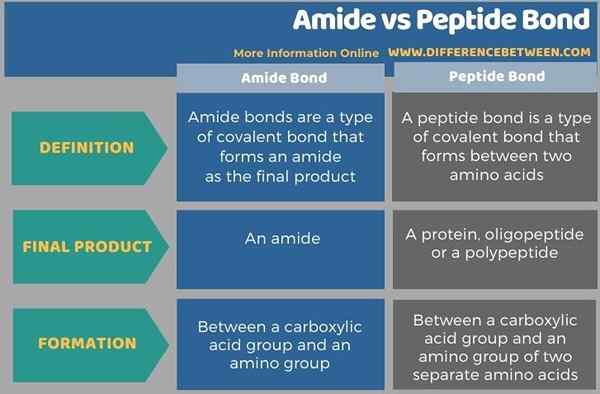
Zusammenfassung -Amid gegen Peptidbindung
In der Biochemie spielen Amidbindungen und Peptidbindungen eine sehr wichtige Rolle bei der Bildung eines Proteinmoleküls. Der Schlüsselunterschied zwischen Amid und Peptidbindung besteht darin, dass eine Amidbindung zwischen einer Hydroxylgruppe und einer Aminogruppe von zwei Molekülen bildet.
Referenz:
1. Helmenstine, Anne Marie. „Amiddefinition und Beispiele in der Chemie.”Thoughtco, Februar. 11, 2020, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. „Amidbindungen Amides V.1 ”von Jü - eigener Arbeit (CC0) über Commons Wikimedia


