Unterschied zwischen Ammoniak und ammoniakalischem Stickstoff
Der Schlüsselunterschied Zwischen Ammoniak und ammoniakalischem Stickstoff befindet sich die Ammoniak ist eine anorganische Verbindung mit der chemischen Formel NH3, während der ammoniakalische Stickstoff ein Maß für die Ammoniakmenge in einer Probe ist.
Ammoniak ist eine gasförmige Verbindung mit einem charakteristischen, scharfen Geruch. Obwohl es bei vielen Gelegenheiten nützlich ist, ist es auch eine giftige Verbindung. Es ist ein häufiger giftiger Schadstoff in Abfallprodukten wie Abwasser, Mist usw. Wir verwenden ammoniakalische Stickstoff, um die Menge dieser toxischen Verbindung zu messen.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Ammoniak
3. Was ist ammoniakaler Stickstoff?
4. Seite an Seitenvergleich - Ammoniak gegen Ammoniakalstickstoff in tabellarischer Form
5. Zusammenfassung
Was ist Ammoniak?
Ammoniak ist eine anorganische Verbindung mit der chemischen Formel NH3. Daher ist es eine gasförmige Verbindung mit einem charakteristischen, scharfen Geruch. Der IUPAC -Name dieser Verbindung ist Azane. Die Molmasse beträgt 17 g/mol und der Siedepunkt –33.34 ° C. Ein Ammoniakmolekül hat ein Stickstoffatom, das über kovalente Bindungen an drei andere Wasserstoffatome gebunden ist. Darüber hinaus hat dieses Molekül eine trigonale Pyramidenform und es ist ein farbloses Gas, das leichter ist als normale Luft.
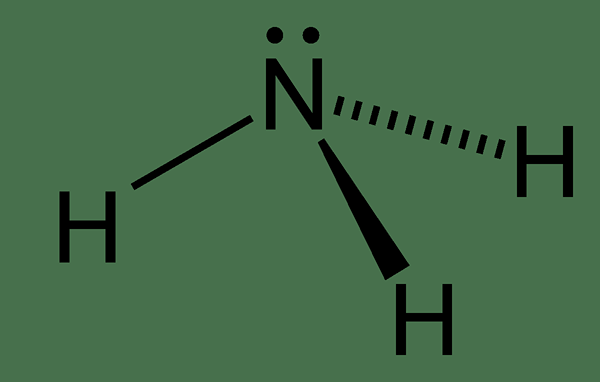
Abbildung 01: Chemische Struktur von Ammoniak
Es gibt Wasserstoffbrückenbindungen zwischen Ammoniakmolekülen. Daher können wir dieses Gas leicht verflüssigen. Diese Verbindung ist in stickstoffhaltigem Abfall von Wasserorganismen häufig. Darüber hinaus trägt es zu den Ernährungsbedürfnissen terrestrischer Organismen bei. Durch die Bereitstellung von Lebensmitteln und Düngemittelbedürfnissen. In seiner konzentrierten Form ist Ammoniak jedoch gefährlich und ätzend.
Was ist ammoniakaler Stickstoff??
Ammoniakalstickstoff ist ein Maß für die Ammoniakmenge in einer Probe. Hier bestimmen wir die toxische Wirkung von Ammoniak auf Deponie -Sackgewirr, Abfallprodukten wie Gülle usw. Daher messen wir die Gesundheit natürlicher Gewässer, da Ammoniak uns direkt in hohen Konzentrationen vergiften kann. Wir bezeichnen ammoniakalischen Stickstoff als NH3-N.

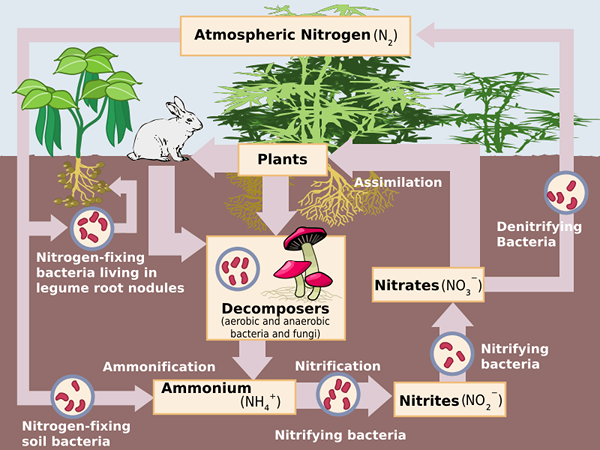
Abbildung 02: Stickstoffzyklus zeigt die ammoniakalischen Stickstoffformen in der Umgebung
Die Messeinheit ist mg/l. Bei dieser Messung messen wir alle Ammoniakformen; Ammoniak (NH3), Ammonium (NH4+), Stickstoffgas (n)2), Nitrate (nein3-), Nitriten (nein2-), organischer Stickstoff wie Proteine, DNA usw.
Was ist der Unterschied zwischen Ammoniak und ammoniakalischem Stickstoff?
Ammoniak ist eine anorganische Verbindung mit der chemischen Formel NH3. Es ist bei niedriger Konzentration nützlich und in hohen Konzentrationen giftig. Ammoniakalstickstoff ist ein Maß für die Ammoniakmenge in einer Probe. Es misst die Menge an Ammoniak auf seinen toxischen Werten. Darüber hinaus bezieht es sich auf alle Ammoniakformen wie Ammoniak (NH3), Ammonium (NH4+), Stickstoffgas (n)2), Nitrate (nein3-), Nitriten (nein2-), organischer Stickstoff wie Proteine, DNA usw.

Zusammenfassung -Ammoniak gegen Ammoniacal Stickstoff
Ammoniak und Ammoniakalstickstoff sind zwei verwandte Begriffe. Der Unterschied zwischen Ammoniak und ammoniakalischem Stickstoff besteht darin.
Referenz:
1. "Ammoniak.Nationales Zentrum für Biotechnologieinformationen. Pubchem Compound -Datenbank, u.S. Nationalbibliothek für Medizin. Hier verfügbar
2. „Ammoniakaler Stickstoff.Wikipedia, Wikimedia Foundation, 10. Juli 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.'Ammoniak-2D'By Radio89-eigene Arbeit, (CC BY-SA 3.0) über Commons Wikimedia
2.'Stickstoffzyklus' von Burkhard (CC BY-SA 3.0) über Commons Wikimedia