Differenz zwischen ausgeglichener Gleichung und Netto -Ionengleichung

Schlüsseldifferenz - ausgewogene Gleichung im Vergleich zu Netto -Ionengleichung
Alle chemischen Reaktionen können als Gleichung geschrieben werden. Zu den Komponenten dieser Gleichung gehören Reaktanten mit ihren physischen Zuständen, ein Pfeil, der die Reaktionsrichtung und die Reaktionsprodukte mit ihren physischen Zuständen zeigt. Wenn besondere Bedingungen verwendet wurden, werden sie auch kurz auf dem Pfeil geschrieben. Wenn sich die Reaktion im Gleichgewicht befindet, werden in entgegengesetzten Richtungen zwei halbe Pfeile verwendet. Eine chemische Gleichung kann auf zwei Arten geschrieben werden: als ausgewogene Gleichung oder als Netto -ionische Gleichung. Der Schlüsselunterschied zwischen ausgewogener Gleichung und nettoer Ionengleichung besteht darin Die ausgewogene Gleichung zeigt alle Reaktionen, die zusammen in einem System stattgefunden haben wohingegen Die Netto -Ionengleichung zeigt nur die Nettoreaktion, die nach Abschluss dieser bestimmten Reaktion aufgetreten ist.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist eine ausgewogene Gleichung
3. Was ist eine Netto -ionische Gleichung
4. Seite an Seitenvergleich - ausgeglichene Gleichung gegen die Netto -Ionen -Gleichung
5. Zusammenfassung
Was ist eine ausgewogene Gleichung?
Chemische Reaktionen sind sehr wichtig, um das Verhalten eines bestimmten Systems zu verstehen. Durch das Schreiben der richtigen Gleichung für die Reaktion kann man eine Vorstellung von den Änderungen verschiedener Arten in diesem System bekommen. Für einfache Reaktionen wie das Auflösen von NaCl in Wasser kann die Gleichung leicht geschrieben werden, indem die möglichen Produkte dieser Reaktion vorhergesagt werden. Für andere komplexe Reaktionen müssen jedoch möglicherweise weitere Tests durchgeführt werden, um die Produkte dieses bestimmten Systems herauszufinden. In den meisten Fällen ist die schriftliche Gleichung jedoch sehr wahrscheinlich unausgeglichen, was es schwierig macht, das chemische Verhalten dieses Systems zu erklären. Daher sollten auch unausgeglichene Gleichungen ausgeglichen sein. Die ausgewogene Gleichung umfasst alle Reaktanten und Produkte dieses Systems. Die Gleichung wird durch Betrachtung der Reaktantenverbindung als Molekül geschrieben. Zum Beispiel die ausgewogene Gleichung zwischen KI und PBNO3 (Wenn diese in Wasser reagiert würden) wäre;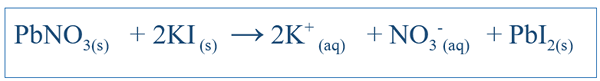
Die Bedeutung einer ausgewogenen Gleichung ist, dass sie die Mengen von Reaktanten zeigt, die hinzugefügt werden sollten, Einzelheiten zu den stöchiometrischen Beziehungen zwischen den Spezies im System zu geben. Im obigen Beispiel das Verhältnis zwischen PBNO3 und KI sollte 1: 2 sein, wenn diese Komponenten in das System hinzugefügt werden.
Was ist eine Netto -ionische Gleichung?
Die Netto -ionische Gleichung zeigt nur die Gesamtreaktion, die im System stattgefunden hat. Es umfasst die ionischen Arten und gebildete Produkte. Es zeigt jedoch nicht alle Reaktionen an, die in einem bestimmten System stattgefunden haben. Wenn beispielsweise eine Reaktion zwischen zwei Molekülen mit Wasser als Medium vorliegt, können sich die Verbindungen in Wasser gelöst und in Ionen getrennt haben. Einige dieser Ionen können an der Reaktion beteiligt sein, andere jedoch nicht. Dann umfasst die Netto -ionische Gleichung nur die Ionen, die an einer Nettoreaktion teilgenommen haben. Andere Ionen, die als Zuschauerionen bezeichnet werden, werden aus der Gleichung beseitigt, um die ionische Netto -Gleichung zu erhalten. Zum Beispiel, wenn Ki und PBNO3 In Wasser reagiert, wäre die ionische Nettoreaktion;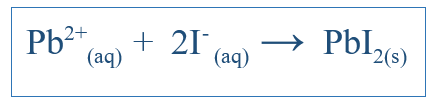
Dies sollte auch K beinhalten+ Ion und No3- Ion, aber diese Ionen werden sich nur auflösen und nicht an der Hauptreaktion teilnehmen; Daher sind sie nicht in die ionische Nettoreaktion einbezogen.
Was ist der Unterschied zwischen ausgeglichener Gleichung und Netto -Ionengleichung?
Ausgeglichene Gleichung gegen Netto -Ionengleichung | |
| Alle verwendeten Komponenten werden als Reaktanten in der ausgewogenen Gleichung geschrieben. | Reaktanten, die nur an der Nettoreaktion beteiligt waren. |
| Produkte | |
| Alle Komponenten am Ende der Reaktion sind in einer ausgewogenen Gleichung enthalten. | In einer Netto -ionischen Gleichung ist nur das Netto -Endprodukt geschrieben. |
| Details angegeben | |
| Die ausgewogene Gleichung gibt Details zu allen Arten, die sich im System befinden. | Die Netto -ionische Gleichung gibt Details nur über Arten, die an der Reaktion teilgenommen haben |
Zusammenfassung - ausgewogene Gleichung im Vergleich zu Netto -ionischen Gleichung
Wenn bestimmte ionische Verbindungen zu Wasser zugesetzt werden, brechen sie auseinander und bilden Ionen, die in Wasser gelöst sind. Dies erzeugt Anionen und Kationen. Um die produzierten Spezies nach Abschluss der Reaktion und der Reaktionsrichtung zu zeigen, kann eine chemische Gleichung geschrieben werden. Diese Gleichung kann unter Berücksichtigung der Anzahl der Atome jeder Art, die sich auf den beiden Seiten des Pfeils befinden, ausgeglichen werden. Manchmal sollte sogar die Ladung dieser Arten in Betracht gezogen werden. Dies gibt eine ausgewogene chemische Gleichung für dieses bestimmte System. Die Netto -ionische Gleichung umfasst jedoch nur die reagierten Spezies. Wie bereits erwähnt, besteht der Schlüsselunterschied zwischen ausgewogener Gleichung und Netto -ionischer Gleichung darin, dass die ausgeglichene Gleichung alle Reaktionen in einem System zeigt.
Verweise:
1. Chang, r., 2010. Chemie. 10. Aufl. Newyork: McGraw-Hill.
2. Chemische Reaktionen. (N.D.). Abgerufen am 26. Mai 2017 von http: // www.Ric.edu/fakultät/ptiskus/reaktionen/
3. Vollständige ionische und netto -ionische Gleichungen. (N.D.). Abgerufen am 26. Mai 2017 von https: // www.Khan Akademie.org/naturwissenschaft/chemisch/chemische reaktionen-stöchiom/-typen-von-chemischen reaktionen/a/vollständig-ionisch-netionischen Gleichung.


