Unterschied zwischen Brom und Bromid

Der Schlüsselunterschied Zwischen Brom und Bromid ist das Bromid ist die reduzierte Form von Brom.
Die chemischen Elemente im Periodenzüchter sind außer den edlen Gasen nicht stabil. Element. Ebenso muss Brom auch ein Elektron bekommen, um die Elektronenkonfiguration des Edelgas Krypton zu erreichen. Alle Metalle reagieren mit Brom und bilden Bromide. Brom und Bromid haben aufgrund der Änderung eines Elektrons unterschiedliche physikalische und chemische Eigenschaften.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Brom?
3. Was ist Bromid
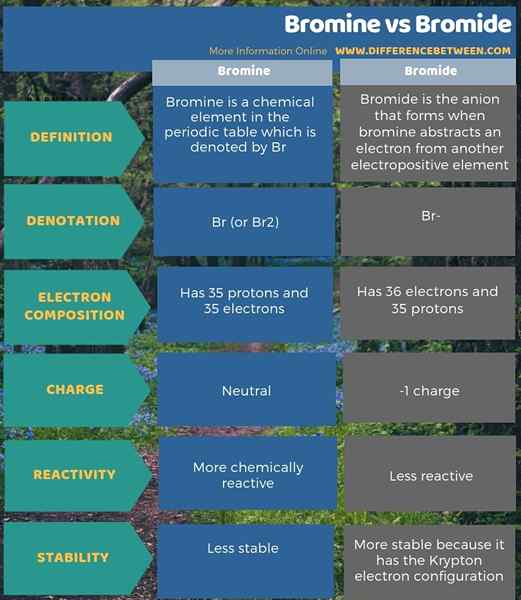
4. Seite an Seitenvergleich - Brom gegen Bromid in tabellarischer Form
5. Zusammenfassung
Was ist Brom??
Brom ist ein chemisches Element in der periodischen Tabelle, die von BR gekennzeichnet ist. Es ist ein Halogen (17th Gruppe) in der 4th Zeitraum der Periodenzüchter. Die atomare Anzahl von Brom beträgt 35; Somit hat es 35 Protonen und 35 Elektronen. Die Elektronenkonfiguration beträgt [AR] 4s2 3d10 4p5. Seit der P Sublevel sollte 6 Elektronen haben, um die Krypton Noble Gaselektronenkonfiguration zu erhalten. Brom hat die Fähigkeit, ein Elektron anzuziehen. Es hat eine hohe Elektronegativität, die ungefähr 2 ist.96, gemäß der Pauling -Skala.
Das Atomgewicht von Brom beträgt 79.904 Amu. Unter Raumtemperatur existiert es als zweistiges Molekül (BR2). Außerdem ist dieses Diatommolekül eine rotbraune Farbflüssigkeit. Brom hat einen Schmelzpunkt von 265.8 K und ein Siedepunkt von 332.0 k.
Weitere Eigenschaften von Brom
Unter allen Bromisotopen sind BR-79 und BR-81 die stabilsten Isotope. Darüber hinaus ist dieses chemische Element in Wasser leicht löslich, aber in organischen Lösungsmitteln wie Chloroform gut löslich, gut löslich. Darüber hinaus hat es 7, 5, 4, 3, 1, -1 Oxidationszustände.
Die chemische Reaktivität von Brom liegt zwischen der von Chlor und Jod. Brom ist weniger reaktiv als Chlor, aber reaktiver als Jod. Brom produziert das Bromidion durch Einnahme eines Elektrons. Daher nimmt Brom leicht an der ionischen Verbindungsbildung beteiligt. Tatsächlich existiert Brom in der Natur als Bromidsalze anstelle von BR2.

Abbildung 01: Brom
Brom kann die Elementanionen oxidieren. Es kann jedoch kein Chlorid oxidieren, um Chlor zu geben. Darüber hinaus können wir BR produzieren, indem wir bromidreiche Sole mit Chlorgas behandeln. Oder Bromgas wird gebildet, indem HBR mit Schwefelsäure behandelt wird. Brom ist sehr nützlich in Industrie- und chemischen Labors. Bromidverbindungen sind als Benzinzusatzstoffe für Pestizide und als Desinfektionsmittel in der Wasserreinigung wichtig.
Was ist Bromid?
Bromid ist das Anion, das sich bildet, wenn Brom ein Elektron aus einem anderen elektropositiven Element abtrkt. Wir können es durch das Symbol BR repräsentieren-. Es ist ein einwertiges Ion mit -1 Ladung. Daher hat es 36 Elektronen und 35 Protonen.

Die Elektronenkonfiguration von Bromid beträgt [AR] 4s2 3d10 4p6. Es existiert in ionischen Verbindungen wie Natriumbromid, Calciumbromid und HBR. Es existiert auch natürlich in Wasserquellen.
Was ist der Unterschied zwischen Brom und Bromid?
Brom ist ein chemisches Element in der periodischen Tabelle, die von Br, während Bromid das Anion ist, das sich bildet, wenn Brom ein Elektron aus einem anderen elektropositiven Element abtrkt. Darüber hinaus besteht der Hauptunterschied zwischen Brom und Bromid darin, dass Bromid die reduzierte Form von Brom ist. Außerdem hat Bromid 36 Elektronen im Vergleich zu 35 Elektronen Brom, aber beide haben 35 Protonen. Daher hat Bromid eine Ladung von -1, während Brom neutral ist.
Darüber hinaus ist Brom chemisch reaktiv als Bromid. Ein weiterer Unterschied zwischen Brom und Bromid besteht darin, dass das Bromid die Krypton -Elektronenkonfiguration erreicht hat und daher stabiler ist als das Bromatom.
Zusammenfassung -Brom gegen Bromid
Brom ist ein chemisches Element in der Periodenzüchttabelle und wird mit BR gekennzeichnet. In der Zwischenzeit ist Bromid das Anion, das sich bildet, wenn Brom ein Elektron aus einem anderen elektropositiven Element abstrahiert. Darüber hinaus besteht der Hauptunterschied zwischen Brom und Bromid darin, dass Bromid die reduzierte Form von Brom ist.
Bild mit freundlicher Genehmigung:
1. "Brom 25ml (transparent)" von w. Oelen -(CC BY -SA 3.0) über Commons Wikimedia
2. "Br-" von Neurotiker - eigene Arbeit (öffentlich zugänglich) über Commons Wikimedia


