Unterschied zwischen Butan und Isobutan

Butan gegen Isobutan
Organische Moleküle sind Moleküle aus Kohlenstoffen. Kohlenwasserstoffe sind organische Moleküle, die nur aus Kohlenstoff- und Wasserstoffatomen bestehen. Kohlenwasserstoffe können aromatisch oder aliphatisch sein. Sie sind hauptsächlich in wenige Typen als Alkane, Alkene, Alkine, Cycloalkane und aromatische Kohlenwasserstoffe unterteilt. Hexan und N-Hexan sind Alkane oder auf andere Weise, die als gesättigte Kohlenwasserstoffe bezeichnet werden. Sie haben die höchste Anzahl von Wasserstoffatomen, die ein Molekül aufnehmen kann. Alle Bindungen zwischen Kohlenstoffatomen und Wasserdingen sind einzelne Bindungen. Aus diesem Grund ist die Bindungsrotation zwischen allen Atomen zulässig. Sie sind die einfachste Art von Kohlenwasserstoffen. Gesättigte Kohlenwasserstoffe haben die allgemeine Formel von CNH2n+2. Diese Bedingungen unterscheiden sich für die Cycloalkane leicht, da sie zyklische Strukturen haben.
Butan
Wie oben erwähnt, ist Butankohlenwasserstoff ein gesättigtes Alkan. Es hat vier Kohlenstoffatome; Daher hat die molekulare Formel von C4H10. Molmasse von Butan ist 58.12 g mol–1. Der Schmelzpunkt von Butan ist 133-139 K und der Siedepunkt 272-274 K ist. Butan ist der gebräuchliche Name, der verwendet wird, um alle Moleküle mit dieser Formel anzuzeigen. Es gibt zwei strukturelle Isomere, die wir zeichnen können, um dieser Formel zu entsprechen. Es hat die folgende Struktur.

Anderes strukturelles Isomer ist wie methyliertes Propanmolekül. Es ist als Isobutan bekannt. Butan ist ein farbloses Gas. Es kann leicht verflüssigt werden. Das Butangas ist sehr brennbar. Butan ist ein Bestandteil von Erdgas und wird erzeugt, wenn Benzin verfeinert wird. Bei vollständiger Verbrennung produziert Butan Kohlendioxid und Wasser. Wenn es jedoch nicht genügend Sauerstoffgas für die Verbrennung gibt, erzeugt es Kohlenmonoxid und Wasser aus der Teilverbrennung. Butan wird als Kraftstoff verwendet. Bei der Herstellung von LP -Gas wird Butan mit Propan und anderen Kohlenwasserstoffen gemischt. Diese werden zu Kochzwecken im Haushalt verwendet. Es wird auch in Feuerzeugen verwendet.
Isobutan
Isobutan ist ein strukturelles Isomer von Butan. Es hat die gleiche molekulare Formel wie Butan, aber die strukturelle Formel ist unterschiedlich. Es ist auch als Methylpropan bekannt. Es hat die folgende Struktur.
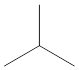
Isobutan hat einen tertiären Kohlenstoff und es ist das einfachste Molekül mit einem tertiären Kohlenstoff. Isobutan ist ein farbloses, geruchloses, transparentes Gas. Der Schmelzpunkt von Isobutan ist 40-240 K und der Siedepunkt 260-264 K beträgt. Es wird hauptsächlich als Kältemittel verwendet. Reine Form von Isobutan wird in Kühlschränken verwendet. Außerdem wird es als Treibmittel in Aerosolsprays verwendet.
| Was ist der Unterschied zwischen Butan und Isobutan? • Isobutan ist ein strukturelles Isomer von Butan. • Butan ist unverzweigt und Isobutan ist verzweigt. • Beide haben die gleiche molekulare Formel, aber die strukturelle Formel ist unterschiedlich. • Butan hat vier Kohlenstoffatome in der geraden Kette, während Isobutan nur drei Kohlenstoffatome in der geraden Kette hat. • Physikalische Eigenschaften von Butan und Isobutan sind unterschiedlich. Zum Beispiel haben sie unterschiedliche Schmelzpunkte, Siedepunkte, Dichte usw. • Reines Isobutan wird hauptsächlich als Kältemittel verwendet |


