Differenz zwischen Calciumcarbonat und Calciumbicarbonat

Der Schlüsselunterschied Zwischen Calciumcarbonat und Calciumbicarbonat befindet sich die Calciumcarbonatmolekül besteht aus chemischen Elementen Ca, C und O, während Calciumbicarbonat aus chemischen Elementen Ca, C, O und H besteht.
Calciumcarbonat ist ein Carbonat aus Kalzium, das die chemische Formel -Caco hat3. Es kommt natürlich vor und erscheint als weißer Feststoff. Im Gegenteil, Calciumbicarbonat ist nicht fest. Die chemische Formel dieser Verbindung ist CA (HCO3)2.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Calciumcarbonat
3. Was ist Calciumbicarbonat
4. Seite für Seitenvergleich - Calciumcarbonat gegen Calciumbicarbonat in tabellarischer Form
5. Zusammenfassung
Was ist Calciumcarbonat?
Calciumcarbonat ist ein Carbonat aus Kalzium, das die chemische Formel -Caco hat3. Diese Verbindung tritt natürlich als Kalkstein, Kreide, Calcit usw. auf. Daher ist es eine häufige Substanz in Felsen. Ex: Calcit oder Aragonit (Kalkstein enthält beide Formen). Diese Verbindung tritt als weiße hexagonale Kristalle oder Pulver auf und ist geruchlos.

Abbildung 01: Calciumcarbonatkristalle
Darüber hinaus hat es einen kalkhaltigen Geschmack. Die Molmasse dieser Verbindung beträgt 100 g/mol und der Schmelzpunkt beträgt 1.339 ° C (für die Calcit -Form). Es hat jedoch keinen Siedepunkt, da sich diese Verbindung bei hohen Temperaturen zersetzt. Wir können diese Verbindung erhalten, indem wir die Calcium-tragenden Mineralien abbilden. Aber diese Form ist nicht rein. Wir können eine reine Form mit einer reinen, abgebrannten Quelle wie Marmor erhalten. Wenn Calciumcarbonat mit Säuren reagiert, bildet es CO2 Gas. Wenn es mit Wasser reagiert, bildet es Calciumhydroxid. Darüber hinaus kann es sich einer thermischen Zersetzung ergeben, um Co zu veröffentlichen2 Gas.
Was ist Calciumbicarbonat?
Calciumbicarbonat ist Carbonat von Calcium mit der chemischen Formel CA (HCO3)2. Es tritt nicht als Feststoff vor, existiert nur als wässrige Lösung. Diese Lösung enthält Calciumionen (CA)2+), Bicarbonationen (HCO3-) und co32- zusammen mit gelöstem Kohlendioxid. Die Konzentrationen dieser Ionen hängen jedoch vom pH -Wert des Mediums ab, was bedeutet, dass unterschiedliche Ionen bei verschiedenen pH -Werten vorherrschen.
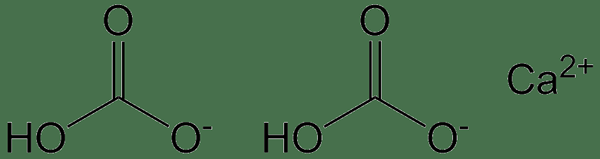
Abbildung 02: Chemische Struktur von Calciumbicarbonat
Die Molmasse dieser Verbindung ist 162.11 g/mol. Diese Verbindung bildet sich, wenn Regenwasser, das gelöstes Kohlendioxid enthält, mit Kalkstein reagiert. Folglich wäscht diese Verbindung mit Regenwasser weg.
Was ist der Unterschied zwischen Calciumcarbonat und Calciumbicarbonat?
Calciumcarbonat ist ein Carbonat aus Kalzium, das die chemische Formel -Caco hat3. Die Molmasse dieser Verbindung beträgt 100 g/mol. Darüber hinaus enthalten diese Moleküle CA-, C- und O -chemische Elemente. Calciumbicarbonat ist Carbonat von Calcium mit der chemischen Formel CA (HCO3)2. Die Molmasse dieser Verbindung ist 162.11 g/mol. Darüber hinaus enthalten diese Moleküle CA-, C-, O- und H -chemische Elemente.

Zusammenfassung -Calciumcarbonat gegen Calciumbicarbonat
Das Carbonat von Calcium ist Calciumcarbonat und Calciumbicarbonat. Der Hauptunterschied zwischen Calciumcarbonat und Calciumbicarbonat besteht darin.
Referenz:
1. "Kalziumkarbonat.Nationales Zentrum für Biotechnologieinformationen. Pubchem Compound -Datenbank, u.S. Nationalbibliothek für Medizin. Hier verfügbar
2. „Calciumbicarbonat.Wikipedia, Wikimedia Foundation, 29. Juni 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.'Calciumcarbonat Rocks'By Ferdous - eigene Arbeit, (CC BY -SA 3.0) über Commons Wikimedia
2.'Calcium Bicarbonat'by Epop - eigene Arbeit (öffentlich zugänglich) über Commons Wikimedia


