Unterschied zwischen Chlorat und Perchlorat
Der Schlüsselunterschied Zwischen Chlorat und Perchlorat ist das Chlorat ist das Anion, das aus der Dissoziation von Chlorsäure abgeleitet ist, während Perchlorat das Anion ist, das aus der Dissoziation von Perchlorsäure abgeleitet ist.
Chlorat und Perchlorat sind Oxyanionen, die Chlor- und Sauerstoffatome enthalten. Im Allgemeinen werden diese Begriffe auch verwendet, um die Salze von Chlor- und Perchlorsäure zu benennen. Mit anderen Worten, der Begriff Chlorat kann sich auf jede Verbindung beziehen, die ein Chloratanion mit einem anderen Kation enthält.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Chlorat
3. Was ist Perchlorat
4. Seite an Seitenvergleich - Chlorat gegen Perchlorat in tabellarischer Form
5. Zusammenfassung
Was ist Chlorat?
Chlorat ist ein Anion mit der chemischen Formel CLO3-. Der Oxidationszustand des Chorinatoms beträgt +5. Die chemischen Verbindungen, die dieses Anion enthalten, werden jedoch auch als allgemeiner Begriff als Chlorate bezeichnet. Dieses Anion ist das Salz der Chorsäure. Die Struktur dieses Anions ist wie folgt:
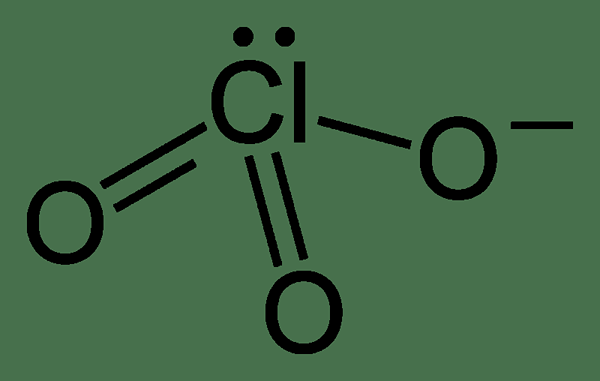
Die Geometrie dieses Anion ist trigonaler Pyramiden. Darüber hinaus sind die Verbindungen, die dieses Anion enthalten. Daher müssen wir sie von leicht oxidierten Materialien fernhalten. Dieses Anion kann Resonanz zeigen; Daher ist die tatsächliche Struktur des Chlorats eine Hybridstruktur, die alle Cl-O-Bindung mit derselben Länge aufweist. Darüber hinaus ist das Chloratom hier hypervalent. Dies bedeutet, dass das Chloratom mehr als acht Elektronen um es herum hat.
Bei der Betrachtung der Zubereitung können wir im Labor Chlorate produzieren, indem wir Chlor zu heißen Hydroxiden hinzufügen, i.e. Koh. In der industriellen Skala können wir es aus der Elektrolyse von wässrigem Natriumchlorid produzieren.
Was ist Perchlorat?
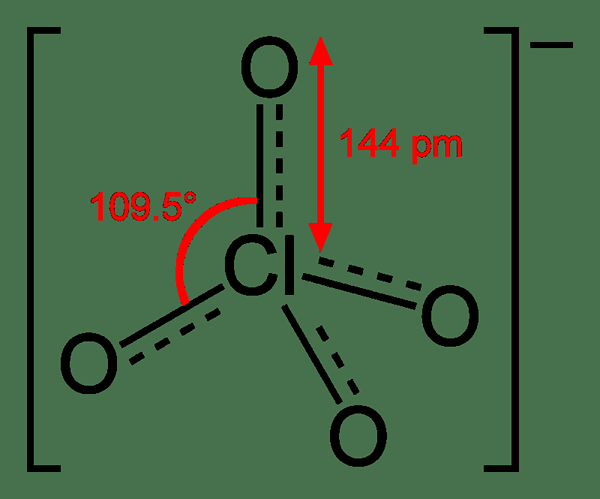
Perchlorat ist ein Anion mit der chemischen Formel CLO4-. Es stammt aus Perchlorsäure. Im Allgemeinen kann sich dieser Begriff auf eine Verbindung beziehen, die Perchloratanion enthält. Der Oxidationszustand des Chorinatoms in dieser Verbindung beträgt +7. Es ist die am wenigsten reaktive Form unter anderen Chloraten. Die Geometrie dieses Ions ist tetraedrisch.

Meistens existiert Verbindungen, die dieses Anion enthalten. Dieses Anion bildet sich, wenn Perchloratverbindungen in Wasser dissoziieren. In der industriellen Skala können wir dieses Ion über die Elektrolysemethode produzieren. Hier tritt eine Oxidation von wässrigem Natriumchlorat auf.
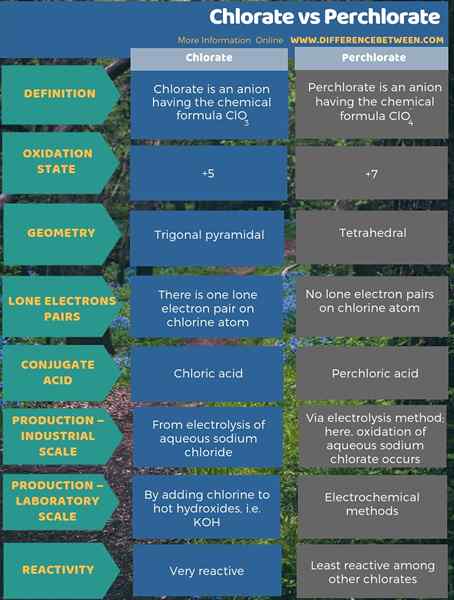
Was ist der Unterschied zwischen Chlorat und Perchlorat?
Der Schlüsselunterschied zwischen Chlorat und Perchlorat besteht darin. Darüber hinaus beträgt der Oxidationszustand des Chloratoms im Chlorat +5 und der Oxidationszustand von Perchlorat +7. Wenn man die Geometrie dieser Anionen berücksichtigt.
Zusammenfassung -Chlorat gegen Perchlorat
Chlorat und Perchlorat sind im Grunde genommen Oxyanionen des Chors. Der Schlüsselunterschied zwischen Chlorat und Perchlorat besteht darin.
Referenz:
1. „Chlorat.”Wikipedia, Wikimedia Foundation, 27. August. 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Chlorate-2d" von Benjah-BMM27-eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Perchlorat-2D-Dimensionen" von Benjah-BMM27-eigene Arbeit (Public Domain) über Commons Wikimedia


