Unterschied zwischen Chloroform und Dichlormethan
Der Schlüsselunterschied Zwischen Chloroform und Dichlormethan ist das Chloroform enthält drei Chloratome pro Molekül, während Dichlormethan zwei Chloratome pro Molekül enthält.
Chloroform und Dichlormethan sind Organochlormoleküle, die ähnliche Atomität und eine ähnliche Geometrie oder molekulare Form enthalten.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Chloroform
3. Was ist Dichlormethan
4. Seite an Seitenvergleich - Chloroform gegen Dichlormethan in tabellarischer Form
5. Zusammenfassung
Was ist Chloroform?
Chloroform ist eine organische Verbindung mit der chemischen Formel -CHCL3. Es ist nützlich als starkes Anästhetikum. Der IUPAC -Name dieser Verbindung ist Trichlormethan. Es ist eine farblose und dichte Flüssigkeit, die einen süßen Geruch hat. Chloroform wird in großem Maßstab als Vorläufer für die Herstellung von PTFE erzeugt. Darüber hinaus ist der größte Teil des Chloroforms in der Umwelt (etwa 90%) auf Emissionen natürlicher Herkunft zurückzuführen. Zum Beispiel produzieren viele Arten von Seetang und Pilzen diese Verbindung und füllen sie in die Atmosphäre frei.
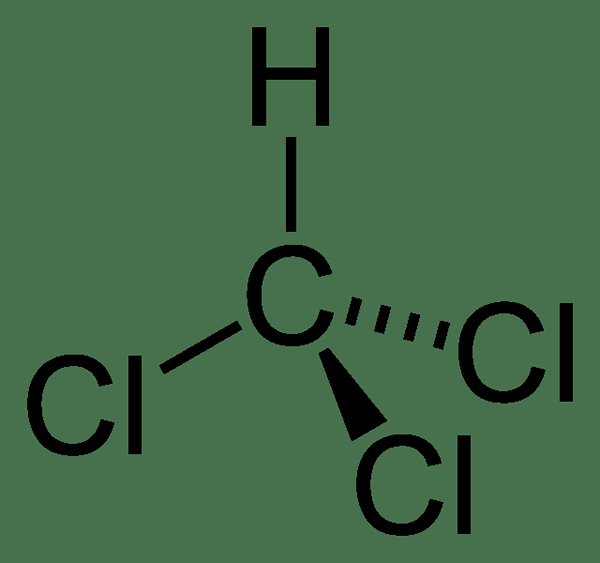
Die Molmasse von Chloroform beträgt 119.37 g/mol, und es erscheint bei Raumtemperatur als farblose Flüssigkeit. Diese Flüssigkeit hat einen schweren ätherischen Geruch. Sein Schmelzpunkt beträgt –63.5 ° C und der Siedepunkt ist 61.15 ° C. Darüber hinaus zersetzt sich Chloroform bei 450 ° C. Dieses Molekül hat eine tetraedrische Geometrie.

Abbildung 01: Chemische Struktur von Chloroform
Im industriellen Maßstab können wir diese Verbindung durch Erhitzen einer Mischung aus Chlor und Chlormethan produzieren (oder manchmal verwenden wir auch Methan). Nach dem Erhitzen tritt bei 400-500 ° C eine free radikale Halogenierung auf. Dies bildet chlorierte Verbindungen von Chlormethan (oder Methan), die Chloroforms ergeben. Diese Verbindung kann sich einer weiteren Chlorierung unterziehen und Kohlenstofftetrachlorid bilden. Das Endprodukt dieser Reaktion ist jedoch eine Mischung aus Chlormethanen, die wir durch Destillation trennen können, um Chloroform zu erhalten.
Es gibt viele Anwendungen von Chloroform. Es ist als Lösungsmittel nützlich, da das Wasserstoffatom in diesem Molekül eine Wasserstoffbrückenbindung durchlaufen kann. Wir können es auch als Reagenz für viele chemische Reaktionen verwenden. Beispiel: Als Quelle der Dichlorocarbän -Gruppe. Noch wichtiger ist, dass Chloroform für seine Anästhesiemeigenschaften bekannt ist.
Was ist Dichlormethan?
Dichlormethan ist eine organische Verbindung mit der chemischen Formel CH2Cl2. Es ist eine Organochlorverbindung, und wir können sie als DCM bezeichnen. Diese Verbindung tritt als flüchtige, farblose Flüssigkeit auf, die aus einem chloroformenähnlichen süßen Geruch besteht. Dichlormethan ist hauptsächlich als Lösungsmittel nützlich. Diese Flüssigkeit ist nicht mit Wasser mischbar, obwohl es sich um eine polare Verbindung handelt. Es kann sich jedoch mit vielen anderen organischen Lösungsmitteln vermischen.
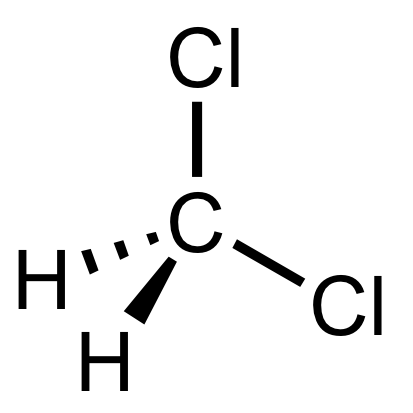
Abbildung 02: Chemische Struktur von Dichlormethan
Es gibt einige natürliche Dichlormethan -Quellen, darunter ozeanische Quellen, Makroalgen, Feuchtgebiete und Vulkane. Wir können jedoch beobachten, dass der größte Teil des Dichlormethans in der Umwelt auf industrielle Emissionen zurückzuführen ist. Wir können Dichlormethan durch die Behandlung von Chlormethan oder Methan mit Chlorgas bei hohen Temperaturen produzieren.
Was ist der Unterschied zwischen Chloroform und Dichlormethan?
Chloroform und Dichlormethan sind Organochlormoleküle. Der Schlüsselunterschied zwischen Chloroform und Dichlormethan besteht darin. Darüber hinaus kann Chloroform durch Erhitzen einer Mischung aus Chlormethan erzeugt werden, während Dichlormethan durch die Behandlung von Chlormethan oder Methan mit Chlorgas bei hohen Temperaturen erzeugt werden kann.
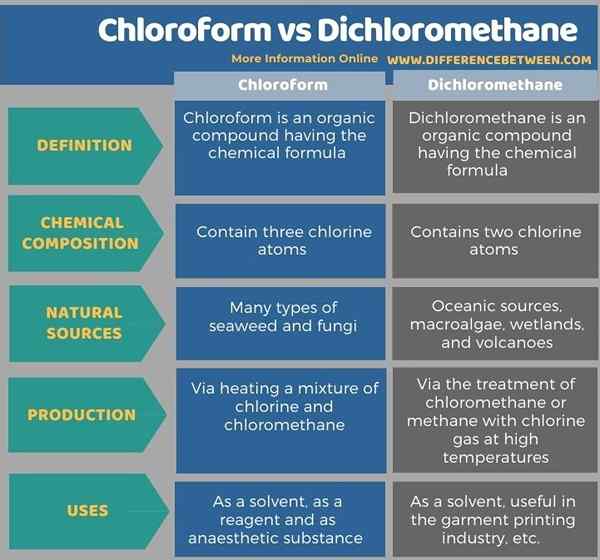
Die folgende Infografik listet die Unterschiede zwischen Chloroform und Dichlormethan in tabellarischer Form auf.
Zusammenfassung -Chloroform gegen Dichlormethan
Kurz gesagt, Chloroform und Dichlormethan sind Organochlormoleküle. Der Schlüsselunterschied zwischen Chloroform und Dichlormethan besteht darin.
Referenz:
1. "Chloroform.” Nationales Zentrum für Biotechnologie Information. Pubchem Compound -Datenbank, U.S. National Library of Medicine, hier verfügbar.
Bild mit freundlicher Genehmigung:
1. "Chloroform angezeigt" von Benjah -BMM27, Vektorisierung: Fvasconcellos - von FVasconcellos (Public Domain) über Commons Wikimedia umgewandelt
2. "Dichlormethanmolekularstruktur" von Ohnodoctor - gezeichnet mit Chemdraw (CC BY -SA 4.0) über Commons Wikimedia


