Unterschied zwischen kovalenter Bindung und Dativbindung
Der Schlüsselunterschied zwischen kovalenter Bindung und Dativbindung ist, dass die Kovalente Bindung bildet sich, wenn ungepaarte Elektronen zweier Atome miteinander assoziieren, während die Dativbindung bildet, wenn ein Atom eines seiner Elektronenpaare an ein anderes Atom spendet.
Obwohl die Dativbindung wie eine kovalente Bindung aussieht, unterscheiden sie sich voneinander, wenn wir die Bildung der Bindung betrachten. Es gibt jedoch keinen Unterschied zwischen kovalenter Bindung und Dativbindung nach ihrer Bildung. Daher nennen wir normalerweise die Dativbindung als kovalente Bindung, die nicht falsch ist.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist kovalente Bindung
3. Was ist Dative Bond
4. Seite an Seitenvergleich - kovalente Bindung gegen Dativbindung in tabellarischer Form
5. Zusammenfassung
Was ist kovalente Bindung?
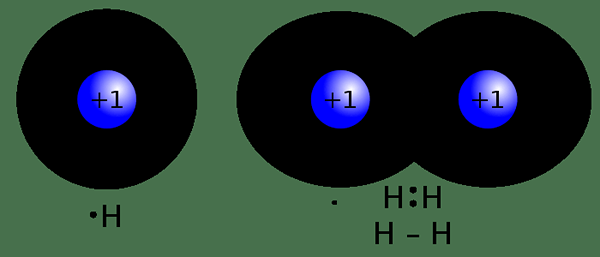
Eine kovalente Bindung ist eine Form der chemischen Bindung, die sich bildet, wenn zwei Atome ein Elektronenpaar teilen. Wir nennen es eine "molekulare Bindung". Die gemeinsam genutzten Elektronen sind „gemeinsame Paare“ oder „Bindungspaare“. Eine kovalente Bindung, die sich aufgrund des stabilen Gleichgewichts der attraktiven und abstoßenden Kräfte zwischen Atomen bildet, wenn sie Elektronen teilen. Diese Elektronenfreigabe ermöglicht es jedem Atom, das Äquivalent einer vollen Außenhülle zu haben. Diese Art von Bindungsformen bildet zwischen zwei nichtmetallischen Atomen mit nahezu ähnlichen Elektronegativitätswerten oder zwischen einem Elektron und einem positiv geladenen Metallion.

Abbildung 01: Bildung einer kovalenten Bindung zwischen zwei Wasserstoffatomen
Kovalente Bindungen sind hauptsächlich von zwei Arten; Sie sind polare Bindungen und unpolare Bindungen. Es gibt polare Bindungen zwischen zwei Atomen mit einem Unterschied zwischen ihren Elektronegativitätswerten im Bereich von 0.4 bis 1.7. Eine unpolare Bindung bildet, wenn dieser Unterschied niedriger als 0 ist.4. Dies liegt daran.
Es gibt drei Haupttypen kovalenter Bindungen gemäß der Anzahl der Elektronenpaare, die zwischen zwei Atomen geteilt werden. Es handelt sich um Einzelbindungen, an denen ein Elektronenpaar beteiligt ist, Doppelbindungen, an denen zwei Elektronenpaare beteiligt sind, und eine Dreifachbindung, an der drei Elektronenpaare beteiligt sind.
Was ist Dative Bond?
Eine Dativbindung ist eine Art kovalenter Bindung, die sich bildet, wenn ein Atom sein Elektronenpaar an ein anderes Atom spendet. Nach der Bildung der Bindung sieht es genauso aus wie eine kovalente Bindung. Dies liegt daran, dass beide Atome das gleiche Elektronenpaar wie das Bondpaar teilen.
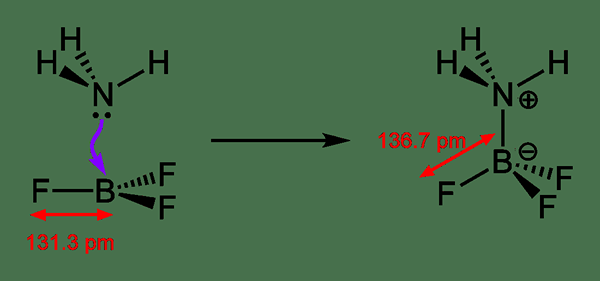
Abbildung 02: Bildung einer Dativbindung
Synonyme für diese Bindung sind "Dipolare Bindung" und "Koordinatenbindung". Das häufigste Beispiel sind die Bindungen in Koordinationskomplexen. Dort binden die Metallionen über diese Koordinatenbindungen mit Liganden mit Liganden.
Was ist der Unterschied zwischen kovalenter Bindung und Dativbindung?
Eine kovalente Bindung ist eine Form der chemischen Bindung, die sich bildet, wenn zwei Atome ein Elektronenpaar teilen. Eine Dativbindung ist eine Art kovalenter Bindung, die sich bildet, wenn ein Atom sein Elektronenpaar an ein anderes Atom spendet. Sie unterscheiden sich je nach Art und Weise, wie sie sich bilden. Daher besteht der Hauptunterschied zwischen kovalenter Bindung und dativem Bind.
Die folgende Infografik stellt den Unterschied zwischen kovalenter Bindung und dativer Bindung in tabellarischer Form dar.
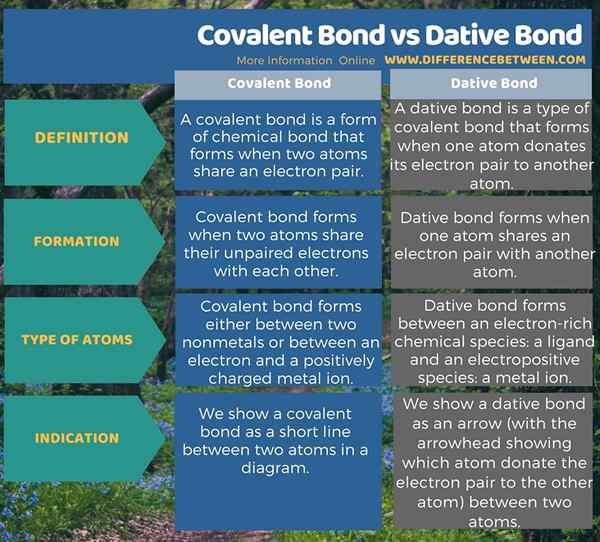
Zusammenfassung -kovalente Bindung gegen Dativbindung
Nach der Bildung der Bindung scheint sowohl die kovalente Bindung als auch die Dativbindung ähnlich zu sein. Sie unterscheiden sich jedoch je nach Art und Weise, wie sie sich bilden. Der Unterschied zwischen kovalenter Bindung und dativem Bind.
Referenz:
1. Helmenstine, Anne Marie, ph.D. „Kovalente Bindungsdefinition.”Thoughtco, Jun. 22, 2018. Hier verfügbar
2. Helmenstine, Anne Marie, ph.D. „Definition der Dativbindungen (Koordinatenbindung).”Thoughtco, Jun. 22, 2018. Hier verfügbar
Bild mit freundlicher Genehmigung:
1.”Kovalenter Bindung Wasserstoff” von Jacek FH - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia
2.”NH3-BF3-Adduct-Bond-Länge-2D” von Ben Mills-eigene Arbeit, (Public Domain) über Commons Wikimedia


