Unterschied zwischen Verdünnung und Verdünnungsfaktor

Schlüsselunterschied - Verdünnung im Verzugsfaktor
Verdünnung und Verdünnungsfaktor sind häufige Begriffe, die für Berechnungen in der analytischen Chemie verwendet werden. Die Verdünnung bezieht sich auf die Abnahme der Konzentration eines bestimmten gelösten Stoffes in einer Lösung. Dieser Begriff kann verwendet werden, um sowohl Flüssigkeiten als auch Gase zu beschreiben. Der Verdünnungsfaktor ist ein Maß für die Verdünnung; Es beschreibt das Ausmaß der Verdünnung. Der Schlüsselunterschied zwischen Verdünnung und Verdünnungsfaktor ist das Verdünnung einer Lösung ist die Abnahme der Konzentration von gelösten Stoffen in dieser Lösung, während der Verdünnungsfaktor das Verhältnis zwischen dem endgültigen Volumen und dem anfänglichen Volumen der Lösung ist.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Verdünnung
3. Was ist Verdünnungsfaktor
4. Seite für Seitenvergleich -Verdünnung gegen Verdünnungsfaktor in tabellarischer Form
5. Zusammenfassung
Was ist Verdünnung?
Verdünnung einer Lösung ist die Abnahme der Konzentration von gelösten Stoffen in dieser Lösung. Eine Lösung besteht aus einem Lösungsmittel, das gelöste gelöste Stoffe darin gelöst ist. Die Konzentration dieser gelösten Stoffe wird als Molarität oder Molalität angegeben. Molarität ist die Menge an gelösten gelösten Stoffe in einem Lösungsvolumen (angegeben durch die Einheit mol/l). Molalität ist die Masse des gelösten Stoffes in einem Einheitsvolumen (angegeben durch die Einheit kg/l). Wenn die Konzentration des gelösten Stoffes in dieser Lösung verringert wird, wird sie als verdünnte Lösung bezeichnet.
Eine Verdünnung erfolgt einfach, indem einfach mehr Lösungsmittel zur Lösung hinzugefügt wird und den gelösten Gehalt konstant hält. Beispielsweise kann eine wässrige Lösung, die Natriumchlorid (NaCl) enthält. Wenn der gelöste Stoff eine farbige Verbindung ist, verblasst die Farbe der Lösung, wenn die Lösung verdünnt wird.

Abbildung 1: Die Farbe wird beim Verdünnen verblasst
Endkonzentrationsberechnung
Die Endkonzentration der Lösung kann unter Verwendung der folgenden Beziehung bestimmt werden.
C1v1 = C2v2
C1 ist die anfängliche Konzentration
V1 ist das Anfangsvolumen
C2 ist die Endkonzentration
V2 ist das endgültige Volumen der Lösung.
Beispiel: Eine wässrige Lösung von KCL enthält 2.0 Mol KCL in 0.2 l Wasser. Was wäre die Endkonzentration der KCL -Lösung, wenn Wasser (400 ml) zugesetzt wird?
Anfängliche Konzentration von kcl (c1) = 2.0 mol/0.2l = 10 mol/l
Anfangsvolumen der Lösung (v1) = 0.2 l
Endgültiges Volumen der Lösung (v2) = 0.2 l + 0.4 l = 0.6 l
Die Endkonzentration der Lösung (C2) kann unter Verwendung:
C1v1 = C2v2
10 mol/l x 0.2 l = C2 x 0.6 l
C2 = 2 mol / 0.6 l = 3.33 mol/l
Was ist Verdünnungsfaktor?
Verdünnungsfaktor (auch bekannt als der Verdünnungsverhältnis) ist das Verhältnis zwischen dem endgültigen Volumen und dem anfänglichen Volumen der Lösung. Das endgültige Volumen ist das Volumen der Lösung nach der Verdünnung. Das anfängliche Volumen ist das Volumen der Lösung vor dem Verdünnung oder das Volumen der für die Verdünnung verwendeten ursprünglichen Lösung. Diese Beziehung kann auch zusammen mit der Masse des gelösten Stoffes verwendet werden.
Verdünnungsfaktorberechnung
Verdünnungsfaktor = Endvolumen (v2) / Anfangsvolumen (v1)
Beispiel: Verdünnung von 200 ml KMNO4 wässrige Lösung durch Zugabe von 200 ml Wasser,
Verdünnungsfaktor = (200 ml + 200 ml) / 200 ml
= 400 ml /200 ml
= 2
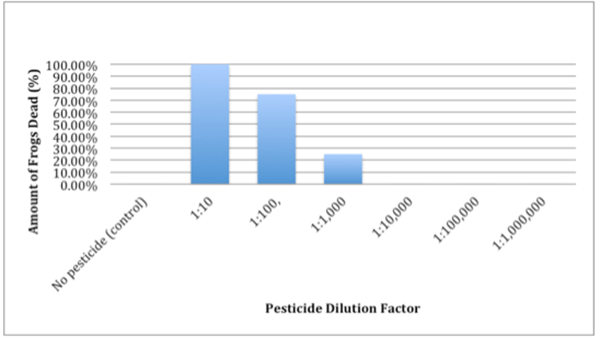
Abbildung 02: Verdünnungsfaktorgrafik
Das obige Diagramm zeigt eine Grafik aus einer Forschung, in der der Tod von Fröschen zusammen mit der Verdünnung der Pestizide zu einem Ökosystem berechnet wird.
Was ist der Unterschied zwischen Verdünnungs- und Verdünnungsfaktor?
Verdünnung gegen Verdünnungfaktor | |
| Verdünnung einer Lösung ist die Abnahme der Konzentration von gelösten Stoffen in dieser Lösung. | Verdünnungsfaktor (Verdünnungsverhältnis) ist das Verhältnis zwischen dem endgültigen Volumen und dem anfänglichen Volumen der Lösung. |
| Konzept | |
| Die Verdünnung ist die Abnahme der Konzentration. | Verdünnungsfaktor ist ein Maß für die Verdünnung. |
| Festlegung | |
| Die Verdünnung wird durch die Gleichung C1V1 = C2v2 bestimmt. | Der Verdünnungsfaktor wird bestimmt, indem das endgültige Volumen der Lösung aus dem Anfangsvolumen geteilt wird. |
| Einheit | |
| Die Verdünnung gibt die Endkonzentration in mol/l Einheiten an. | Der Verdünnungsfaktor ist unitlos. |
Zusammenfassung -Verdünnung gegen den Verdünnungsfaktor
Verdünnung und Verdünnungsfaktor sind sehr häufige Begriffe in der Chemie. Verdünnungsfaktor ist das Maß für die Verdünnung. Der Schlüsselunterschied zwischen Verdünnung und Verdünnungsfaktor besteht darin.
Referenz:
1. „Verdünnung (Gleichung).”Wikipedia, Wikimedia Foundation, 12. Februar. 2018, hier erhältlich.
2. „Verdünnungen: Erklärungen und Beispiele.Quansys Biosciences, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Diffusionsverdünnung" von Tess Watson (CC von 2.0) über Flickr
2. "Abbildung 1 Xenopus laevis" von Krmeyer0717 - eigene Arbeit (CC BY -SA 4.0) über Commons Wikimedia


