Unterschied zwischen elektronischer und ionischer Leitung
Der Schlüsselunterschied Zwischen elektronischer und ionischer Leitung ist das Die elektronische Leitung ist die Bewegung von Elektronen von einem Ort zum anderen, während eine ionische Leitung die Bewegung von Ionen von einem Ort zum anderen ist.
Die Laufzeit leitet sich auf die Energieübertragung durch eine Substanz. Hier kann die Energie in verschiedenen Formen wie Wärme und Strom übertragen werden. Elektronische Leitung und ionische Leitung sind zwei Formen von Energieübertragungsmethoden, die basierend auf dem Leitungsmedium eingestuft werden.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist elektronische Leitung
3. Was ist eine ionische Leitung
4. Seite an Seitenvergleich - elektronische vs ionische Leitung in tabellarischer Form
5. Zusammenfassung
Was ist elektronische Leitung?
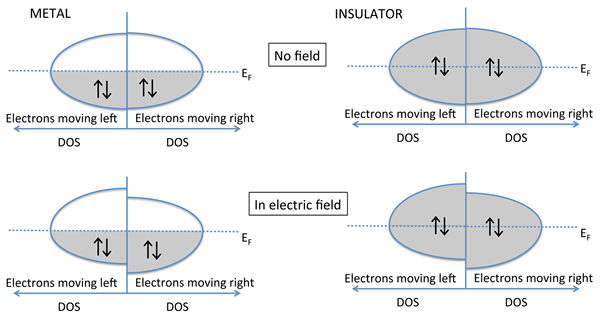
Elektronische Leitung ist der Prozess der Energieübertragung in Form eines elektrischen Stroms. Hier ist die Leitungsmethode die Elektronenbewegung. Ein Elektron in einem System kann jedoch nicht zu dieser Leitungsmethode beitragen. Elektronen müssen sich in einem freien Zustand befinden, um von einem Ort zum anderen zu wechseln. Die inneren Schalenelektronen von Atomen können sich nicht bewegen. Eine weitere Anforderung ist das Vorhandensein eines elektrischen Feldes, das die Bewegung freier Elektronen verursachen kann.

Abbildung 01: Leitung von Elektronen
Elektronen, die in der Lage sind, sich zu leiten, werden als „Leitungselektronen“ bezeichnet. Diese Elektronen sind nicht fest an ein Atom oder ein Molekül gebunden. Diese freien Elektronen können vom Orbital eines Atoms zu einem Orbital eines benachbarten Atoms springen. Insgesamt sind diese Elektronen jedoch an den Leiter gebunden. Die Bewegung von Elektronen beginnt mit der Anwendung eines elektrischen Feldes. Das elektrische Feld gibt den Elektronen eine Richtung, um sich zu bewegen.
Was ist eine ionische Leitung?
Die Ionenleitung ist der Prozess der Energieübertragung über die Bewegung ionischer Spezies. Während der ionischen Leitung bewegen sich verschiedene ionische Arten nach einem ionischen Gradienten von einem Ort zu einem anderen Ort. Ein Ion ist eine geladene Art; Es kann entweder positiv aufgeladen oder negativ aufgeladen werden. Positiv geladene Ionen bewegen sich negativ aufgeladene Orte und umgekehrt. Die Tendenz einer Substanz zur ionischen Leitung wird als ionische Leitfähigkeit gemessen. Es wird durch λ bezeichnet.
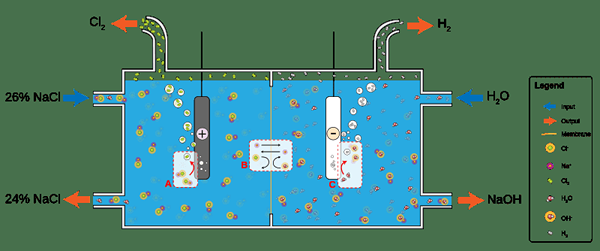
Abbildung 02: Eine Membranzelle, die bei der Elektrolyse der Salzlösung verwendet wird, bei der eine ionische Leitung durch die Membran in der Mitte erfolgt, um die ionischen Konzentrationen stabil zu halten.
Meistens verwenden wir den Begriff ionische Leitung in Bezug auf Kristallgitter. Hier bezieht sich die ionische Leitung auf die Bewegung von Ionen von einem Defekt zum anderen im Kristallgitter. Der Prozess der Leitung von Ionen ist ein Strommechanismus, bei dem Energie von einem Ort zum anderen weitergegeben wird.
Was ist der Unterschied zwischen elektronischer und ionischer Leitung?
Elektronische Leitung und ionische Leitung sind zwei Formen von Energieübertragungsmethoden, die basierend auf dem Leitungsmedium eingestuft werden. Der Hauptunterschied zwischen elektronischer und ionischer Leitung besteht darin, dass die elektronische Leitung die Bewegung von Elektronen von einem Ort zum anderen ist, während die ionische Leitung die Bewegung von Ionen von einem Ort zum anderen ist.
Nachfolgend finden Sie eine Zusammenfassung der Differenz zwischen elektronischer und ionischer Leitung.
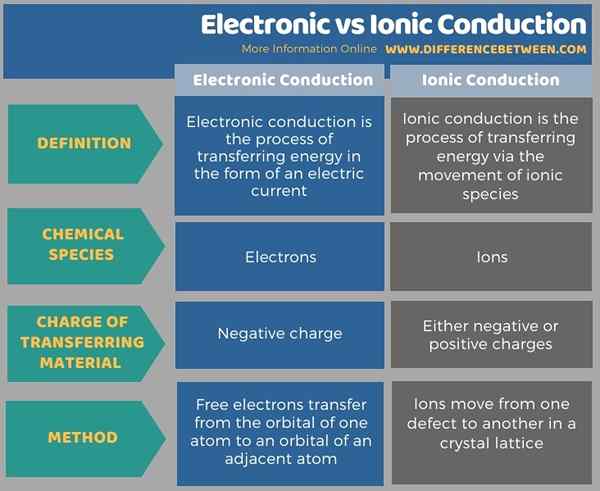
Zusammenfassung -elektronische gegen ionische Leitung
Elektronische Leitung und ionische Leitung sind zwei Formen von Energieübertragungsmethoden, die basierend auf dem Leitungsmedium eingestuft werden. Der Hauptunterschied zwischen elektronischer und ionischer Leitung besteht darin, dass die elektronische Leitung die Bewegung von Elektronen von einem Ort zum anderen ist, während die ionische Leitung die Bewegung von Ionen von einem Ort zum anderen ist.
Referenz:
1. „Metallische Leitung.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., Hier verfügbar.
2. „Elektrische Leitung.”ScienceDaily, Sciencedaily, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Leitung E gegen dos" von TEM5PSU - eigene Arbeit (CC BY -SA 4.0) über Commons Wikimedia
2. "Chloralkali -Membran" von Jkwchui - basierend auf * Bommaraju, Tilak V.; Orosz, Paul J.; Sokol, Elizabeth a.(2007). „Sole -Elektrolyse.Elektrochemie Enzyklopädie. Cleveland: Case Western Rsserve University.MSN ENCARTA. „Chloralkali -Elektrolyse.Archiviert 2009-10-31 (CC BY-SA 3.0) über Commons Wikimedia


