Unterschied zwischen galvanischen Serien und elektrochemischen Serien

Der Schlüsselunterschied Zwischen galvanischen Serien und elektrochemischen Serien befindet sich das Galvanische Serie zeigt die Reihenfolge des Adels von Metallen und Halbmetallen, während die elektrochemische Serie die Reihenfolge der Standard-Elektrodenpotentiale chemischer Elemente zeigt.
Die galvanischen Serien und elektrochemische Serien sind zwei verschiedene Listen, die eine Anordnung chemischer Elemente nach ihren Eigenschaften zeigen. Galvanische Serie zeigt die Order des Adels, der die Resistenz gegen Korrosion und Oxidation in feuchter Luft ist. Die elektrochemische Zelle hingegen zeigt die Standard -Elektrodenpotentiale chemischer Elemente in Ordnung.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist galvanische Serie
3. Was ist elektrochemische Serie
4. Nebenseitiger Vergleich - Galvanische Serie gegen elektrochemische Serie in tabellarischer Form
5. Zusammenfassung
Was ist galvanische Serie?
Die Galvanic-Serie ist eine Anordnung von Metallen und Halbmetallen nach ihrem Adel. Adel ist die Resistenz gegen Korrosion und Oxidation in Gegenwart feuchter Luft. Diese Liste enthält Metalle, Halbmetalle und Legierungen, da nur diese Materialien Korrosion unterzogen werden können. Die Liste ist gemäß den relativen Potentialen dieser Materialien in einer bestimmten Umgebung angeordnet. Im Allgemeinen ist die Umgebung, die wir betrachten, Meerwasser.

Abbildung 01: Galvanische Serie von edlen Metallen
Das Prinzip hinter der Anordnung dieser Liste ist, dass, wenn wir zwei Elektroden in einen Elektrolyten eintauchen und die Elektroden an einen externen Leiter anschließen, das weniger edle Material galvanische Korrosion erfährt. Hier bestimmt der Elektrolyte die Korrosionsrate. Die Eigenschaften dieser Serie sind wie folgt:
• Es zeigt die relativen Positionen von Metallen und Legierungen anstelle von Potentialen an.
• Die praktische Messung des Korrosionspotentials im Gleichgewicht ist die Grundlage für die Anordnung der Serie.
• Laut dieser Serie können wir zwei Legierungen ohne Korrosion verbinden
Es gibt jedoch auch einige Einschränkungen bei der Verwendung dieser Serie.
• Jede Umgebung erfordert eine andere galvanische Serie, da sie von der Umgebung abhängt
• Darüber hinaus hängt die galvanische Korrosion vom Ausmaß der Polarisation von Metallen und Legierungen ab. Somit liefert die Serie möglicherweise nicht genügend Informationen zur galvanischen Korrosion.
Was ist elektrochemische Serie?
Elektrochemische Serien sind eine Liste chemischer Elemente, die die Reihenfolge der Standard -Elektrodenpotentiale darstellt. Es liefert genügend Informationen über die relative Reaktivität von Metallen in wässrigen Lösungen unter Standardbedingungen. Ein weiterer gebräuchlicher Name für diese Serie ist die „Aktivitätsreihe“. Darüber hinaus listet diese Serie Metalle auf, um die Reaktivität zu verringern.
An der Spitze der Serie verfügt es über Alkali -Metalle und alkalische Erdmetalle. Diese sind reaktiver und oxidieren Sie leicht als die Metalle am Boden. Darüber hinaus reagieren sie leicht auf Verbindungen. Diese Metalle werden daher als "aktive Metalle" bezeichnet.
Am Ende der Serie befinden sich Übergangsmetalle. Sie sind relativ sehr stabil und bilden keine Verbindungen leicht. Beispiele sind Kupfer, Gold, Silber usw. Aufgrund ihrer geringen Reaktivität verwenden wir sie oft, um Münzen, Schmuck usw. herzustellen.; Wir nennen sie "edle Metalle".
Darüber hinaus gibt diese Serie das Elektrodenpotential dieser chemischen Elemente an, und die Liste wird gemäß den Standard -Elektrodenpotentialen angeordnet. Wir können diesen Wert messen, indem wir das bestimmte Metall als Kathode und Standard -Wasserstoffelektrode als Anode nehmen.
Was ist der Unterschied zwischen galvanischen Serien und elektrochemischen Serien?
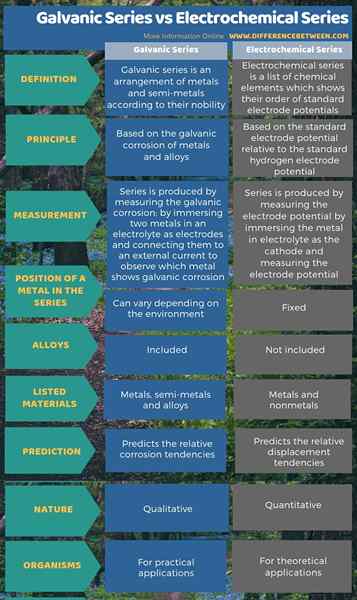
Der wichtigste Unterschied zwischen galvanischen Serien und elektrochemischen Serien besteht darin, dass die Galvan-Serie die Reihenfolge der Adelsöder von Metallen und Halbmetallen zeigt, während die elektrochemische Serie die Reihenfolge der Standard-Elektrodenpotentiale chemischer Elemente zeigt. Bei der Betrachtung des Prinzips der Erstellung jeder Liste stammt die galvanische Serie aus der galvanischen Korrosion von Metallen und Legierungen, während die elektrochemische Serie aus dem Standard -Elektrodenpotential relativ zum Standard -Wasserstoffelektrodenpotential stammt.
Darüber hinaus kann die Position eines Metalls in galvanischen Serien je nach Umwelt variieren. In der elektrochemischen Reihe hat es jedoch eine feste Position. Ein weiterer Unterschied zwischen galvanischen Serien und elektrochemischen Serien besteht darin, dass galvanische Serien für praktische Anwendungen geeignet sind, während die elektrochemische Serie für theoretische Anwendungen geeignet ist.
Zusammenfassung -Galvanische Serie gegen elektrochemische Serie
Der wichtigste Unterschied zwischen galvanischen Serien und elektrochemischen Serien besteht darin, dass die Galvan-Serie die Reihenfolge der Adelsöder von Metallen und Halbmetallen zeigt, während die elektrochemische Serie die Reihenfolge der Standard-Elektrodenpotentiale chemischer Elemente zeigt.
Referenz:
1. „Elektrochemische Serie: Erklärung und ihre Anwendungen.Wissen neu definieren, 4. Dezember. 2018, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Galvanische Serie Noble Metals" von Tugsataydin - eigener Arbeit (CC BY -SA 4.0) über Commons Wikimedia


