Unterschied zwischen Glutamin und L-Glutamin

Glutamin gegen L-Glutamin
Aminosäure ist ein einfaches Molekül, das mit C, H, O, N gebildet wird und kann s sein. Es hat die folgende allgemeine Struktur.
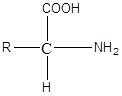
Es gibt ungefähr 20 häufige Aminosäuren. Alle Aminosäuren haben einen -cooh, -nh2 Gruppen und ein -h an einen Kohlenstoff gebunden. Der Kohlenstoff ist ein chiraler Kohlenstoff, und Alpha -Aminosäuren sind in der biologischen Welt die wichtigsten. D-Aminosäuren sind in Proteinen nicht und nicht Teil des Metabolismus höherer Organismen gefunden. Einige sind jedoch wichtig für die Struktur und den Stoffwechsel niedrigerer Lebensformen. Zusätzlich zu häufigen Aminosäuren gibt es eine Reihe von nicht-Protein abgeleiteten Aminosäuren, von denen viele entweder metabolische Zwischenprodukte oder Teile von Nicht-Protein-Biomolekülen (Ornithin, Citrullin) sind. Die R -Gruppe unterscheidet sich von Aminosäure zu Aminosäure. Die einfachste Aminosäure, bei der R -Gruppe H ist, ist Glycin. Nach der R -Gruppe können Aminosäuren in aliphatische, aromatische, nicht polare, polare, positiv geladene, negativ geladene oder polar ungeladene usw. kategorisiert werden. Aminosäuren, die als Zwitterionen im physiologischen pH 7 vorhanden sind.4. Aminosäuren sind die Bausteine von Proteinen. Wenn sich zwei Aminosäuren zusammenschließen, um ein Dipeptid zu bilden, findet die Kombination im -NH statt2 Gruppe einer Aminosäure mit -COOH-Gruppe einer anderen Aminosäure. Ein Wassermolekül wird entfernt und die gebildete Bindung wird als Peptidbindung bezeichnet.
Glutamin
Glutamin ist eine der wichtigsten Aminosäuren, die nicht wesentlich sind. Es wird als Gln abgekürzt. Die R -Gruppe hat eine zusätzliche Amingruppe. Es hängt mit der Struktur von Glutaminsäure zusammen, außer dass Glutamin eine Amid -Seitenkette anstelle der Hydroxylgruppe von Glutaminsäure hat. Glutamin hat die folgende Struktur.
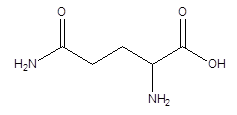
Glutamin ist die am häufigsten vorkommende freie Aminosäure im menschlichen Blut. Die Blutkonzentration beträgt etwa 500-900 µmol/l. Glutamin wird von den CAA- und CAG -Codons erzeugt. Es wird durch das Glutamat -Synthetase -Enzym aus Glutamat und Ammoniak synthetisiert. Es wird hauptsächlich in den Muskeln produziert, und kleine Mengen werden aus Lungen und Gehirn freigesetzt.
Glutamin hat verschiedene Funktionen in den biologischen Systemen. Es beteiligt sich an der Bildung von Proteinen, wie es jede andere Aminosäure tun würde. Glutamin ist verantwortlich für die Regulierung des Säure -Basen -Gleichgewichts in den Nieren. Es fungiert sowohl als Stickstoff- und Kohlenstoffquelle als auch als Energiequelle nach Glukose. Das aus den Stoffwechselaktivitäten erzeugte Ammoniak ist für Zellen giftig, wenn es frei ist. Glutamin ist eine ungiftige Methode, um Ammoniak im Blut zu transportieren.
L-Glutamin
Glutamin ist ein chirales Molekül, das nicht übereinstimmbare Spiegelbilder aufweist. Daher gibt es zwei Isomere zu Glutamin als L-Glutamin und D-Glutamin. Unter beiden ist L-Glutamin im Körper reichlich vorhanden und beteiligt sich an verschiedenen Funktionen.
Rindfleisch, Hühnchen, Eier, Fisch, Milch, Kohl, Rüben, Bohnen, Spinat und Petersilie sind diätetische Quellen für L-Glutamin.
Glutamin gegen L-Glutamin
- L-Glutamin und D-Glutamin sind zwei Isomere Glutamin.
- L-Glutamin ist in Organismen reichlich vorhanden als D-Glutamin.
- L-Glutamin wird für Zellkulturen als Nahrungsergänzungsmittel verwendet.


