Unterschied zwischen H2S und SO2
Der Schlüsselunterschied Zwischen H2S und SO2 ist das H2S hat den Geruch eines faulen Eies, während SO2 den Geruch eines verbrannten Matchs hat.
Sowohl H2S als auch SO2 sind gasförmige Verbindungen bei Raumtemperatur. Diese Verbindungen enthalten Schwefelatome. H2S ist ein Schwefelhydrid, während SO2 ein Schwefeloxid ist. Darüber hinaus haben diese beiden Gase einen scharfen Geruch.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist H2S
3. Was ist SO2
4. Seite an Seite Vergleich -H2S vs SO2 in tabellarischer Form
5. Zusammenfassung
Was ist H2S?
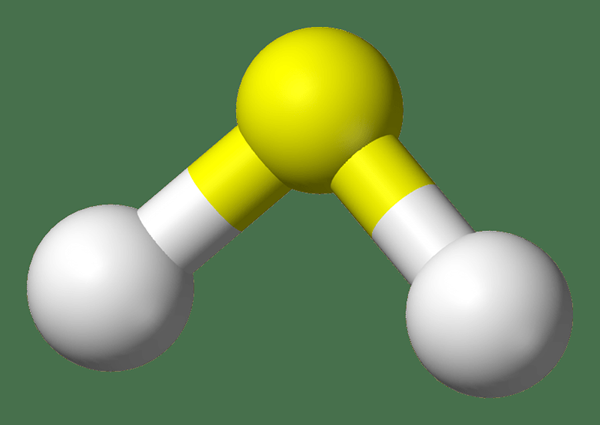
H2S ist Wasserstoffsulfid. Es ist ein Gas bei Raumtemperatur, der den Geruch eines faulen Eies hat. Daher hat es einen scharfen und irritierenden Geruch. Dieses Gas ist sehr giftig. Darüber hinaus ist es auch ätzend und brennbar. Daher müssen wir sorgfältig damit umgehen. Die Molmasse von H2S beträgt 38.09 g/mol. Es erscheint als farbloses Gas.
Das H2S -Gas ist leicht dichter als die normale atmosphärische Luft. Eine Mischung aus Luft und H2S kann jedoch explosive Reaktionen verursachen. Darüber hinaus brennt dieses Gas in Luft mit einer blauen Flamme nach Vorhandensein von Sauerstoffgas. Diese Reaktion gibt SO2 und Wasser. Im Allgemeinen wirkt H2S -Gas als Reduktionsmittel, da es nur einer Oxidation erfahren kann, da sich das Schwefelatom in dieser Verbindung in seinem geringsten Oxidationszustand befindet (kann nicht weiter reduziert werden).

Abbildung 01: Struktur von H2S -Gas
Wir können H2S verwenden, um elementaren Schwefel zu erhalten. Die Reaktion zwischen H2S und SO2 in Gegenwart eines Katalysators und hoher Temperatur ergibt einen elementaren Schwefel und Wasser. Dies ist eine wichtige Methode, um H2S zu entsorgen. Darüber hinaus ist H2S leicht wasserlöslich und kann bei Auflösung eine schwache Säure bilden.
H2s können mit Metallen reagieren und Metallsulfide bilden. Diese Metallsulfide sind wasserunlösliche Verbindungen mit dunklen Farben. Zum Beispiel können wir ein Lead (II) -Acetat -Applied Papier verwenden, um H2S zu erkennen, die sich aus einer Probe entwickeln.
Was ist SO2?
SO2 ist Schwefeldioxid. Es ist ein giftiges Gas, das farblos ist und den Geruch von verbrannten Spielen hat. In der Natur wird dieses Gas aus vulkanischen Ausbrüchen entwickelt. Die Molmasse dieses Gases beträgt 64.8 g/mol. Es ist leicht wasserlöslich und bei der Auflösung bildet es schwefelische Säure. Darüber hinaus kann dieses Gas sowohl Oxidations- als auch Reduktionsreaktionen erfahren. Daher kann SO2 sowohl als Reduktionsmittel als auch als Oxidationsmittel wirken.
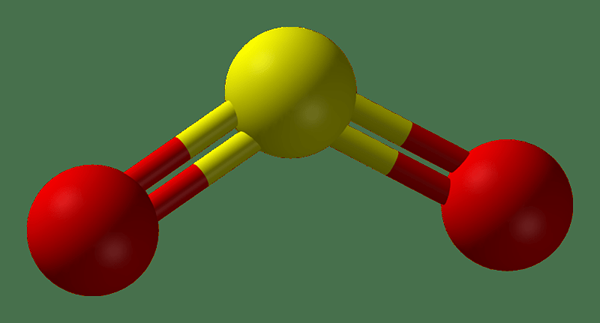
Abbildung 02: Struktur von SO2 -Gas
Bei der Betrachtung der Produktion von SO2 wird es hauptsächlich aus der Schwefelsäure hergestellt. Darüber hinaus ist SO2 Gas das Produkt des brennenden Schwefels (oder des Brennmaterials, das Schwefel enthalten). Darüber hinaus ist dieses Gas ein Nebenprodukt der Herstellung von Calciumsilikatzement. Wir können SO2 aus der Reaktion einer wässrigen Basis mit SO2 produzieren.
Was ist der Unterschied zwischen H2S und SO2?
Sowohl H2S als auch SO2 sind gasförmige Verbindungen bei Raumtemperatur. Der wichtigste Unterschied zwischen H2S und SO2 besteht darin, dass H2S den Geruch eines faulen Eies hat, während SO2 den Geruch eines verbrannten Matchs hat. Daher haben diese beiden Gase einen scharfen Geruch. Außerdem können wir H2s über die Trennung von Sauergas produzieren, während wir SO2 als Nebenprodukt aus Schwefelsäure herstellen können.
Bei der Betrachtung der Verwendung dieser Gase können wir H2S für die Herstellung von elementaren Schwefel, bei der qualitativen Analyse von Metallen, als Vorläufer von Metallsulfiden usw. verwenden., Während SO2 als Vorläufer für Schwefelsäure, als Lebensmittelzusatz, als Reduktionsmittel, in der Weinherstellung usw. nützlich ist, usw.
Nachfolgend Infografik fasst den Unterschied zwischen H2S und SO2 zusammen.
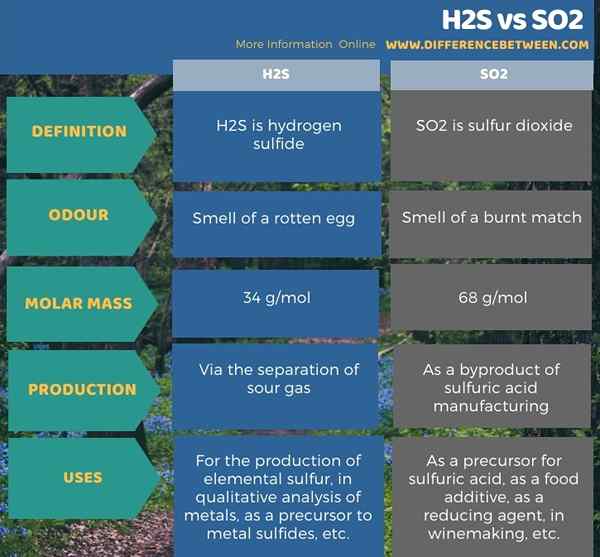
Zusammenfassung -H2S gegen SO2
Sowohl H2S als auch SO2 sind gasförmige Verbindungen bei Raumtemperatur. Der wichtigste Unterschied zwischen H2S und SO2 besteht darin, dass H2S den Geruch eines faulen Eies hat, während SO2 den Geruch eines verbrannten Matchs hat.
Referenz:
1. Helmenstine, Anne Marie, „10 interessante Schwefelfakten.”Thoughtco, Oktober. 8, 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Wasserstoff-Sulfid-3D-Balls" von Ben Mills-eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Schwefel-Dioxid-3D-Balls" von Ben Mills-eigene Arbeit (Public Domain) über Commons Wikimedia


