Unterschied zwischen Hydratation und Hydrierung
Der Schlüsselunterschied Zwischen Hydratation und Hydrierung ist das Hydratation bezieht sich auf die Zugabe von Wassermolekülen zu einer organischen Verbindung.
Hydratation und Hydrierung sind wichtig für chemische Synthesereaktionen. Beide Reaktionen beinhalten das Öffnen einer Doppelbindung in einer organischen Verbindung durch Zugabe eines Substituenten der Kohlenstoffatome in der Doppelbindung. Die in diesen Prozessen hinzugefügten Substituenten unterscheiden sich voneinander.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist Flüssigkeitszufuhr
3. Was ist Hydrierung
4. Seite für Seitenvergleich -Hydratation gegen Hydrierung in tabellarischer Form
5. Zusammenfassung
Was ist Flüssigkeitszufuhr?
Hydratation ist die Zugabe eines Wassermoleküls zu einer organischen Verbindung. Die organische Verbindung ist normalerweise ein Alken, das eine doppelte Bindung zwischen zwei Kohlenstoffatomen hat. Das Wassermolekül wird dieser Doppelbindung in Form einer Hydroxylgruppe (OH-) und ein Proton (h+). Daher dissoziiert das Wassermolekül vor dieser Zugabe in seine Ionen. Die Hydroxylgruppe ist an ein Kohlenstoffatom der Doppelbindung angebracht, während das Proton an das andere Kohlenstoffatom befestigt ist.
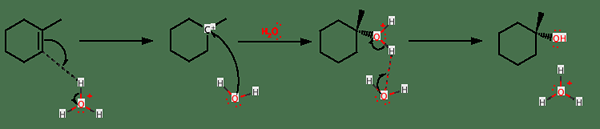
Abbildung 01: Eine einfache Hydratationsreaktion
Da es sich um Bindungsunterbrechung und Bindungsform beinhaltet, ist die Reaktion sehr exotherm. Das bedeutet; Die Reaktion setzt Energie in Form von Wärme frei. Es ist eine schrittweise Reaktion; Im ersten Schritt wirkt das Alken als Nucleophil und greift das Proton des Wassermoleküls an und binde durch das weniger substituierte Kohlenstoffatom mit ihm. Hier folgt die Reaktion der Markonikov -Regel.
Der zweite Schritt beinhaltet die Befestigung des Sauerstoffatoms des Wassermoleküls an das andere Kohlenstoffatom (hochsetztes Kohlenstoffatom) der Doppelbindung. Zu diesem Zeitpunkt trägt das Sauerstoffatom des Wassermoleküls eine positive Ladung, da es drei einzelne Bindungen trägt. Dann kommt ein weiteres Wassermolekül, das das zusätzliche Proton des angebrachten Wassermoleküls aufnimmt und die Hydroxylgruppe am weniger substituierten Kohlenstoffatom bleibt. Somit führt diese Reaktion zur Bildung eines Alkohols. Alkine (Dreifachbindungen mit Kohlenwasserstoffen) können jedoch auch einer Hydratationsreaktion unterzogen werden.
Was ist Hydrierung?
Hydrierung ist der Prozess der Zugabe eines Wasserstoffmoleküls zu einer organischen Verbindung. Darüber hinaus beinhaltet diese Reaktion die Behandlung einer organischen Verbindung mit Wasserstoffgas. Normalerweise tritt die Reaktion in Gegenwart eines Katalysators wie Nickel, Palladium oder Platin auf. Nicht katalytische Hydrationen sind nur bei sehr hohen Temperaturen möglich. Auch dieser Prozess ist wichtig für die Verringerung ungesättigter organischer Verbindungen. Das bedeutet; Die Hydrierung kann Doppelbindungen oder Dreifachbindungen in organischen Verbindungen öffnen und sie in Verbindungen verwandeln, die Einzelbindungen enthalten.
Der Prozess der Hydrierung hat drei Komponenten: ungesättigter Substrat, Wasserstoffquelle und Katalysator. Die Reaktionsbedingungen wie Temperatur und Druck variieren je nach Art der ungesättigten Verbindung und des Katalysators. Das Substrat kann entweder ein Alken oder ein Alkin sein. Die Hydrierung kann auf zwei Arten stattfinden: homogene Katalyse und heterogene Katalyse.
In der homogenen Katalyse bindet das Katalysatormetall sowohl mit Alken als auch mit Wasserstoff, um ein Zwischenprodukt zu ergeben (Alken-Katalysator-Wasserstoff-Zwischenkomplex). Dann tritt die Übertragung eines Wasserstoffatoms von Metall auf Kohlenstoff in der Doppelbindung (oder der Dreifachbindung) auf. Was als nächstes passiert, ist die Übertragung des anderen Wasserstoffatoms von der Wasserstoffquelle auf die Alkylgruppe mit gleichzeitiger Dissoziation des Alkans.

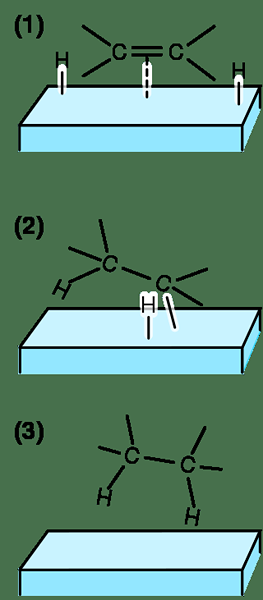
Abbildung 02: Drei Schritte der Hydrierung
In der heterogenen Katalyse bindet die ungesättigte Bindung mit dem Katalysator, während die Wasserstoffquelle eine Dissoziation in zwei Wasserstoffatome unterzieht. Dann tritt ein reversibler Schritt auf, bei dem ein Wasserstoffatom an die ungesättigte Bindung bindet. Schließlich tritt eine irreversible Reaktion auf, bei der sich das andere Wasserstoffatom an die Alkylgruppe befindet.
Was ist der Unterschied zwischen Hydratation und Hydrierung?
Hydratation und Hydrierung sind wichtige Prozesse in der chemischen Synthese. Der Schlüsselunterschied zwischen Hydratation und Hydrierung besteht darin, dass die Hydratation auf die Zugabe von Wassermolekülen zu einer organischen Verbindung bezieht, während die Hydrierung auf die Zugabe eines Wasserstoffmoleküls zu einer organischen Verbindung bezieht.
Die folgende Infografik fasst den Unterschied zwischen Hydratation und Hydrierung zusammen.
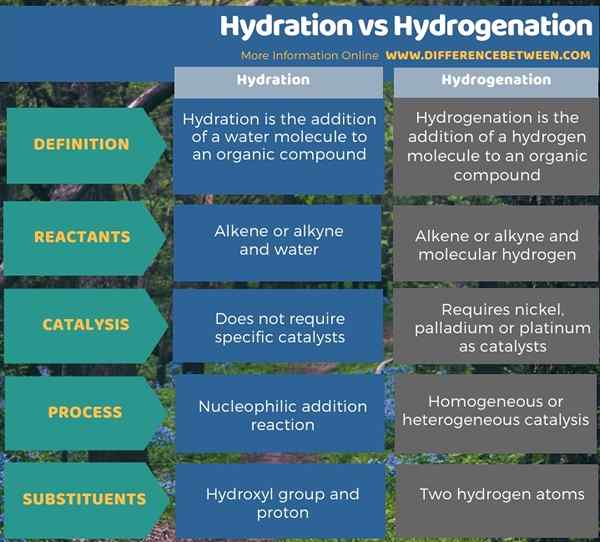
Zusammenfassung -Hydratation gegen Hydrierung
Hydratation und Hydrierung sind wichtige Prozesse in der chemischen Synthese. Der Schlüsselunterschied zwischen Hydratation und Hydrierung besteht darin, dass die Hydratation auf die Zugabe von Wassermolekülen zu einer organischen Verbindung bezieht, während die Hydrierung auf die Zugabe eines Wasserstoffmoleküls zu einer organischen Verbindung bezieht.
Referenz:
1. „Spezifikation für ionselektive Elektroden, Referenzelektroden, Kombinationselektroden und ionselektive Elektrodenmesser zur Bestimmung von Ionen in Lösung.”Doi: 10.3403/00222406U.
Bild mit freundlicher Genehmigung:
1. "HydrationRection" von Ccroberts - eigene Arbeit (Public Domain) über Commons Wikimedia
2. "Hydrierung auf Katalysator" von Michael Schmid - Zeichnung habe selbst geschaffen (CC BY -SA 4.0) über Commons Wikimedia


