Unterschied zwischen Latimer -Diagramm und Frostdiagramm
Der Schlüsselunterschied Zwischen dem Latimer -Diagramm und dem Frostdiagramm ist das Das Latimer -Diagramm fasst die Standard -Elektrodenpotentiale eines chemischen Elements zusammen, während das Frostdiagramm die relative Stabilität verschiedener Oxidationszustände einer Substanz zusammenfasst.
Latimer -Diagramm und Frostdiagramm sind im Grunde wichtig, um Details zu Redoxreaktionen anzuzeigen. Darüber hinaus wurden diese Diagramme nach den Wissenschaftlern benannt, die sie ursprünglich geschaffen haben; Das Latimer -Diagramm hatte seinen Namen von Wendell Mitchell Latimer, während das Frostdiagramm nach Arthur Atwater Frost benannt wurde.
INHALT
1. Überblick und wichtiger Unterschied
2. Was ist das Latimer -Diagramm
3. Was ist Frostdiagramm
4. Seite für Seitenvergleich - Latimer -Diagramm gegen Frostdiagramm in tabellarischer Form
5. Zusammenfassung
Was ist das Latimer -Diagramm?
Latimer -Diagramm ist eine Zusammenfassung der Standard -Elektrodenpotentiale eines Elements. Das Diagramm ist nach dem amerikanischen Chemiker Wendell Mitchell Latimer benannt. Wenn wir diese Art von Diagrammen konstruieren, sollten wir die stark oxidierte Form des chemischen Elements auf der linken Seite schreiben. Dann können wir die Oxidationszustände in absteigender Reihenfolge nach links schreiben - die linke Ecke hat den geringsten Oxidationszustand. Zwischen diesen Oxidationszuständen verwenden wir einen Pfeil (Pfeilspitze links). Darüber hinaus müssen wir oben am Pfeil das Standard -Elektrodenpotential für die Reaktion der Umwandlung des Oxidationszustands auf der rechten Seite auf der linken Seite schreiben. Zum Beispiel,
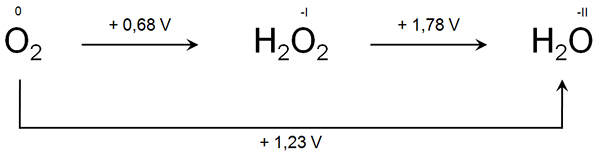
Abbildung 01: Ein Latimer -Diagramm, das die unterschiedlichen Oxidationszustände des Sauerstoffatoms zeigt
Das chemische Element, das wir im obigen Beispiel betrachteten. Es hat die folgenden chemischen Spezies mit entsprechenden Oxidationszuständen von Sauerstoff:
- Ö2 - Der Oxidationszustand ist Null
- H2Ö2 - Der Oxidationszustand des Sauerstoffs beträgt -1
- H2O - Oxidationszustand des Sauerstoffs beträgt -2
Das Latimer-Diagramm ist wichtig für den Bau von Frostdiagramm. Darüber hinaus ist es wichtig, anzuzeigen, ob eine bestimmte chemische Spezies unter den Bedingungen, unter denen das Elektrodenpotential angegeben ist.
Was ist Frostdiagramm?
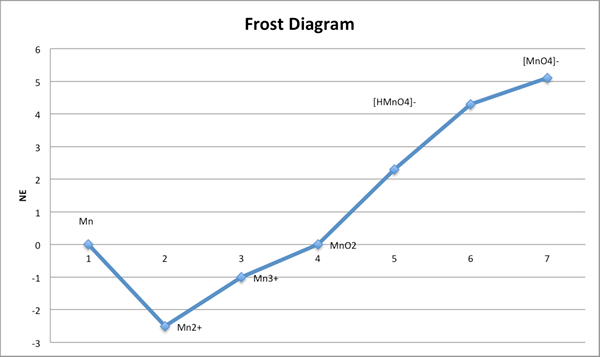
Frostdiagramm ist eine Darstellung, die die relative Stabilität verschiedener Oxidationszustände einer Substanz zeigt. Es ist wichtig für die anorganische Chemie und Elektrochemie. Darüber hinaus ist es ein Diagramm und hat den Oxidationszustand bei der X-Achse und die freie Energie bei der y-Achse. Hier hängt die Grafik vom pH -Wert ab. Daher müssen wir den pH -Wert einbeziehen, an dem wir Messungen durchführen. Wir können die freie Energie mithilfe der Oxidations-Reduktion-Halbreaktionen bestimmen. Darüber hinaus können wir die Reduktionspotentiale leicht anhand dieses Diagramms bestimmen, anstatt ein Latimer -Diagramm zu verwenden.

Abbildung 02: ein Frostdiagramm
Beim Bau des Diagramms müssen wir den Oxidationszustand in der X-Achse und die freie Energie an der y-Achse mit Null in der Mitte markieren. Weil die freie Energie sowohl negative als auch positive Werte hat. Darüber hinaus zeigt die Steigung des Diagramms das Standard -Elektrodenpotential zwischen den beiden Oxidationszuständen.
Was ist der Unterschied zwischen dem Latimer -Diagramm und dem Frostdiagramm?
Latimer -Diagramm und Frostdiagramm sind wichtig, um Informationen über Oxidation und Verringerung der Redoxreaktionen zu bestimmen. Der Hauptunterschied zwischen dem Latimer -Diagramm und dem Frostdiagramm besteht jedoch darin, dass das Latimer -Diagramm die Standard -Elektrodenpotentiale eines chemischen Elements zusammenfasst, das Frostdiagramm jedoch die relative Stabilität verschiedener Oxidationszustände eines Substanz fasst.
Die folgende Infografik fasst den Unterschied zwischen dem Latimer -Diagramm und dem Frostdiagramm in tabellarischer Form zusammen.
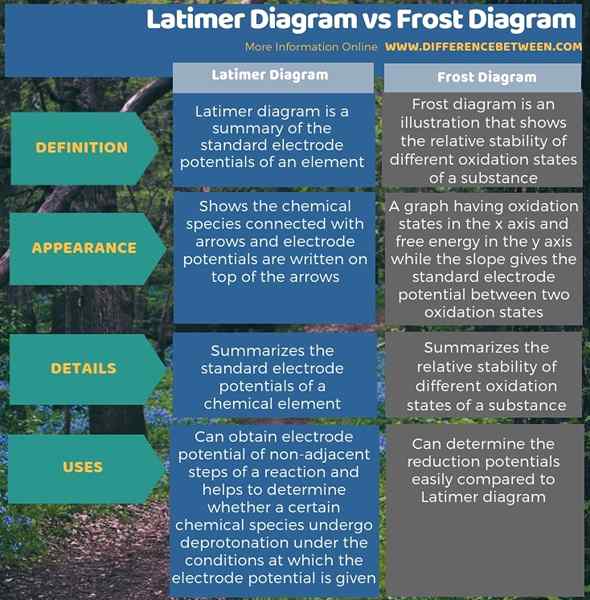
Zusammenfassung -Latimer -Diagramm gegen Frostdiagramm
Insgesamt helfen uns das Latimer -Diagramm und das Frostdiagramm, Informationen über Oxidation und Verringerung der Redoxreaktionen zu bestimmen. Der Hauptunterschied zwischen dem Latimer -Diagramm und dem Frostdiagramm besteht jedoch darin, dass das Latimer -Diagramm die Standard -Elektrodenpotentiale eines chemischen Elements zusammenfasst, während das Frostdiagramm die relative Stabilität verschiedener Oxidationszustände eines Substanz zusammenfasst.
Referenz:
1. „Diagramme, die in Redoxchemie verwendet werden. ”Western Oregon University, hier erhältlich.
2. “4.3: Latimer- und Frostdiagramme.”Chemistry Libretexten, Libretexte, 5. Juni 2019, hier erhältlich.
Bild mit freundlicher Genehmigung:
1. "Latimerdiagram Zuurstof" von Dr.T - eigene Arbeit (CC BY -SA 3.0) über Commons Wikimedia
2. "Frostdiagramm" von JLange1125 - Ich habe das Diagramm in Excel (CC BY -SA 3) gemacht.0) über Commons Wikimedia


